Clear Sky Science · it
Un nuovo metodo con camera a flusso accoppiata all’IA che quantifica la fragilità osmotica degli eritrociti
Perché la fragilità dei globuli rossi è importante
Ogni secondo, milioni di globuli rossi si schiacciano attraverso vasi sottilissimi trasportando ossigeno. Quanto facilmente queste cellule si rompono sotto stress — la loro “fragilità” — può rivelare anemia, problemi nella conservazione del sangue e complicazioni di infezioni gravi come la sepsi. Questo studio presenta un dispositivo moderno, assistito dall’intelligenza artificiale, che misura quanto rapidamente i globuli rossi si disgregano in soluzioni salate, con l’obiettivo di rendere questo test importante più veloce, più preciso e più semplice da eseguire sia nei laboratori di ricerca sia, un giorno, negli ospedali.
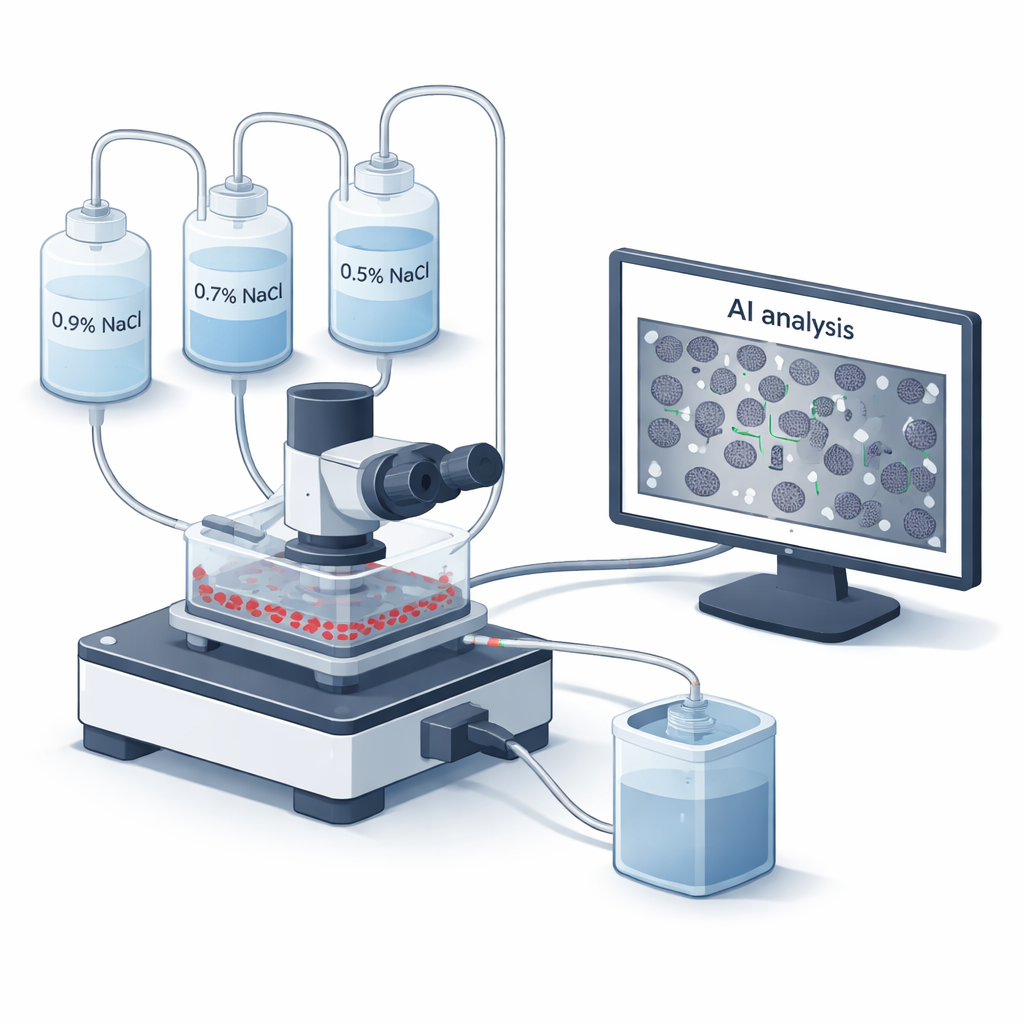
Un nuovo modo di osservare le cellule del sangue sotto stress
I medici usano i test di fragilità osmotica dagli anni Quaranta per valutare quanto siano robuste le membrane dei globuli rossi. Tradizionalmente il sangue viene miscelato con una serie di soluzioni saline e una macchina misura quanto emoglobina fuoriesce quando le cellule si rompono. Pur essendo affidabile, questo metodo classico è lento, manuale e non mostra come appaiono le singole cellule mentre falliscono. Il team dietro questo lavoro ha costruito un nuovo sistema microfluidico a “camera a flusso”, chiamato BioExP, che distribuisce i globuli rossi in uno strato monodimensionale sottile su un vetrino trattato. Diverse soluzioni saline sono pompate attraverso questo strato mentre un microscopio e una videocamera registrano cosa succede in tempo reale, e il software integrato usa l’intelligenza artificiale per contare quante cellule rimangono integre a ciascun livello di salinità.
Mettere alla prova l’IA e il controllo del flusso
Per valutare l’affidabilità di BioExP, i ricercatori lo hanno confrontato direttamente con l’assay spettrofotometrico tradizionale impiegando sangue di quattro donatori sani. Si sono concentrati su un valore chiave chiamato MCF₅₀: la concentrazione di sale alla quale metà dei globuli rossi si è rotta. Prima hanno dovuto ottimizzare il nuovo sistema trovando il miglior “tempo di saturazione” — quanto a lungo esporre le cellule a una data soluzione ipotonica in modo che le cellule più vulnerabili lisciscano senza esagerare. Seguendo quante cellule scomparivano a 0,4% di sale in 15 minuti, hanno rilevato che quasi l’80% dell’emolisi avveniva nei primi tre minuti. Questa finestra di tre minuti è diventata il loro tempo di esposizione standard, bilanciando velocità e misure affidabili.
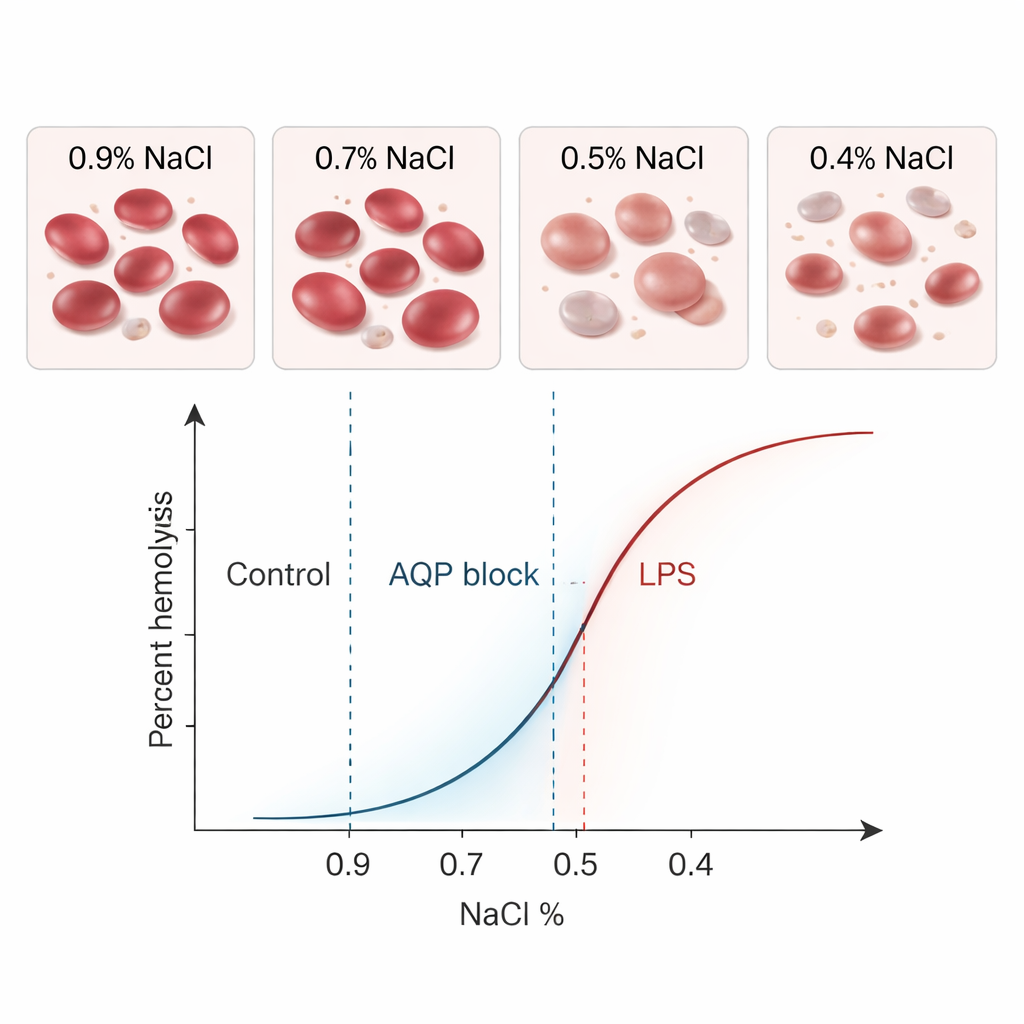
Confrontare il test classico e sondare la biologia reale
Quando hanno processato gli stessi campioni sani con entrambi i metodi, BioExP e il test classico hanno fornito valori medi di MCF₅₀ quasi identici — 0,41% di sale — con variabilità simile. Le analisi statistiche non hanno mostrato differenze rilevanti tra i metodi e la maggior parte dei risultati appaiati rientrava in stretti limiti di concordanza. In altre parole, il nuovo dispositivo “parlava” efficacemente la stessa lingua dell’assay consolidato. Il vero punto di forza di BioExP, tuttavia, sta nella sua capacità di verificare come varie condizioni modifichino la fragilità cellulare. I ricercatori hanno scelto due modificatori biologicamente rilevanti: il cloruro di mercurio, che blocca le proteine canale dell’acqua chiamate acquaporine nella membrana cellulare, e il lipopolisaccaride batterico (LPS), una tossina associata alla sepsi.
Come tossine e canali dell’acqua influenzano la resistenza cellulare
Il blocco delle acquaporine ha reso i globuli rossi più difficili da far scoppiare: l’MCF₅₀ si è spostato verso concentrazioni di sale inferiori, cioè le cellule tolleravano una diluizione maggiore prima di rompersi. Sia BioExP che il metodo classico hanno rilevato chiaramente questo spostamento verso sinistra. LPS ha avuto l’effetto opposto. Quando i globuli rossi sono stati incubati con un’alta dose di LPS in assenza di plasma, sono diventati più fragili, rompendosi a concentrazioni saline più elevate. Al microscopio molte cellule hanno cambiato forma, diventando più sferiche o spinose — segni visivi che le loro membrane erano state disturbate. Anche in questo caso, entrambi i metodi hanno registrato un marcato e statisticamente significativo spostamento verso destra nelle curve di fragilità. In tutti questi test, il nuovo sistema a camera a flusso ha seguito costantemente le stesse tendenze biologiche del metodo tradizionale, con valori assoluti leggermente più bassi ma piccoli e sistematici.
Cosa significa per pazienti e laboratori
La piattaforma BioExP riduce il tempo dell’assay da diverse ore a meno di un’ora, richiede solo volumi di sangue minimi (potenzialmente una semplice puntura del dito) e automatizza il conteggio e l’adattamento delle curve con l’IA invece di fare molti passaggi manuali. Poiché Fotografa le stesse cellule nel tempo, può collegare l’aspetto cellulare alla loro suscettibilità alla rottura e può testare molti livelli di salinità o condizioni farmacologiche in una singola corsa. Lo studio dimostra che questo approccio moderno può eguagliare la precisione del test classico di fragilità osmotica aggiungendo velocità, flessibilità e dettagli visivi ricchi. Se validato ulteriormente su gruppi di donatori più ampi e diversificati, tali sistemi potrebbero diventare strumenti preziosi per diagnosticare anemie emolitiche, monitorare il sangue conservato nelle banche e studiare come infezioni o nuovi farmaci indeboliscano o proteggano i nostri globuli rossi.
Citazione: Fırat, I.S., Alaçayır, Ö., Creutz, T. et al. A novel AI-coupled flow chamber method quantifying erythrocyte osmotic fragility. Sci Rep 16, 7175 (2026). https://doi.org/10.1038/s41598-026-38322-z
Parole chiave: globuli rossi, fragilità osmotica, microfluidica, sepsi, intelligenza artificiale