Clear Sky Science · it
DeepLab V3+ con attenzione multi-livello e EfficientNetB0 per la segmentazione degli organi del tratto gastrointestinale in scansioni MRI
Mirare con più precisione ai tumori
Quando i medici trattano i tumori del sistema digerente con la radioterapia, affrontano un delicato equilibrio: colpire il tumore con decisione risparmiando però gli organi sani vicini come stomaco e intestino. Oggi, delineare manualmente quegli organi su ogni scansione di risonanza magnetica (MRI) può richiedere fino a un’ora per paziente al giorno. Questo studio presenta un sistema di visione artificiale che traccia automaticamente questi organi nelle immagini MRI, promettendo una pianificazione del trattamento più veloce e precisa e meno effetti collaterali per i pazienti.
Perché mappare l’intestino è importante
I tumori gastroenterici sono comuni e spesso letali, con una sopravvivenza complessiva intorno al 30 percento. La radioterapia è una colonna portante del trattamento, ma il tratto digerente è compresso all’interno dell’addome e gli organi sani possono spostarsi leggermente di giorno in giorno. Per evitare di danneggiare stomaco, intestino tenue e intestino crasso, gli specialisti devono sapere esattamente dove si trovano prima di ogni seduta. Il delineamento manuale è lento e soggetto a variazioni tra gli esperti. Un metodo automatico e affidabile per tracciare questi confini potrebbe accorciare le visite, permettere ai medici di trattare più pazienti e migliorare la sicurezza e l’accuratezza delle dosi di radiazione.
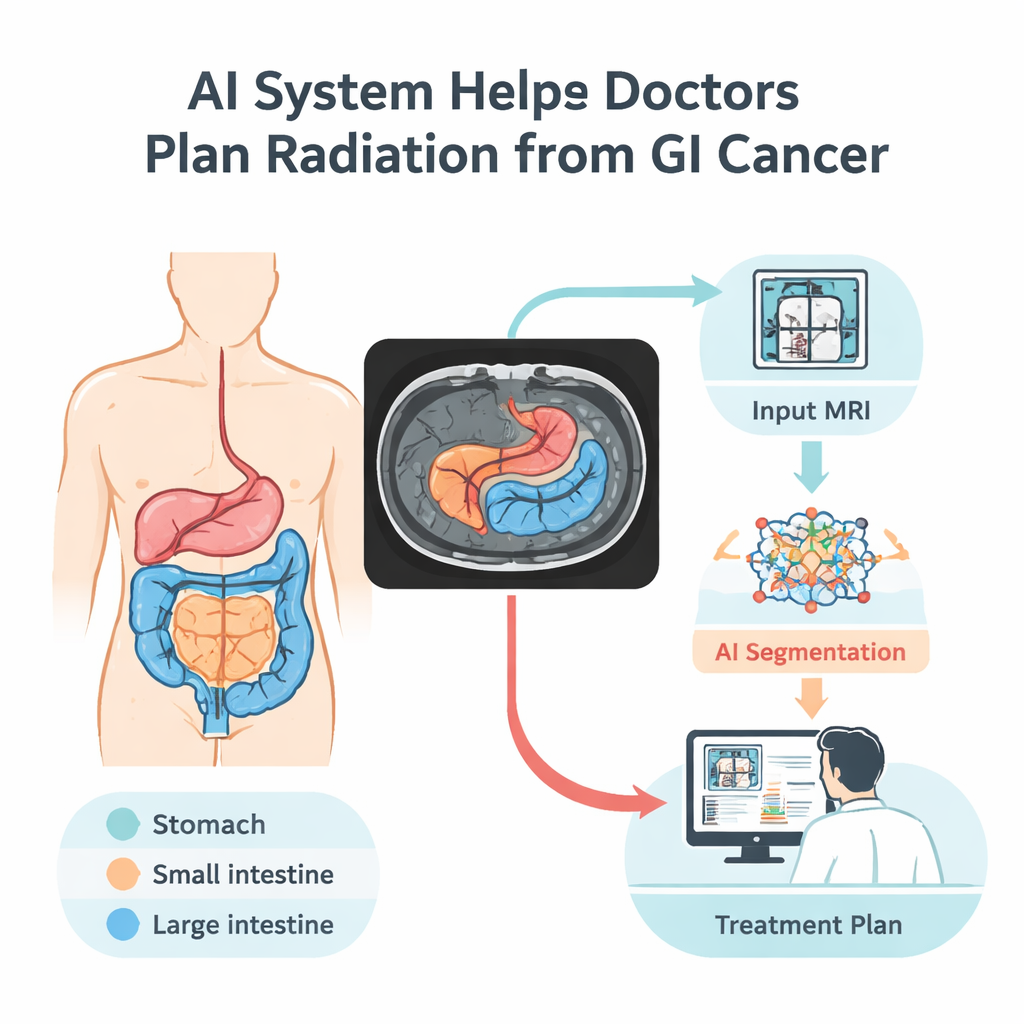
Insegnare ai computer a leggere le scansioni MRI
I ricercatori hanno costruito un modello di intelligenza artificiale che impara a riconoscere tre organi digestivi chiave nelle scansioni MRI: stomaco, intestino tenue e intestino crasso. Lo hanno addestrato sul dataset UW–Madison GI Tract, l’unica raccolta pubblica con contorni organici dettagliati su MRI addominale. Questo dataset include 38.496 immagini provenienti da 85 pazienti, insieme a etichette accuratamente preparate che indicano dove appare ciascun organo — o dove non è presente nessun organo. Per sfruttare al meglio questo campione relativamente piccolo, il gruppo ha suddiviso i dati per paziente (così il modello non vede mai la stessa persona sia nel training sia nel test) e ha ampliato il dataset ribaltando, ruotando, schiarendo e deformando leggermente le immagini. Queste variazioni controllate aiutano il sistema a gestire le differenze reali nella posizione del paziente, nella luminosità delle immagini e nelle sottili variazioni di forma.
Come il nuovo modello AI osserva i pattern
All’interno del modello, diverse idee moderne di riconoscimento delle immagini sono combinate per affinare il suo “sguardo” sull’anatomia. Innanzitutto, una rete compatta chiamata EfficientNet B0 scansiona ogni immagine e costruisce strati di caratteristiche visive — dai bordi semplici alle forme complesse degli organi — mantenendo contenuti i requisiti computazionali. Poi, una struttura nota come DeepLab V3+ osserva l’immagine a più scale, un po’ come zoomare dentro e fuori per comprendere sia i dettagli fini sia il contesto generale. Su questo, gli autori aggiungono un meccanismo di “attenzione” a diversi livelli di dettaglio. In termini semplici, l’attenzione aiuta il sistema a decidere quali parti dell’immagine e quali segnali interni meritano più peso, in modo da concentrarsi su indizi sottili ma importanti che distinguono, per esempio, lo stomaco da anse di intestino tenue. Infine, una fase di decodifica ricompone questi indizi in una maschera pulita e a grandezza originale che mostra i tre organi.
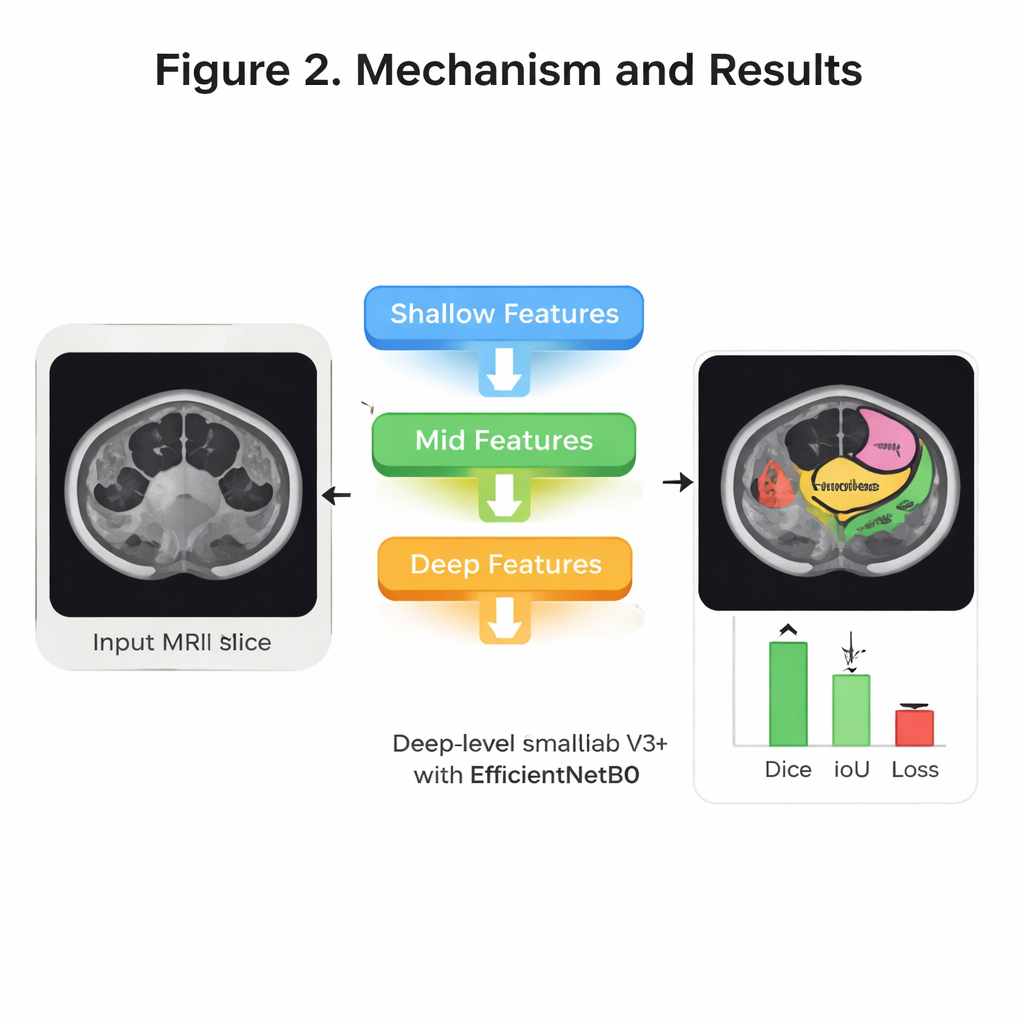
Testare accuratezza ed efficienza
Il team ha ottimizzato in modo sistematico le modalità di addestramento del sistema — provando diversi metodi di ottimizzazione, numeri di cicli di training e modi di suddividere i dati per la validazione. La loro migliore configurazione ha usato un ottimizzatore chiamato RMSprop, una validazione incrociata a quattro fold e 30 epoche di addestramento. Su pazienti di test indipendenti, il modello ha etichettato correttamente più del 99 percento dei pixel complessivi e ha mostrato una forte sovrapposizione con i contorni tracciati dagli esperti. Una misura comunemente usata di sovrapposizione, il punteggio di Dice, ha raggiunto circa il 94 percento in media sui tre organi, mentre una misura correlata, l’Intersection over Union, si è attestata intorno al 92 percento. Altrettanto importante per l’uso ospedaliero, il sistema è relativamente leggero: ha circa 8,3 milioni di parametri addestrabili e può elaborare una tipica fetta MRI 224×224 in circa 31 millisecondi, abbastanza veloce da supportare quasi in tempo reale la pianificazione quotidiana del trattamento.
Cosa potrebbe significare per i pazienti
In termini pratici, questo studio dimostra che un’IA progettata con cura può tracciare in modo affidabile stomaco e intestini nelle immagini MRI, uguagliando le prestazioni degli esperti mentre lavora molto più rapidamente e con maggiore coerenza. Questa capacità potrebbe aiutare gli oncologi radioterapisti ad adattare i fasci con maggiore precisione intorno ai tessuti sensibili, riducendo danni indesiderati ed effetti collaterali durante il trattamento. Anche se il modello attuale è stato addestrato su scansioni di un unico centro e su anatomie prevalentemente sane, fornisce una solida base per futuri sistemi che includano organi malati e dati provenienti da più ospedali. Con ulteriori test e perfezionamenti, strumenti come questo potrebbero diventare assistenti di routine nella sala di pianificazione radioterapica, assicurando in modo discreto che i raggi salvavita colpiscano esattamente dove servono di più.
Citazione: Sharma, N., Gupta, S., Al-Yarimi, F.A.M. et al. Multi-level attention DeepLab V3+ with EfficientNetB0 for GI tract organ segmentation in MRI scans. Sci Rep 16, 7546 (2026). https://doi.org/10.1038/s41598-026-38247-7
Parole chiave: cancro gastrointestinale, segmentazione MRI, pianificazione della radioterapia, apprendimento profondo in medicina, analisi di immagini mediche