Clear Sky Science · it
L’inibizione della via SHH e la co-coltura con astrociti inducono risposte distinte in glioblastoma e nelle cellule staminali tumorali
Perché i tumori cerebrali sono così difficili da trattare
Il glioblastoma è uno dei tumori cerebrali più letali e, nonostante chirurgia, radioterapia e chemioterapia, solo una piccola frazione di pazienti supera i cinque anni di sopravvivenza. Un motivo è che questi tumori non sono composti da un unico tipo di cellula. Contengono un piccolo gruppo di cellule particolarmente tenaci, le cosiddette “cellule staminali tumorali”, che possono sopravvivere ai trattamenti e favorire la ricrescita del tumore. Questo studio pone una domanda chiave: come rispondono i diversi tipi cellulari del tumore quando viene bloccato un segnale che stimola la crescita, e in che modo la presenza di cellule cerebrali normali di supporto, chiamate astrociti, modifica questa risposta?
Uno sguardo più da vicino alle cellule più resistenti del tumore
I ricercatori hanno lavorato con due principali tipi cellulari provenienti da un modello comune di glioblastoma: le cellule del tumore in massa e una piccola sotto‑popolazione marcata dalla proteina CD133, che si comporta come cellule staminali tumorali. Queste cellule di tipo staminale si dividevano meno, apparivano più piccole e tondeggianti e formavano gruppi più compatti rispetto alle cellule di massa. Il gruppo ha inoltre coltivato le cellule tumorali insieme agli astrociti, le cellule a forma di stella che contribuiscono a mantenere il tessuto cerebrale sano. Questa coltura mista imita meglio l’ambiente tumorale reale, dove le cellule cancerose “parlano” continuamente con i loro vicini. 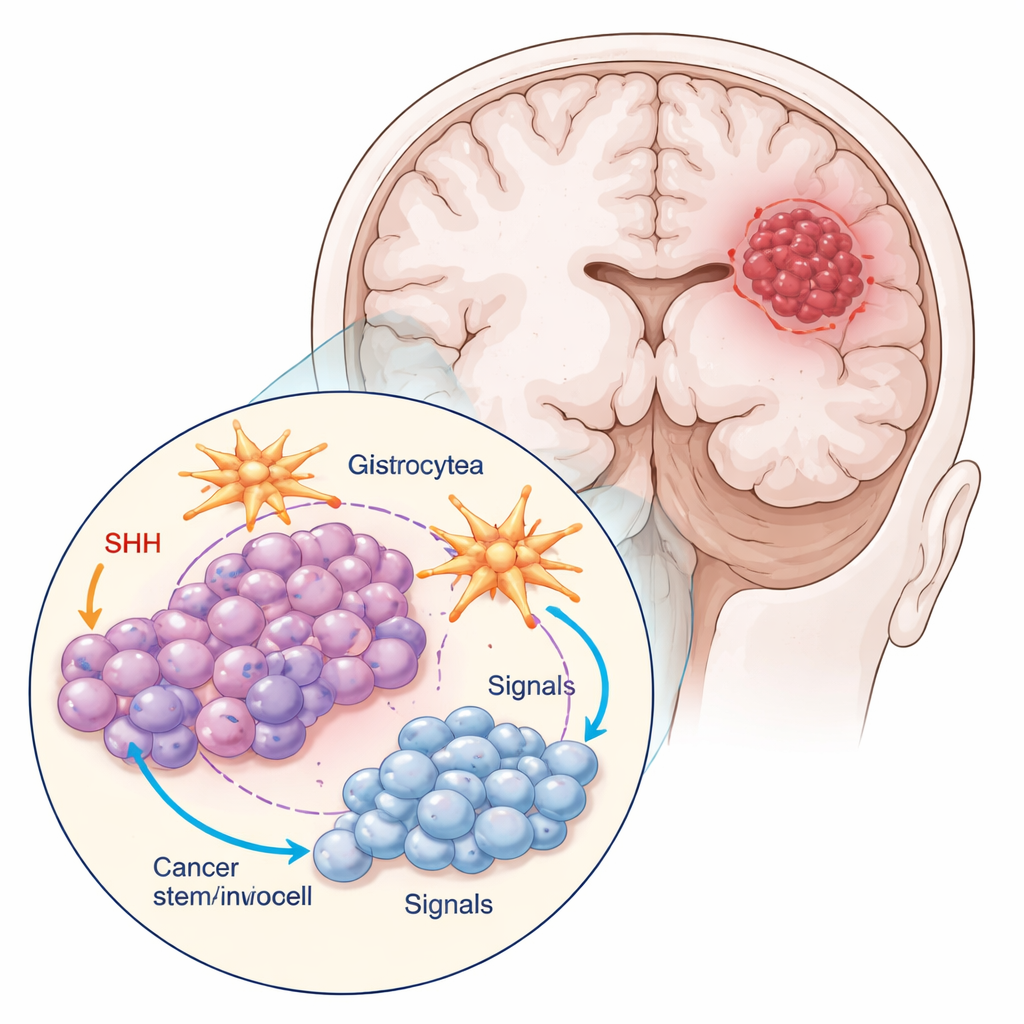
Bloccare un segnale dello sviluppo che i tumori riutilizzano
Molti glioblastomi, in particolare le loro cellule di tipo staminale, dirottano una via di comunicazione molecolare chiamata Sonic Hedgehog (SHH), normalmente attiva durante lo sviluppo cerebrale. Il gruppo ha usato la ciclopamina, un composto che blocca un componente chiave di SHH, per vedere come rispondessero sia le cellule tumorali di massa sia le cellule staminali tumorali. Hanno misurato l’attività di geni e proteine legati a SHH, la velocità con cui le cellule transitavano nel ciclo cellulare e la frequenza con cui subivano la morte programmata (apoptosi). La ciclopamina modificava la segnalazione SHH in modo fortemente dipendente dal tipo cellulare e dalla presenza di astrociti. Le cellule staminali tumorali producevano il segnale SHH più intensamente quando crescevano da sole, ma questa secrezione diminuiva quando erano coltivate con astrociti e trattate con il farmaco, suggerendo che le cellule cerebrali circostanti possono attenuare il “sostegno chimico” del tumore.
Come il vicinato modifica crescita e morte
Oltre a SHH, il gruppo ha seguito altre reti geniche che dirigono se le cellule continuano a dividersi, si arrestano o iniziano a specializzarsi. In colture semplici contenenti solo il tumore, il blocco di SHH spingeva le cellule di massa verso un arresto nella fase finale della divisione (fase G2/M), mentre le cellule di tipo staminale tendevano ad accumularsi nelle fasi iniziali o di riposo (G0/G1). Con l’aggiunta degli astrociti questi schemi cambiavano: le cellule staminali tumorali, che erano più quiescenti, si spostavano verso un arresto in G2/M, implicando un diverso insieme di “freni” applicati nell’ambiente misto. I ricercatori hanno inoltre osservato che segnali collegati al destino cellulare e alla morfogenesi tissutale — come le vie WNT, BMP e TGF‑β — venivano modulati differentemente nelle cellule di massa e in quelle staminali quando erano presenti astrociti, il che significa che il microambiente può inclinare le cellule verso un mantenimento dello stato staminale o verso una maggiore differenziazione e minore aggressività.
Indurre la morte nelle cellule più resistenti
Lo studio ha esaminato anche la propensione delle cellule ad andare incontro ad apoptosi. Letture genetiche e un test di rilevamento del danno al DNA (saggio TUNEL) hanno mostrato che la ciclopamina favoriva una via “esterna” della morte cellulare, mediata da una proteina chiamata CASP8, in particolare nella popolazione di cellule staminali tumorali. Interessante è che, nelle cellule tumorali coltivate da sole, la mortalità complessiva a volte diminuiva dopo il blocco di SHH, suggerendo che queste cellule potessero attivare strategie di sopravvivenza alternative. Al contrario, quando le cellule di tipo staminale erano co‑coltivate con astrociti, la ciclopamina aumentava i marcatori di apoptosi, indicando che le cellule cerebrali circostanti possono rendere queste cellule altrimenti resistenti più vulnerabili una volta bloccata la segnalazione SHH. 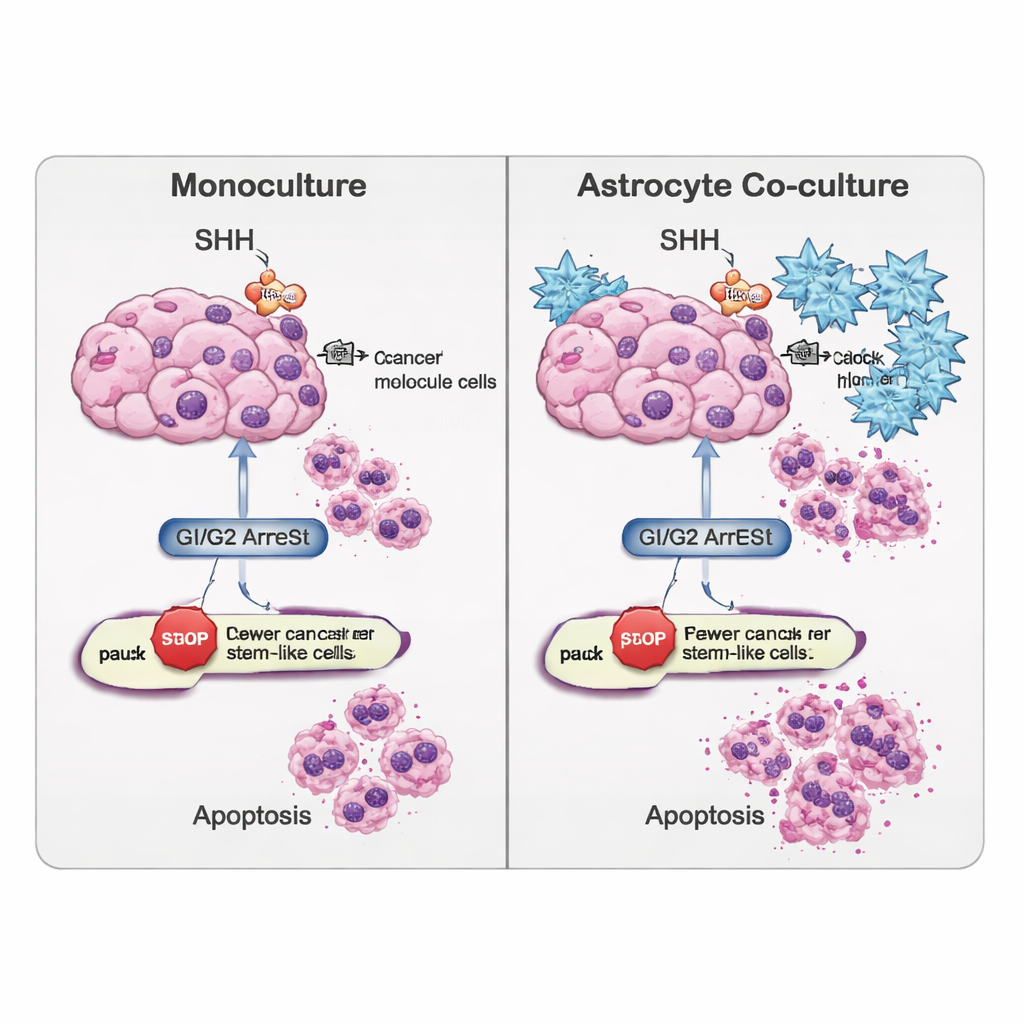
Cosa significa per i futuri trattamenti del cancro cerebrale
Per un pubblico non specialista, il messaggio principale è che mirare a un singolo segnale di crescita nel glioblastoma non basta se si ignora il “vicinato” del tumore. Questo lavoro mostra che gli astrociti — le cellule normali che condividono lo spazio con il tumore — possono cambiare profondamente come sia le cellule tumorali di massa sia le cellule staminali tumorali rispondono al blocco della via SHH. In particolare, le cellule staminali tumorali diventavano più inclini all’arresto del ciclo cellulare e a una forma di morte cellulare quando erano in presenza di astrociti. Gli autori concludono che i farmaci diretti contro SHH e vie correlate avranno maggiori probabilità di funzionare se testati e infine impiegati in modi che riflettano l’ambiente cerebrale reale, possibilmente in combinazione con altri trattamenti che attaccano le vie di sopravvivenza di riserva del tumore. In breve, comprendere e sfruttare la “conversazione” tra cellule tumorali e vicini potrebbe aprire strategie più precise e durature contro questo cancro altrimenti implacabile.
Citazione: Kocaturk, D.C., Ozdil, B., Adali, Y. et al. SHH pathway inhibition and astrocyte co-culture induce distinct responses in glioblastoma and cancer stem cells. Sci Rep 16, 7712 (2026). https://doi.org/10.1038/s41598-026-38199-y
Parole chiave: glioblastoma, cellule staminali tumorali, via Sonic Hedgehog, microambiente tumorale, astrociti