Clear Sky Science · it
Obinutuzumab induce la destabilizzazione lisosomiale tramite inibizione di TRPML2 dipendente dalla sfingomielina
Perché questa storia sugli anticorpi è importante
Per molte persone con linfomi delle cellule B, i farmaci anticorpali moderni hanno trasformato una diagnosi un tempo uniformemente letale in una malattia trattabile. Tuttavia non tutti gli anticorpi sono uguali: alcuni uccidono le cellule tumorali in modo più potente e più affidabile di altri. Questo studio esplora perché un farmaco in particolare, l’obinutuzumab, è più efficace nel provocare la morte diretta delle cellule di linfoma rispetto al suo predecessore rituximab, concentrandosi su un colpevole inaspettato nel profondo della cellula — i centri di riciclo della cellula stessa, chiamati lisosomi, e il delicato equilibrio di lipidi e canali ionici nelle loro membrane.
Dal bersaglio di superficie all’autodistruzione interna
Sia il rituximab sia l’obinutuzumab riconoscono lo stesso bersaglio sulle cellule B, una proteina chiamata CD20. Ma gli autori dimostrano che l’obinutuzumab viene internalizzato nella cellula molto più rapidamente ed efficacemente. Una volta legati a CD20 sulla superficie delle cellule tumorali, i complessi anticorpo‑recettore vengono richiamati all’interno tramite un processo endocitico e dirigiti verso compartimenti acidi, compresi i lisosomi. Lì, l’obinutuzumab induce la permeabilizzazione della membrana lisosomiale: la membrana lisosomiale, normalmente robusta, diventa porosa, consentendo a enzimi digestivi come le catepsine di fuoriuscire nella cellula e attivare vie di morte cellulare. Alterazioni nell’equilibrio di sali e acqua di questi compartimenti, che causano il rigonfiamento dei lisosomi, amplificano notevolmente questo effetto letale.
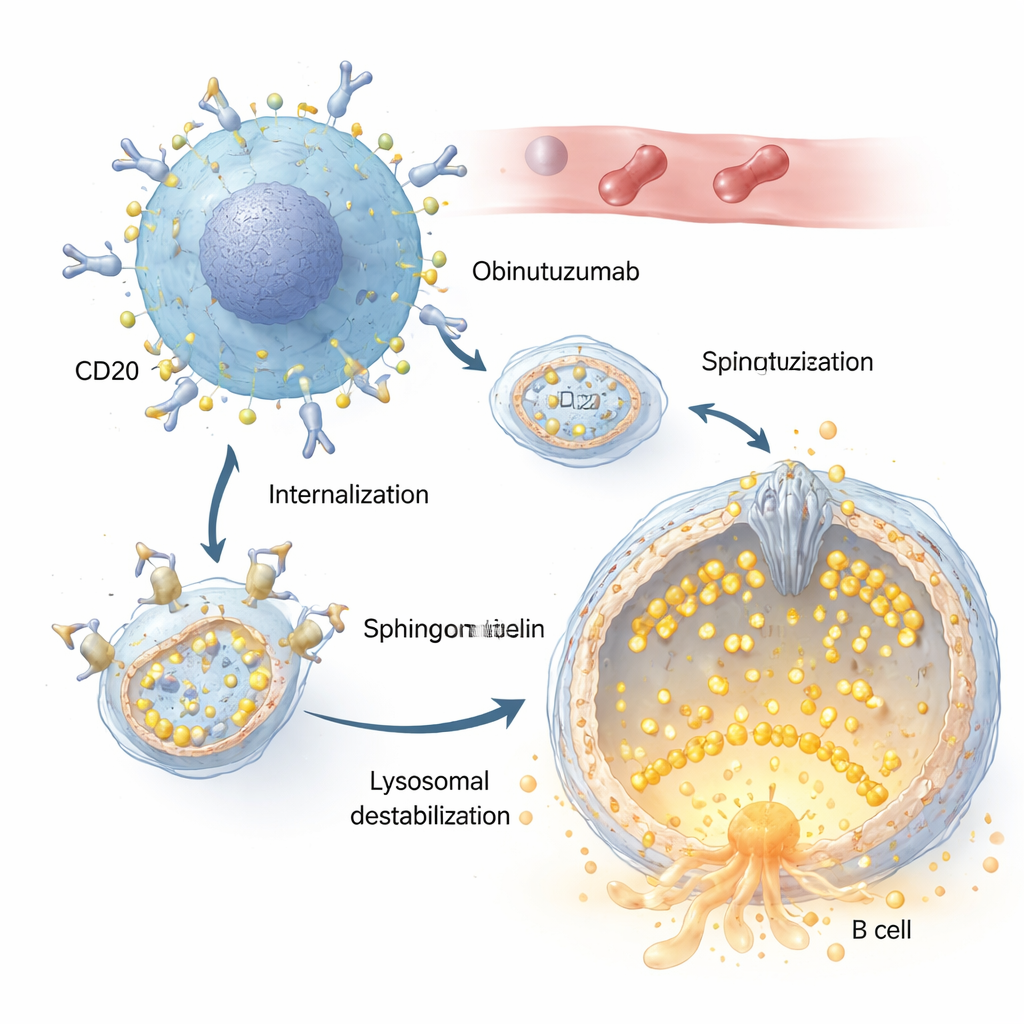
Il ruolo di un minuscolo canale guardiano
Al centro di questa storia c’è TRPML2, un canale del calcio inserito nella membrana lisosomiale. In condizioni normali, TRPML2 aiuta i lisosomi a far fronte allo stress meccanico e osmotico rilasciando calcio, il quale sostiene la riparazione della membrana, il traffico intracellulare e il controllo del volume. Utilizzando una combinazione di sonde fluorescenti per il calcio e versioni ingegnerizzate di TRPML2 sensibili al calcio, i ricercatori mostrano che l’obinutuzumab spegne rapidamente questo canale: nel giro di pochi minuti dal trattamento, un agente che normalmente apre i canali TRPML non induce più il rilascio di calcio. Approcci genetici che riducono i livelli di TRPML2, oppure inibitori a piccola molecola che bloccano l’attività dei TRPML, rendono entrambi le cellule di linfoma più vulnerabili all’obinutuzumab, portando a maggiore perdita di integrità lisosomiale e a tassi più elevati di morte cellulare diretta.
Come i lipidi di membrana inclinano l’equilibrio
Lo studio indaga poi cosa collega l’internalizzazione degli anticorpi allo spegnimento del canale. L’attenzione si sposta sulla sfingomielina, un lipide (grasso) abbondante nelle membrane cellulari e noto per interferire con i canali TRPML. Usando una sonda fluorescente che si lega alla sfingomielina, gli autori rilevano che le vescicole contenenti obinutuzumab sono ricche di sfingomielina una volta raggiunti i compartimenti acidi, molto più di quelle contenenti rituximab. Quando le cellule vengono trattate con la sfingomielinasi, un enzima che riduce la sfingomielina, l’attività di rilascio di calcio di TRPML2 si ripristina anche in presenza di obinutuzumab. In queste condizioni i lisosomi sono meno inclini a perdere integrità e muoiono meno cellule, suggerendo con forza che l’accumulo di sfingomielina disabilita TRPML2 e predispone i lisosomi alla rottura.
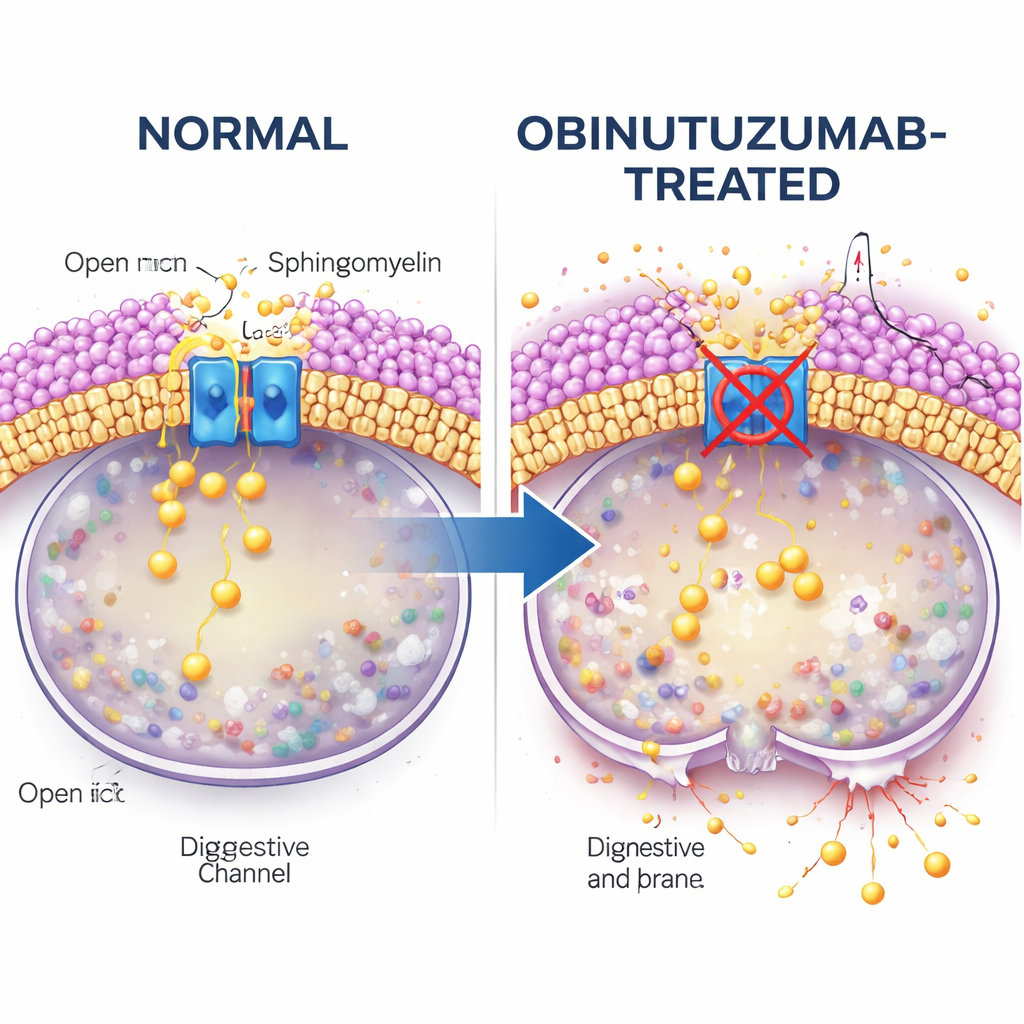
Rotte di traffico e checkpoint del colesterolo
Anche il percorso che l’obinutuzumab segue per entrare nella cellula è importante. La microscopia elettronica e la marcatura anticorpale sensibile al pH rivelano che l’obinutuzumab lascia la superficie cellulare ed entra nelle vescicole intracellulari più rapidamente rispetto al rituximab. Quando i ricercatori interferiscono con rotte di captazione specifiche, scoprono che bloccare una forma di endocitosi dipendente dal colesterolo (con un composto chiamato filipina) impedisce all’obinutuzumab di spegnere TRPML2 e riduce parzialmente il danno lisosomiale e la morte cellulare. Altri inibitori dell’endocitosi non producono questo effetto protettivo. Ciò indica l’esistenza di una via specializzata, ricca di colesterolo e sfingomielina, che consegna l’obinutuzumab ai lisosomi in modo tale da innescare l’inibizione di TRPML2 e la successiva destabilizzazione della membrana.
Cosa significa questo per i futuri trattamenti del cancro
In termini semplici, questo lavoro mostra che l’obinutuzumab uccide i linfomi delle cellule B così efficacemente perché costringe i loro lisosomi in uno stato fragile. Portando i complessi anticorpo–CD20 in compartimenti ricchi di sfingomielina, il farmaco spegne indirettamente un canale protettivo del calcio, TRPML2. Una volta che questa salvaguardia viene meno, i lisosomi sono più propensi a rompersi sotto stress, riversando enzimi corrosivi che smantellano la cellula tumorale dall’interno. Comprendere questo asse lipide–canale ionico spiega non solo perché l’obinutuzumab supera il rituximab, ma suggerisce anche nuove strategie per potenziare le terapie anticorpali — per esempio combinandole con farmaci che modificano gli sfingolipidi o che aumentano l’attività di TRPML2 per modulare con precisione quando e come i lisosomi delle cellule tumorali si autodistruggono.
Citazione: Oh, J., Jin, N., Kwon, S. et al. Obinutuzumab induces lysosomal destabilization via sphingomyelin-dependent inhibition of TRPML2. Sci Rep 16, 7079 (2026). https://doi.org/10.1038/s41598-026-38087-5
Parole chiave: obinutuzumab, linfoma delle cellule B, lisosoma, sfingomielina, TRPML2