Clear Sky Science · it
Proprietà funzionali delle vescicole extracellulari derivate da miotubi scheletrici basate sui profili di microRNA: un’analisi comparativa con vescicole extracellulari derivate da cellule staminali mesenchimali
Messaggi muscolari in piccoli pacchetti
I nostri muscoli fanno molto più che muoverci: inviano costantemente “messaggi” molecolari in tutto il corpo. Questo studio esplora come le particelle minute rilasciate dalle cellule muscolari si confrontano con particelle simili provenienti da cellule staminali ampiamente usate per future terapie. Decodificando i segnali genetici trasportati da queste particelle, gli autori pongono una domanda pratica: per quali tipi di malattie le particelle derivate dal muscolo potrebbero essere migliori rispetto a quelle derivate da cellule staminali?
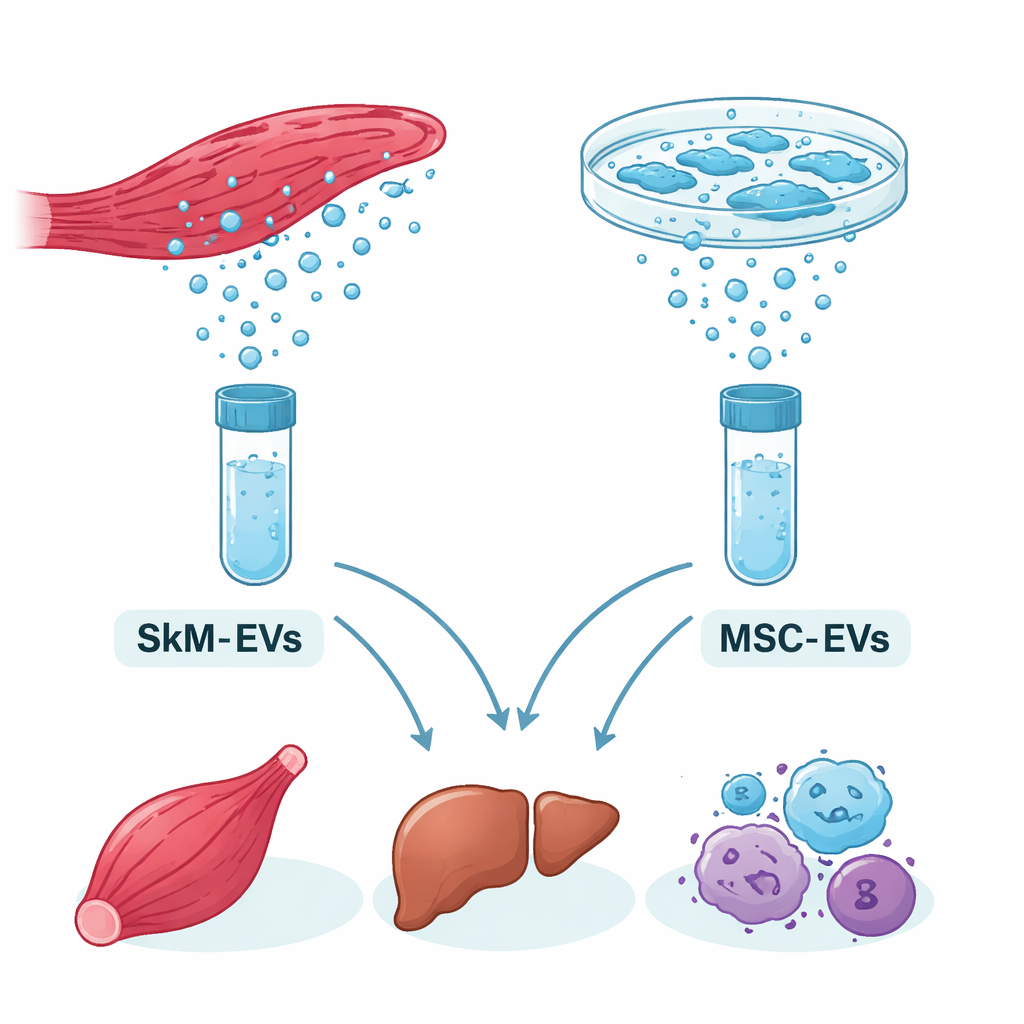
Piccoli corrieri in viaggio nel corpo
Tutte le cellule rilasciano bolle microscopiche chiamate vescicole extracellulari, o EV. Si tratta di pacchetti a scala nanometrica avvolti da lipidi e carichi di molecole. Un tipo chiave di carico sono i microRNA — brevi frammenti di RNA che aiutano a modulare l’espressione genica, plasmando il comportamento cellulare. Il muscolo scheletrico, il tessuto che alimenta il movimento, risulta essere il più grande organo secretore del corpo e può rilasciare grandi quantità di EV, specialmente se stimolato con metodi non invasivi come gli ultrasuoni. Le cellule staminali mesenchimali, invece, sono già ampiamente impiegate negli studi clinici, e le loro EV sono testate per la riparazione tissutale e la modulazione dell’infiammazione.
Leggere il codice genetico del carico
Invece di testare le EV direttamente in animali o persone, i ricercatori hanno rianalizzato dataset di sequenziamento esistenti che catalogano quali microRNA sono presenti nelle EV provenienti da miotubi scheletrici di topo (fibre muscolari coltivate in laboratorio) e da cellule staminali mesenchimali derivate dal midollo osseo. Le EV muscolari avevano alcuni microRNA dominanti, come miR-206-3p e miR-378a-3p, che costituivano oltre il 60 percento del loro carico, mentre le EV delle cellule staminali mostravano una miscela più uniforme, inclusa la famiglia let-7, di azione ampia. Poiché ogni microRNA può influenzare molti geni bersaglio, e molti microRNA possono convergere sulle stesse vie, il gruppo ha sviluppato metodi computazionali per comprendere come interi profili — non singole molecole — possano rimodellare programmi cellulari.
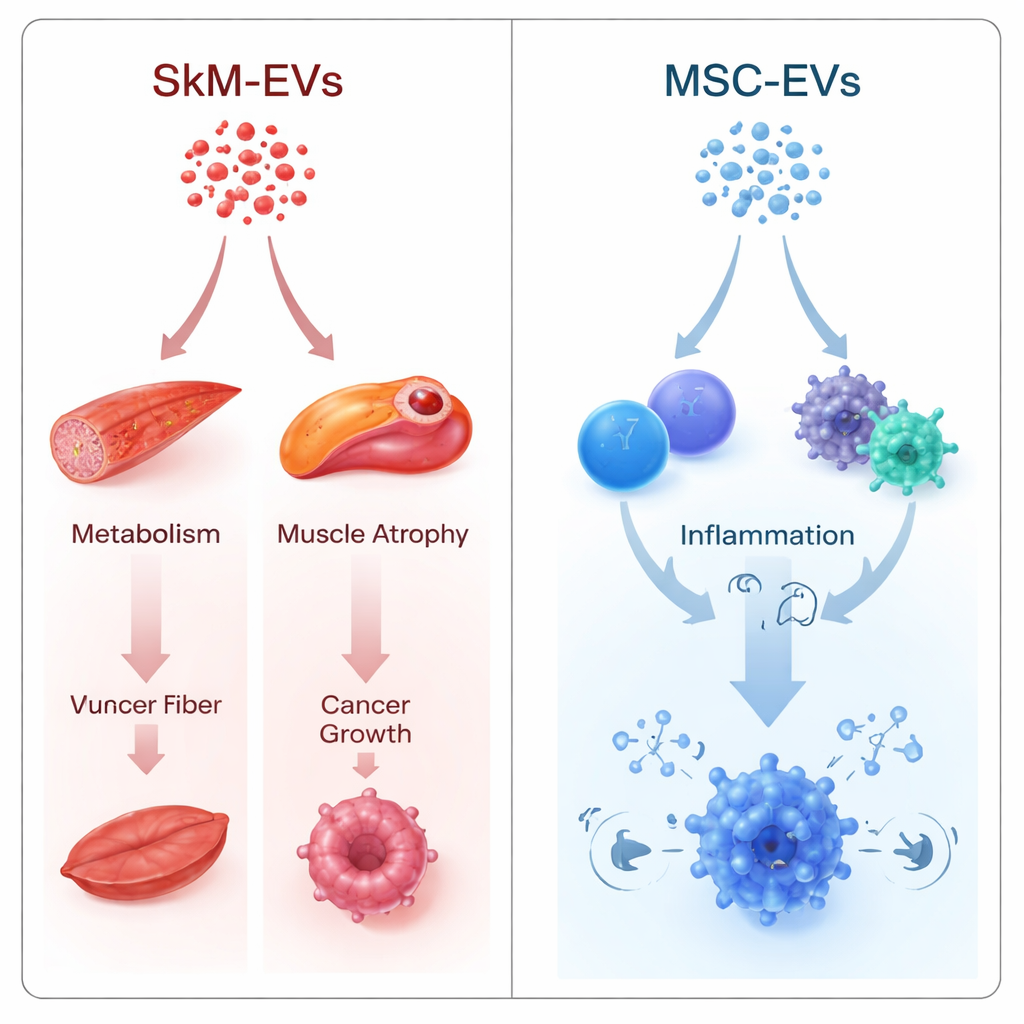
Vie legate al muscolo, al metabolismo e al cancro
Gli autori hanno usato due strategie complementari. Una ha confrontato direttamente EV muscolari e di cellule staminali, chiedendo dove i loro microRNA differissero. L’altra ha trattato ogni tipo di EV separatamente, convertendo il suo profilo di microRNA in un “punteggio di impatto” a livello genico che stima quanto il carico potrebbe attenuare determinate vie. Nonostante la differenza matematica, entrambe le strategie hanno indicato la stessa direzione. Le EV derivate dal muscolo mostravano una tendenza predetta a sopprimere vie legate alla perdita muscolare (segnalazione FoxO e TGF-β), al controllo della glicemia e all’equilibrio energetico (FoxO, mTOR, AMPK), e a vie implicate nella crescita tumorale (segnalazione ErbB e un gruppo etichettato “microRNA nel cancro”). Molti dei bersagli più influenti erano regolatori centrali della gluconeogenesi epatica, driver chiave dell’atrofia muscolare e geni centrali che promuovono il cancro.
Vescicole di cellule staminali e il sistema immunitario
Le EV delle cellule staminali raccontano una storia diversa. Il loro carico di microRNA era previsto agire in modo più marcato su percorsi legati al sistema immunitario: segnalazione NF-κB, interazioni citochina-recettore, segnalazione dei recettori B e T e differenziamento delle cellule Th17. Queste vie sono centrali per come l’organismo rileva le infezioni, accende o spegne l’infiammazione e determina l’identità delle cellule immunitarie. Questo orientamento è in linea con evidenze sperimentali crescenti che le EV delle cellule staminali possono modulare ampiamente le risposte immunitarie e vengono testate in condizioni in cui il contenimento dell’infiammazione è cruciale, come nelle malattie autoimmuni e infiammatorie.
Dalle previsioni computazionali alle terapie future
Nel complesso, il lavoro suggerisce che le EV derivate dal muscolo potrebbero essere naturalmente adatte a condizioni che coinvolgono la perdita muscolare, il metabolismo alterato o la crescita cellulare incontrollata, mentre le EV delle cellule staminali potrebbero essere più indicate per malattie guidate da disfunzioni immunitarie. I risultati sono ricavati interamente da analisi computazionali di dati esistenti e non provano ancora un beneficio nei pazienti, né tengono conto di altri carichi delle EV come proteine o lipidi. Tuttavia, convertendo complessi profili di microRNA in “impronte” a livello di vie, questo studio offre una roadmap per abbinare le fonti di EV ai tipi di malattia e aiuta a dare priorità alle combinazioni più promettenti da testare in laboratorio e, in futuro, in ambito clinico.
Citazione: Kawamoto, Y., Yamaguchi, A., Ma, X. et al. Functional properties of skeletal myotube-derived extracellular vesicles based on microRNA profiles: a comparative analysis with mesenchymal stem cell-derived extracellular vesicles. Sci Rep 16, 7436 (2026). https://doi.org/10.1038/s41598-026-38076-8
Parole chiave: vescicole extracellulari, muscolo scheletrico, microRNA, cellule staminali mesenchimali, vie di segnalazione cellulare