Clear Sky Science · it
Analisi radiografica assistita da AI per rilevare la gravità e i pattern della perdita di osso alveolare
Perché questo è importante per la tua prossima visita dal dentista
La malattia gengivale non si limita a far sanguinare le gengive: erode silenziosamente l’osso che sostiene i denti. I dentisti cercano di individuare questo danno nelle radiografie dentali, ma interpretare queste immagini è difficile e richiede tempo, e piccole alterazioni possono sfuggire facilmente. Questo studio mostra come l’intelligenza artificiale (IA) possa aiutare i dentisti a misurare la perdita ossea attorno a ogni dente in modo più rapido e coerente, aprendo la strada a trattamenti più precoci e a maggiori possibilità di salvare i denti.
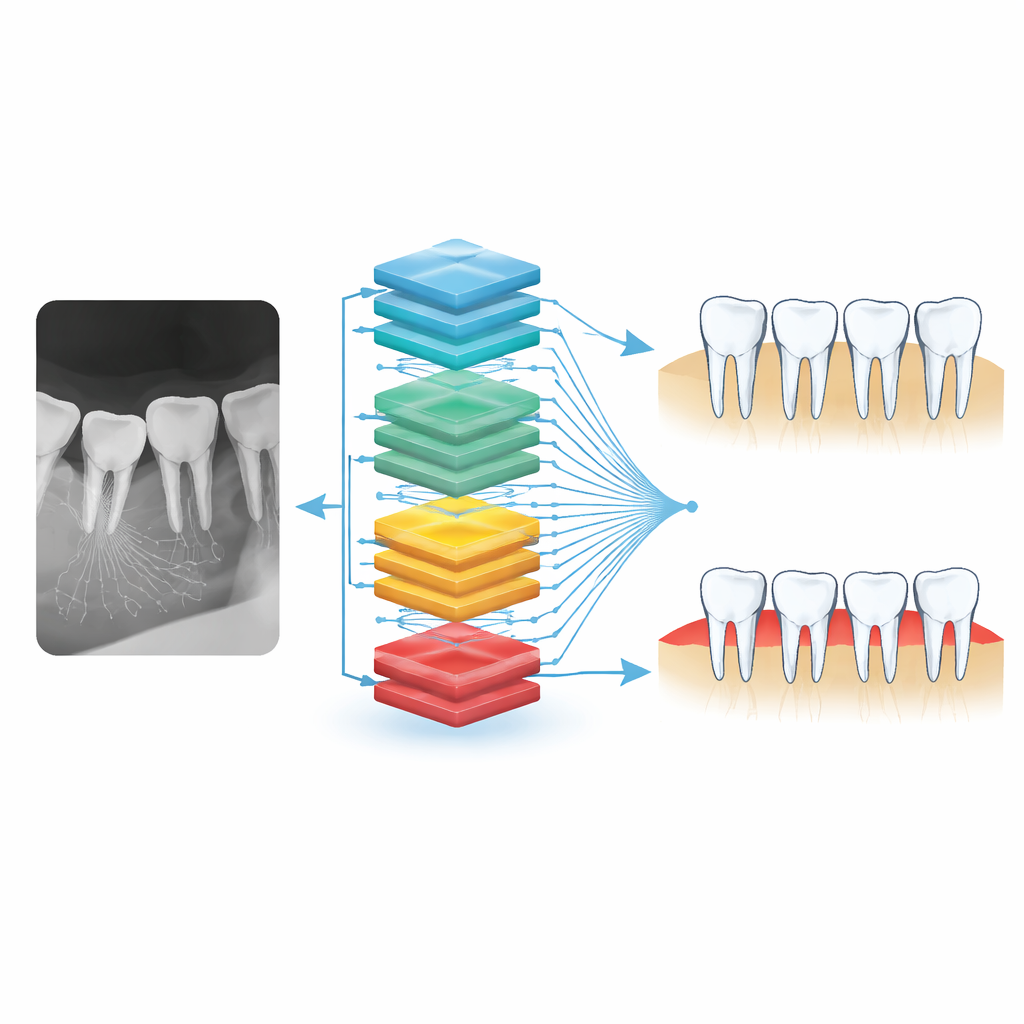
L’osso nascosto che mantiene i denti al loro posto
Ogni dente è ancorato da un sistema di supporto che comprende tessuto gengivale, piccole fibre legamentose e l’osso mandibolare o mascellare. Quando infezioni gengivali prolungate non vengono trattate, questo supporto si deteriora lentamente, portando alla «perdita di osso alveolare», la riduzione dell’osso che avvolge le radici dei denti. A livello mondiale, le forme severe di questo danno colpiscono circa una persona su cinque oltre i 15 anni e sono una delle principali cause di perdita dentale. Nelle radiografie, i dentisti valutano la gravità di questa perdita misurando la distanza tra un punto di riferimento naturale sulla superficie del dente e il margine superiore dell’osso circostante; osservano anche la forma di quel margine osseo—se si è abbassato in modo uniforme (perdita orizzontale) o presenta un calo a cuneo più acuto (perdita angolare). Sia l’estensione sia il tipo di perdita ossea sono importanti per scegliere il trattamento adeguato, compresa la valutazione dell’efficacia possibile delle procedure di rigenerazione ossea.
Perché valutare le radiografie a occhio non basta
Nonostante la sua importanza, la valutazione della perdita ossea sulle radiografie è ancora in gran parte manuale e dipende molto dall’esperienza e dallo stato di affaticamento del dentista. Due clinici possono dare letture diverse sulla stessa immagine, e ambulatori affollati potrebbero avere difficoltà a esaminare ogni superficie dentale in dettaglio. I tentativi precedenti di applicare l’IA in questo campo spesso potevano indicare la presenza di perdita ossea o la sua gravità approssimativa, ma raramente fornivano misurazioni precise dente per dente e di solito non coglievano contemporaneamente sia la gravità sia il pattern della perdita. Gli autori di questo lavoro si sono proposti di costruire un unico sistema automatizzato in grado di svolgere entrambi i compiti—misurare quanto osso manca e classificare se la perdita è orizzontale o angolare—utilizzando il tipo di radiografie periapicali ravvicinate che i dentisti già acquisiscono nella pratica quotidiana.
Come l’IA interpreta le radiografie dentali
Il gruppo ha utilizzato una raccolta pubblica di 1.000 radiografie periapicali intraorali accuratamente annotate, ciascuna con diverse dentature in primo piano. Prima, un modello di IA è stato addestrato a individuare e disegnare riquadri attorno a ogni dente nell’immagine. All’interno di ciascun dente, una seconda famiglia di modelli ha individuato tre punti chiave: il confine smalto-cemento vicino alla linea gengivale, l’apice della radice e il punto in cui il margine osseo visibile attraversa la superficie del dente. Proiettando questi punti su una linea retta e confrontandone le distanze, il sistema ha trasformato gli spazi in pixel in una percentuale di perdita ossea per ogni dente. Un modello separato ha tracciato i contorni sia dei denti sia dei margini ossei, poi ha convertito quelle forme in linee sottili. In ogni sito in cui veniva rilevata una perdita ossea, il software ha confrontato l’inclinazione della superficie del dente con l’inclinazione della linea ossea; angoli più piccoli indicavano difetti angolari, mentre linee più inclinate e parallele segnalavano perdita orizzontale. Questa catena di passaggi ha permesso all’IA di passare dalle radiografie grezze a misurazioni dettagliate e a etichette di pattern in modo automatico.
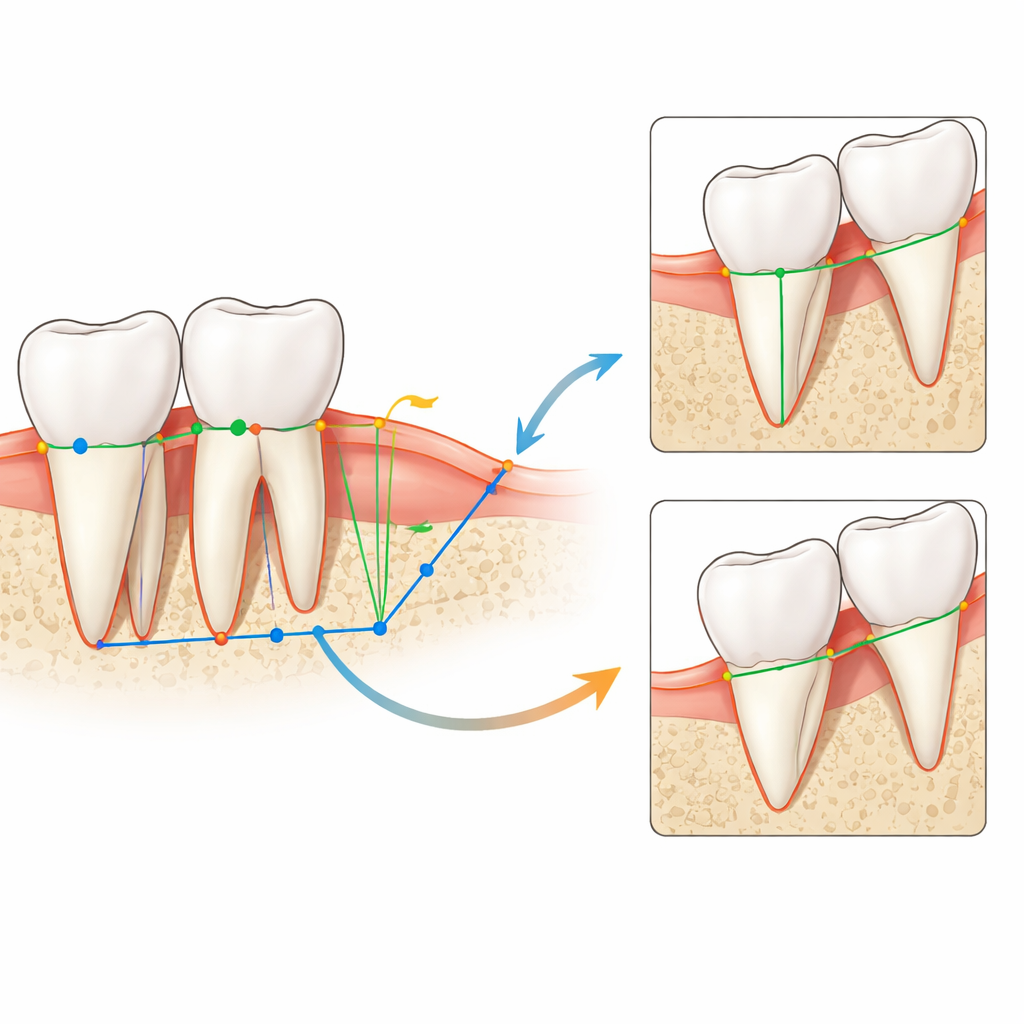
Quanto bene ha funzionato il sistema
Per verificare l’affidabilità delle misurazioni dell’IA, i ricercatori le hanno confrontate con annotazioni di esperti e con le letture manuali di un dentista su un set separato di radiografie. Per la gravità della perdita ossea, l’accordo tra il sistema e gli esperti umani è stato classificato nella fascia «buona» secondo le statistiche standard di attendibilità, e la correlazione con le stime di un clinico esperto è risultata forte. Per i pattern di perdita ossea, l’IA ha distinto correttamente la perdita orizzontale da quella angolare in circa nove casi su dieci e ha mostrato un accordo moderato con le decisioni dell’esperto. Il software è risultato anche più veloce di un lettore umano: poteva analizzare un’intera radiografia in circa 25 secondi, rispetto a 1–4 minuti per uno specialista, esaminando allo stesso tempo ogni superficie dentale in modo uniforme.
Cosa significa per pazienti e dentisti
Lo studio suggerisce che l’IA può diventare una seconda coppia di occhi utile nello studio dentistico, offrendo misurazioni oggettive e ripetibili di quanto osso è stato perso e quale tipo di danno è presente. I dentisti continueranno a prendere la decisione finale, ma potrebbero essere avvisati prima di cambiamenti sottili, pianificare i trattamenti con maggiore sicurezza e monitorare se la terapia sta rallentando o arrestando la perdita ossea nel tempo. Sebbene il sistema necessiti ancora di test sul campo nella pratica clinica quotidiana, indica un futuro in cui le radiografie dentali di routine fungono anche da strumenti precisi, assistiti dal computer, per preservare l’osso che mantiene i nostri denti al loro posto.
Citazione: Wimalasiri, C., Rathnayake, P., Wijerathne, S. et al. AI-assisted radiographic analysis in detecting alveolar bone-loss severity and patterns. Sci Rep 16, 7974 (2026). https://doi.org/10.1038/s41598-026-38061-1
Parole chiave: parodontite, radiografie dentali, intelligenza artificiale, perdita ossea, deep learning