Clear Sky Science · it
Progettazione di criogel funzionalizzati con polietilenimina e metallo per un legame della catalasi, attività e durata a lungo termine superiori
Perché è importante mantenere gli enzimi al loro posto
Il perossido di idrogeno è un sottoprodotto chimico comune in ambiti che vanno dalla trasformazione degli alimenti ai trattamenti medici, e le cellule viventi si affidano all’enzima catalasi per scomporlo in acqua e ossigeno innocui. Nell’industria, tuttavia, la catalasi viene solitamente impiegata in forma libera e dissolta, che perde rapidamente efficacia, non è facilmente recuperabile e deve essere sostituita spesso. Questo studio esplora un modo per “parcheggiare” la catalasi all’interno di un materiale simile a una spugna in modo che resti attiva più a lungo, possa essere riutilizzata molte volte e lavori in modo più efficiente—tutti fattori che potrebbero ridurre i costi e rendere i processi enzimatici più puliti e sostenibili.

Costruire una spugna intelligente
I ricercatori hanno progettato una speciale spugna polimerica, chiamata criogel, ottenuta congelando e scongelando una miscela liquida in modo che i cristalli di ghiaccio scavino pori grandi e interconnessi. Questi pori consentono ai liquidi di fluire liberamente, come l’acqua attraverso un luffa, mentre la struttura solida rimane resistente ed elastica. Il team ha utilizzato un materiale di base chiamato Poly(HEMA-co-GMA), quindi ha innestato chimicamente su di esso una molecola ramificata ricca di gruppi azotati, la polietilenimina (PEI). Infine, ha legato ioni metallici—rame, nichel o cobalto—a questi siti azotati. L’idea era che gli ioni metallici fungessero da punti di ancoraggio che attraggono e trattengono fortemente le molecole di catalasi senza ostacolare il flusso del liquido attraverso la spugna.
Regolare il materiale per le migliori prestazioni
Per capire come ogni fase di questo progetto modificasse il materiale, il team ha utilizzato diverse tecniche di laboratorio per sondarne la struttura, la chimica e la stabilità. Hanno dimostrato che l’aggiunta di PEI e poi dei metalli non ha fatto collassare la rete porosa, ma ha effettivamente aumentato la capacità della spugna di trattenere acqua, cosa utile per mantenere gli enzimi in condizioni favorevoli e attivi. Tra i tre metalli, il rame ha prodotto l’ambiente più idratato e ben organizzato. Le immagini microscopiche hanno rivelato che il materiale originale appariva come granuli compatti, mentre le versioni trattate con PEI e metalli si aprivano in una rete più pulita e continua di pori ampi. Le misure del contenuto metallico hanno confermato che il rame si legava in modo più forte e in quantità maggiori rispetto a nichel o cobalto, suggerendo che avrebbe fornito i punti di ancoraggio più efficaci per la catalasi.
Fissare la catalasi al suo posto
Quando la catalasi è stata introdotta nelle diverse spugne contenenti metalli, tutte e tre hanno catturato l’enzima rapidamente, ma la versione al rame si è distinta. Ha caricato la quantità più alta di catalasi—circa 392 milligrammi per grammo di spugna secca—raggiungendo un livello stabile in circa otto ore. I ricercatori hanno quindi esaminato quanto bene l’enzima immobilizzato funzionasse rispetto alla catalasi libera in soluzione. Sebbene la velocità massima di reazione per grammo di enzima sia diminuita leggermente, la catalasi immobilizzata ha mostrato un’attrazione apparente molto più forte per il suo substrato, il perossido di idrogeno. In termini pratici, ciò significa che l’enzima legato svolgeva il suo compito in modo più efficiente a concentrazioni di substrato inferiori, probabilmente perché la spugna di rame porosa e ricca d’acqua concentrava il substrato vicino all’enzima e contribuiva a mantenere la sua conformazione attiva.
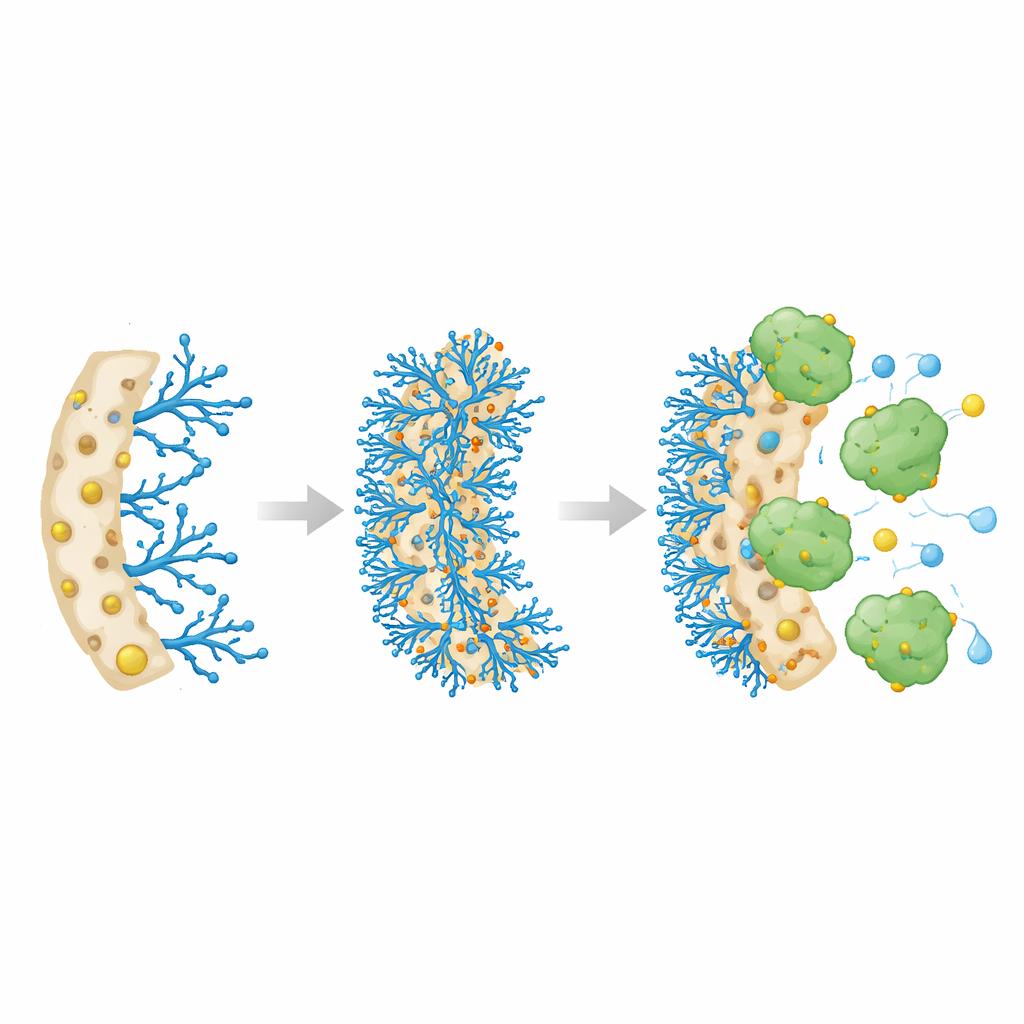
Un enzima che dura
Uno dei vantaggi principali dell’immobilizzazione degli enzimi è la promessa di riutilizzo e di lunga conservazione. In questo caso, la catalasi legata al criogel a base di rame si è dimostrata molto più durevole della sua controparte libera. Dopo 15 cicli di utilizzo ripetuti, l’enzima immobilizzato ha conservato ancora circa un terzo della sua attività iniziale, mentre la catalasi libera verrebbe tipicamente scartata dopo un singolo utilizzo. Nei test di conservazione a temperatura frigorifero per oltre 70 giorni, la catalasi immobilizzata ha mantenuto più del 60% della sua attività, circa il doppio rispetto all’enzima libero. La spugna ha inoltre permesso di staccare e ricaricare l’enzima più volte utilizzando una semplice soluzione salina, mostrando che il materiale stesso può essere riutilizzato senza una significativa perdita di capacità.
Cosa significa per l’uso nel mondo reale
Per un non specialista, il messaggio principale è che i ricercatori hanno realizzato una specie di “spugna per enzimi” riutilizzabile che trattiene la catalasi in modo saldo ma delicato, aiutandola a funzionare meglio a livelli chimici inferiori e a durare molto più a lungo in uso e in conservazione. Accoppiando un criogel altamente poroso con PEI e ioni rame, hanno creato una piattaforma che combina elevato carico enzimatico, maggiore efficienza e forte stabilità a lungo termine. Materiali di questo tipo potrebbero essere integrati in sistemi industriali o ambientali per degradare il perossido di idrogeno e sostanze correlate in modo più affidabile e con meno spreco, offrendo un passo pratico verso tecnologie enzimatiche più verdi.
Citazione: Erol, K., Alkan, M.H. & Alacabey, İ. Engineering polyethylenimine–metal functionalized cryogels for superior catalase binding, activity, and long-term durability. Sci Rep 16, 7880 (2026). https://doi.org/10.1038/s41598-026-38040-6
Parole chiave: immobilizzazione degli enzimi, catalasi, criogel, polimeri funzionalizzati al rame, biocatalisi