Clear Sky Science · it
Somministrazione cronica di NH4Cl migliora la tolleranza al glucosio senza modificare la sensibilità all’insulina nei topi
Perché l’equilibrio acido–base conta per la glicemia
Le persone con malattia renale cronica spesso sviluppano una condizione chiamata acidosi metabolica, in cui il sangue diventa leggermente più acido del normale. I medici tendono a considerarla dannosa, anche perché episodi brevi di acidosi sono noti per peggiorare il controllo della glicemia. Questo studio rovescia quell’idea: nei topi, un’acidosi lieve e prolungata ha in realtà migliorato la gestione del glucosio, senza alterare l’efficacia dell’ormone insulina. Comprendere questo risultato sorprendente potrebbe aiutare in futuro a perfezionare i trattamenti per la malattia renale e il diabete di tipo 2.
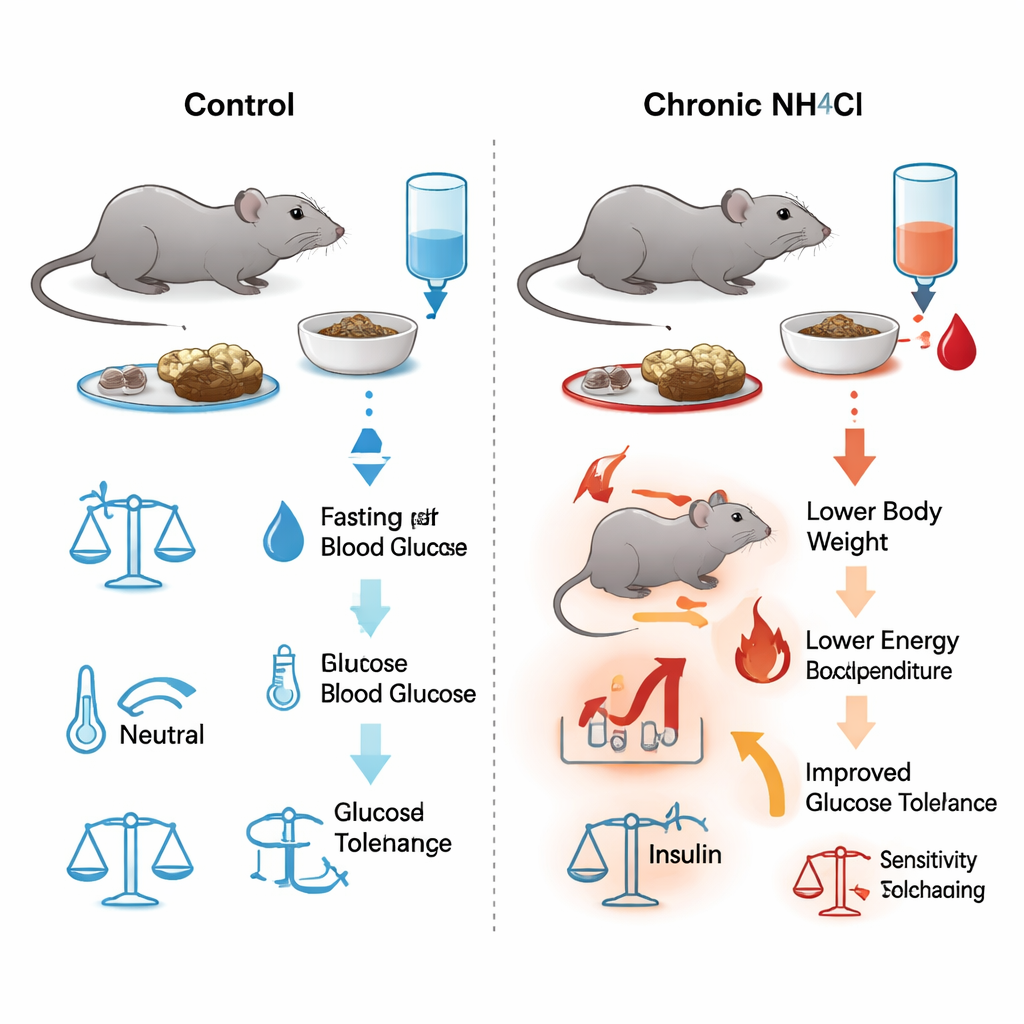
Una sfida acida a lungo termine nei topi
I ricercatori hanno somministrato a topi maschi acqua da bere contenente cloruro di ammonio, un sale che acidifica dolcemente il sangue, per un periodo fino a sei mesi. Questo trattamento riproduce il carico acido cronico osservato nella malattia renale. Gli esami del sangue hanno confermato un’acidosi metabolica persistente e lieve: pH e bicarbonato più bassi, cloro più alto e misure renali correlate (come urea e ematocrito) sostanzialmente stabili. Nonostante mangiassero e bevessero quanto — o più — dei topi non trattati, gli animali esposti all’acido hanno smesso di aumentare di peso dopo circa due mesi. Misurazioni dettagliate in gabbie metaboliche hanno mostrato che questi topi bruciavano più energia in generale, avevano meno massa magra (ricca di muscolo) e una quota relativa di grasso maggiore, suggerendo un costo metabolico più elevato per vivere sotto acidosi cronica.
Migliore controllo glicemico senza un aiuto extra dall’insulina
Il gruppo ha valutato ripetutamente quanto bene i topi eliminassero il glucosio dal sangue mediante iniezioni di glucosio e monitoraggio dei livelli ematici nel tempo. Già dopo una settimana dall’inizio della bevanda acidificante, i topi trattati abbassavano più rapidamente la glicemia rispetto ai controlli, e questo vantaggio è persistito in molti punti temporali fino a 180 giorni. La glicemia a digiuno è risultata costantemente più bassa nel gruppo acidosico. Tuttavia, quando gli scienziati hanno misurato l’insulina nel sangue durante questi test, i livelli erano gli stessi in entrambi i gruppi. Test separati in cui ai topi è stata somministrata insulina direttamente hanno mostrato che la sensibilità complessiva all’insulina era anch’essa invariata. In altre parole, l’acidosi cronica ha migliorato la tolleranza al glucosio senza spingere il pancreas a produrre più insulina né richiedere una risposta tissutale più forte.
Spostamenti su dove e come viene prodotto e perso il glucosio
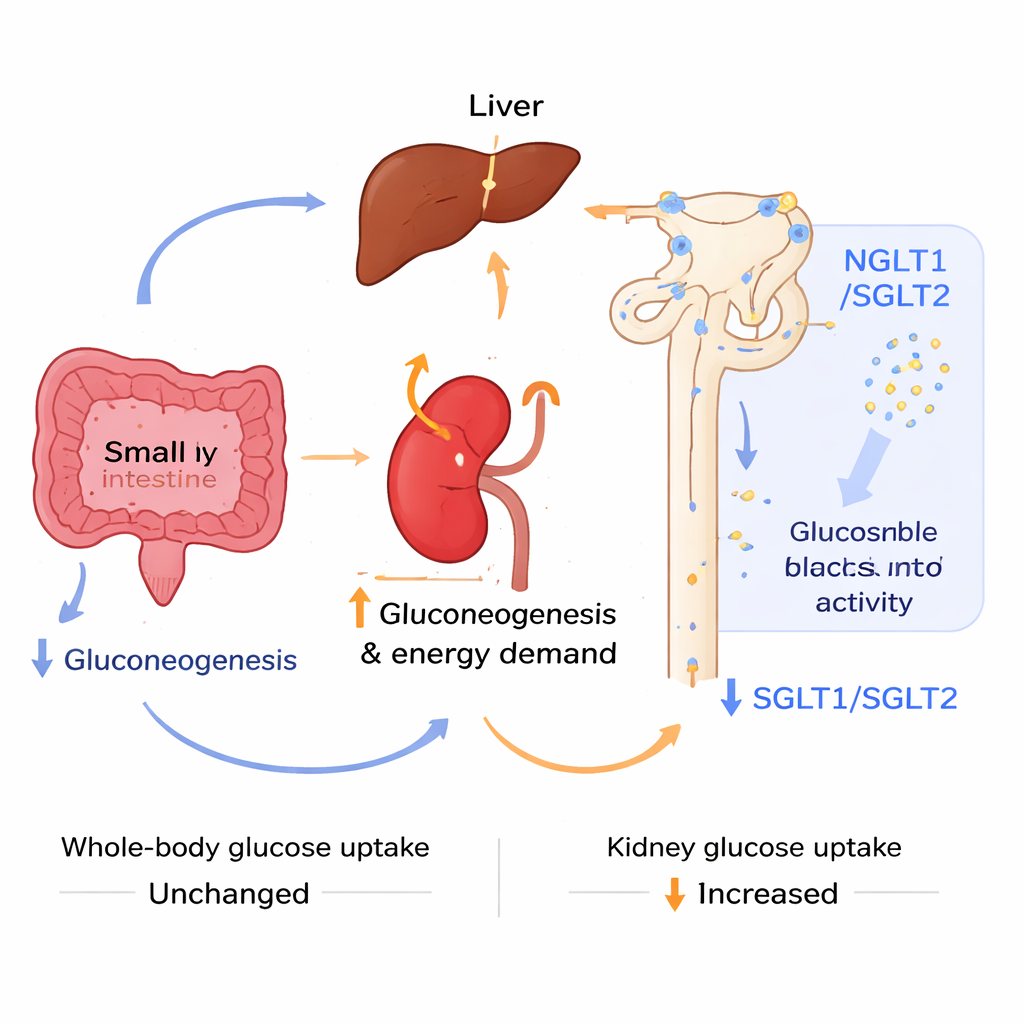
Per capire da dove provenisse il miglior controllo glicemico, i ricercatori hanno indagato come diversi organi producevano glucosio. Hanno usato sostanze specifiche — piruvato, alanina e glutamina — che alimentano le vie di produzione del glucosio nel fegato, nel rene e nell’intestino. Nel tempo, il fegato e parti dell’intestino dei topi acidosici sono diventati meno attivi nella neoformazione di glucosio, in particolare da alanina e glutamina. Al contrario, il rene ha mostrato segnali di maggiore attività: geni chiave coinvolti nella produzione di glucosio e nell’approvvigionamento energetico sono risultati upregolati e immagini con un analogo del glucosio radioattivo hanno rivelato una maggiore captazione di zucchero nei reni e nella vescica, anche se la captazione totale corporea non è cambiata. Allo stesso tempo, più glucosio è stato perso nelle urine dopo un carico di zucchero, perché i principali trasportatori sodio–glucosio renali, che normalmente riassorbono lo zucchero filtrato, risultavano ridotti sia a livello di RNA sia di proteina. Questa combinazione — meno glucosio prodotto da fegato e intestino, più glucosio consumato e perso dal rene — ha contribuito a mantenere sotto controllo i valori ematici.
Profondi cambiamenti all’interno delle cellule renali
I profili di attività genica dei reni durante i primi due mesi di trattamento hanno mostrato un ampio rimodellamento dei meccanismi cellulari. Sono state potenziate le vie coinvolte nel trasporto di particelle cariche (anioni), nel riassorbimento del bicarbonato e nel funzionamento dei mitocondri e della fosforilazione ossidativa — i principali generatori di energia della cellula. Anche i geni legati al metabolismo del glucosio e dei grassi si sono spostati verso l’alto, mentre alcune vie immunitarie e di detossificazione, comprese parti del sistema del complemento e della famiglia dei citocromi P450, sono risultate attenuate. Questi modelli sono coerenti con un rene che lavora di più per escretare l’acido, consumando più combustibile e al contempo riprogrammando il modo in cui gestisce zuccheri e lipidi per soddisfare la maggiore richiesta energetica.
Che cosa significa per le persone con problemi renali e metabolici
In sintesi, un’acidosi metabolica lieve e prolungata nei topi non ha danneggiato il controllo della glicemia — anzi, lo ha migliorato — riducendo la produzione di glucosio nel fegato e nell’intestino, abbassando il riassorbimento renale di glucosio e aumentando l’uso energetico del rene. L’insulina di per sé non ha avuto un ruolo maggiore del normale. Questo non significa che l’acidosi sia un bene o che i pazienti debbano rimanere in uno stato acidosico; l’acidosi ha comunque molti effetti nocivi. Ma i risultati rivelano che il corpo può adattarsi in modi inaspettati e sottolineano il rene come regolatore potente della glicemia. Studi futuri potrebbero riuscire a sfruttare alcuni di questi meccanismi renali — come l’aumento della perdita urinaria di glucosio e la modifica della produzione di glucosio — senza esporre i pazienti ai rischi dell’acidosi cronica.
Citazione: Zaibi, N., Montaigne, J., Baraka-Vidot, J. et al. Chronic NH4Cl loading improves glucose tolerance without modifying insulin sensitivity in mice. Sci Rep 16, 7048 (2026). https://doi.org/10.1038/s41598-026-38007-7
Parole chiave: acidosi metabolica, tolleranza al glucosio, funzione renale, gluconeogenesi, rischio di diabete di tipo 2