Clear Sky Science · it
La modellizzazione dell'intera cellula predice strategie alternative di allocazione del proteoma nell'archeone Methanococcus maripaludis
Perché contano i minuscoli produttori di metano
Methanococcus maripaludis è un archeone microscopico che trasforma semplici molecole come anidride carbonica e formiato in metano, un componente principale del gas naturale. Comprendere come questo microbo ripartisce le sue risorse interne — in particolare le proteine — può rivelare regole generali della vita in condizioni di limitata disponibilità energetica e guidare gli sforzi per sfruttarlo come fabbrica biologica di metano o come piattaforma per la chimica verde.
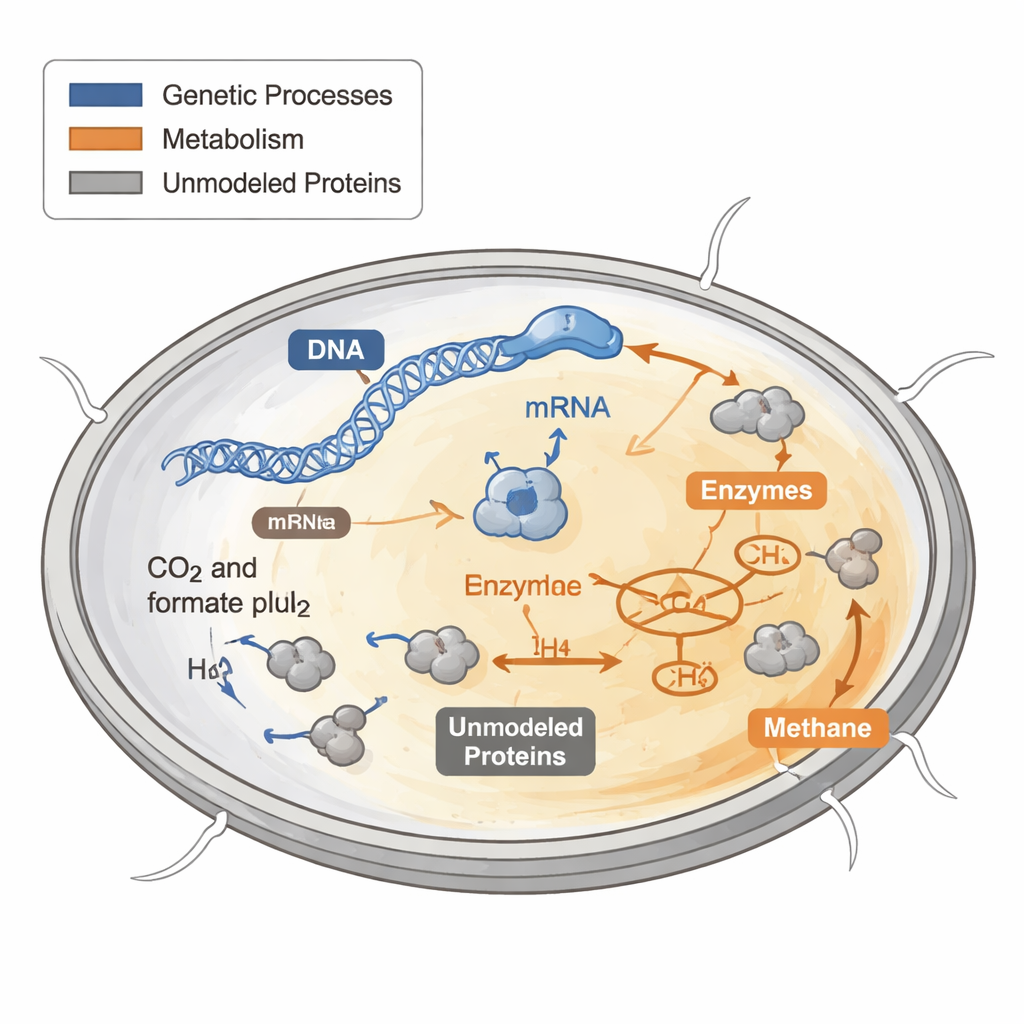
Come le cellule spendono il loro budget proteico
Ogni cellula deve decidere come spendere il suo limitato “budget” di proteine. Alcune proteine costruiscono nuove parti cellulari, altre raccolgono energia e altre ancora svolgono funzioni di manutenzione. I precedenti modelli computazionali del metabolismo trattavano queste proteine come se fossero libere e illimitate, un'approssimazione che funziona male quando si cerca di prevedere la crescita in condizioni difficili o povere di nutrienti. In batteri e lieviti, esperimenti hanno mostrato che le cellule che crescono rapidamente dedicano una fetta maggiore del loro budget proteico ai ribosomi, le macchine molecolari che sintetizzano nuove proteine, mentre le cellule a crescita lenta spostano le risorse altrove.
Un archeone che infrange le regole
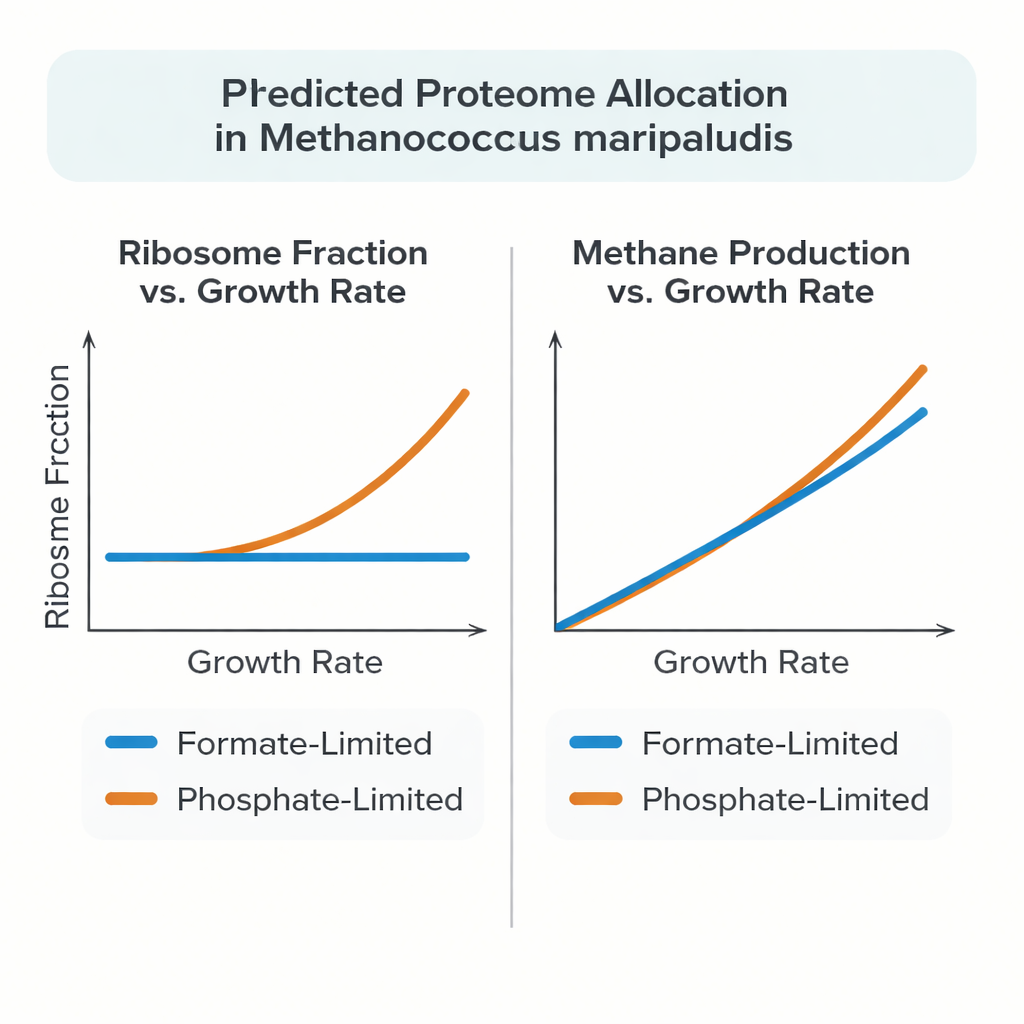
Esperimenti recenti hanno rivelato che M. maripaludis non sempre segue questo schema. Quando cresce usando il formiato sia come cibo sia come fonte di energia, la frazione del budget proteico investita nei ribosomi rimane quasi costante al rallentare della crescita. In condizioni di limitazione del fosfato, invece, l'archeone appare più convenzionale: la quota dedicata ai ribosomi aumenta con il tasso di crescita, in modo simile a Escherichia coli e ai lieviti. Per spiegare questo comportamento insolito, gli autori hanno costruito un modello dettagliato in stile whole-cell che collega il metabolismo al processo costoso di sintesi e assemblaggio di proteine e RNA, invece di trattare le proteine come semplici tassi di reazione astratti.
Costruire un modello in stile whole-cell
I ricercatori sono partiti da una mappa metabolica esistente di M. maripaludis e vi hanno sovrapposto migliaia di reazioni aggiuntive che descrivono l'espressione genica: la copia del DNA in RNA, l'amminoacilazione degli RNA di trasporto, l'assemblaggio di ribosomi e complessi enzimatici e la diluizione di questi componenti durante la divisione cellulare. Hanno raccolto i limiti di velocità degli enzimi da database biochimici e dalla letteratura e stimato quanto della massa proteica sia costituita da proteine “non modellate” che non sono direttamente legate alle reazioni nella mappa. Hanno quindi imposto vincoli globali che limitano la massa totale di proteine e RNA, collegano i tassi di reazione alla quantità di enzima disponibile e vincolano la produzione proteica alla capacità ribosomiale. Con questi vincoli, il modello deve scegliere come allocare un budget proteico fisso per sostenere la crescita.
Cosa hanno rivelato le simulazioni
Quando testato su esperimenti in chemostato di alta qualità, il modello ha riprodotto accuratamente le masse misurate di proteine e RNA, i tassi di produzione di metano e le rese di crescita su un intervallo di bassi tassi di crescita. In condizioni di limitazione del formiato, la cellula simulata si è naturalmente attestata su una frazione proteica ribosomiale quasi costante al variare della crescita, rispecchiando i dati sperimentali. In condizioni di limitazione del fosfato, il modello ha corrisposto all'aumento osservato della frazione ribosomiale solo quando ai ribosomi è stato permesso di lavorare più velocemente a bassi tassi di crescita, coerente con misure che mostrano un maggior numero di ribosomi attivamente impegnati nella sintesi proteica. Il modello ha anche suggerito che una quota consistente delle proteine in M. maripaludis non è strettamente necessaria per la crescita minima, e che carbonio ed energia in eccesso possono essere immagazzinati o deviate verso altre grandi molecole come glicogeno o amminoacidi liberi, a seconda del nutriente limitante.
Esplorare mutanti e limiti di crescita
Poiché il modello tiene esplicitamente conto del costo proteico di ciascun percorso, può prevedere non solo se mutanti genetici crescono, ma quanto bene crescono rispetto al tipo selvatico. Gli autori hanno simulato ceppi privi di diversi enzimi coinvolti nel processamento dell'idrogeno e hanno confrontato la fitness prevista con le misure di laboratorio in diverse condizioni di crescita, inclusa la presenza o assenza di idrogeno e monossido di carbonio. In molti casi il modello ha catturato se i mutanti potevano crescere e ha prodotto stime ragionevoli dei loro tassi di crescita relativi, migliorando i modelli precedenti che potevano dare solo risposte sì-o-no. Lo stesso framework è stato usato per stimare i tassi massimi di crescita possibili in condizioni di batch per diverse combinazioni di substrati.
Cosa significa per la scienza e la tecnologia
In termini pratici, questo studio mostra che M. maripaludis adotta una strategia alternativa per gestire la sua forza lavoro proteica, mantenendo le sue “fabbriche” proteiche a una quota stabile del budget in alcune condizioni invece di ridurle mentre la crescita rallenta. Integrando questo comportamento in un modello dettagliato e guidato dai dati, il lavoro fornisce un banco di prova per esplorare come i microrganismi soggetti a limitazioni energetiche bilanciano crescita, manutenzione e accumulo. Per la ricerca applicata, il modello offre una guida per ingegnerizzare questo archeone affinché produca più metano o altri prodotti identificando quali enzimi e percorsi sono più costosi in termini di investimento proteico. Più in generale, estende la potente modellizzazione in stile whole-cell oltre batteri e lieviti al dominio degli archei, aiutando a colmare il divario tra dettagli molecolari e comportamento su larga scala delle comunità microbiche coinvolte in clima, energia e biotecnologia industriale.
Citazione: Kasem, G.S., Soliman, T.H.A., Mousa, M.A.A. et al. Whole-cell modeling predicts alternative proteome allocation strategies in the archaeon Methanococcus maripaludis. Sci Rep 16, 7386 (2026). https://doi.org/10.1038/s41598-026-37887-z
Parole chiave: Methanococcus maripaludis, allocazione del proteoma, modellizzazione dell'intera cellula, metanogenesi, metabolismo degli archei