Clear Sky Science · it
Strategie computazionali per ricavare intuizioni da inibitori noti per l’ottimizzazione del lead: uno studio di caso sugli analoghi del celecoxib
Perché piccole modifiche negli analgesici contano
Gli antidolorifici moderni non si limitano ad attenuare i dolori; modulano la chimica del corpo in modi molto precisi. Il celecoxib, un diffuso farmaco antinfiammatorio, prende di mira un enzima coinvolto nel dolore e nel gonfiore risparmiando in larga misura un enzima affine che protegge lo stomaco. Eppure dozzine di stretti cugini chimici del celecoxib si comportano in modo molto diverso nell’organismo. Questo studio usa la modellistica computazionale per porre una domanda apparentemente semplice ma con grandi implicazioni per farmaci più sicuri: quanto conta una singola piccola modifica in una molecola?
L’enzima che accende il dolore
Quando un tessuto è lesionato o infiammato, il corpo rilascia una molecola grassa chiamata acido arachidonico. Un enzima chiamato COX-2 converte questa molecola in prostaglandine, che scatenano dolore, febbre e gonfiore. Un enzima correlato, COX-1, aiuta a proteggere la mucosa gastrica e le piastrine. I farmaci antinfiammatori più vecchi come l’ibuprofene colpiscono entrambi gli enzimi, alleviando il dolore ma spesso irritando l’intestino. Il celecoxib è stato progettato per infilarsi in una tasca leggermente più ampia presente soprattutto in COX-2, bloccando i segnali del dolore e lasciando intatte gran parte delle funzioni protettive di COX-1. Capire la forma dettagliata di questa tasca e come le molecole del farmaco si sistemano al suo interno è centrale per progettare nuovi medicinali potenti e sicuri.
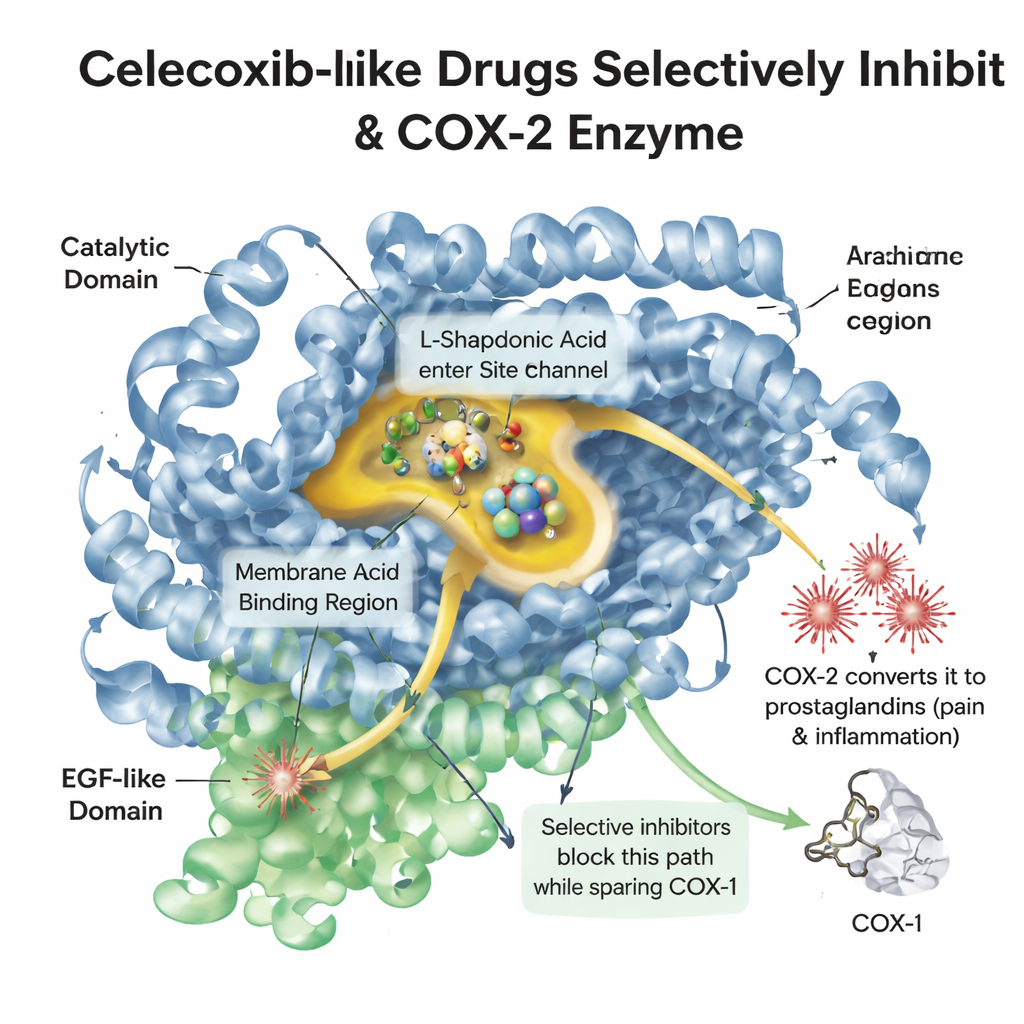
Una libreria digitale di farmaci somiglianti
I ricercatori hanno assemblato un insieme di 375 molecole che condividono tutte lo scheletro di base a tre anelli del celecoxib ma differiscono in piccoli dettagli, come lo scambio di un singolo atomo o di un gruppo laterale. Hanno estratto queste strutture e le loro misurate capacità di bloccare COX-2 da un database pubblico di farmaci. Usando software chimico, hanno generato modelli 3D di ciascuna molecola, calcolato quasi 2.000 descrittori numerici delle loro forme e proprietà, e poi le hanno scagliate (docked) in una struttura ad alta risoluzione dell’enzima COX-2. Nel docking, un computer posiziona una molecola nella tasca dell’enzima in molte configurazioni e valuta quanto ciascuna posa si adatti in modo aderente.
Ciò che controlla veramente potenza e selettività
Il team si è concentrato su tre regioni chiave del celecoxib. "Sito-1" è un anello che si trova in una zona apolare della tasca; "Sito-2" è un anello con una coda ricca di fluoro; e "Sito-3" è un anello che porta un gruppo sulfonamide in grado di formare forti legami a idrogeno. La loro analisi ha mostrato che il Sito-1 preferisce gruppi piccoli e non polari che preservano i contatti idrofobici; rendere quest’area più affine all’acqua, per esempio aggiungendo un gruppo –OH o acido, generalmente indeboliva il farmaco. Al Sito-2, piccoli gruppi elettronegativi come il fluoro spesso aumentavano la potenza migliorando le interazioni in una tasca ristretta, mentre code più ingombranti o più polari tendevano a penalizzare l’attività. Al Sito-3, l’azoto della sulfonamide, capace di donare un legame a idrogeno, era cruciale; sostituirlo con una versione non legante riduceva significativamente l’affinità.
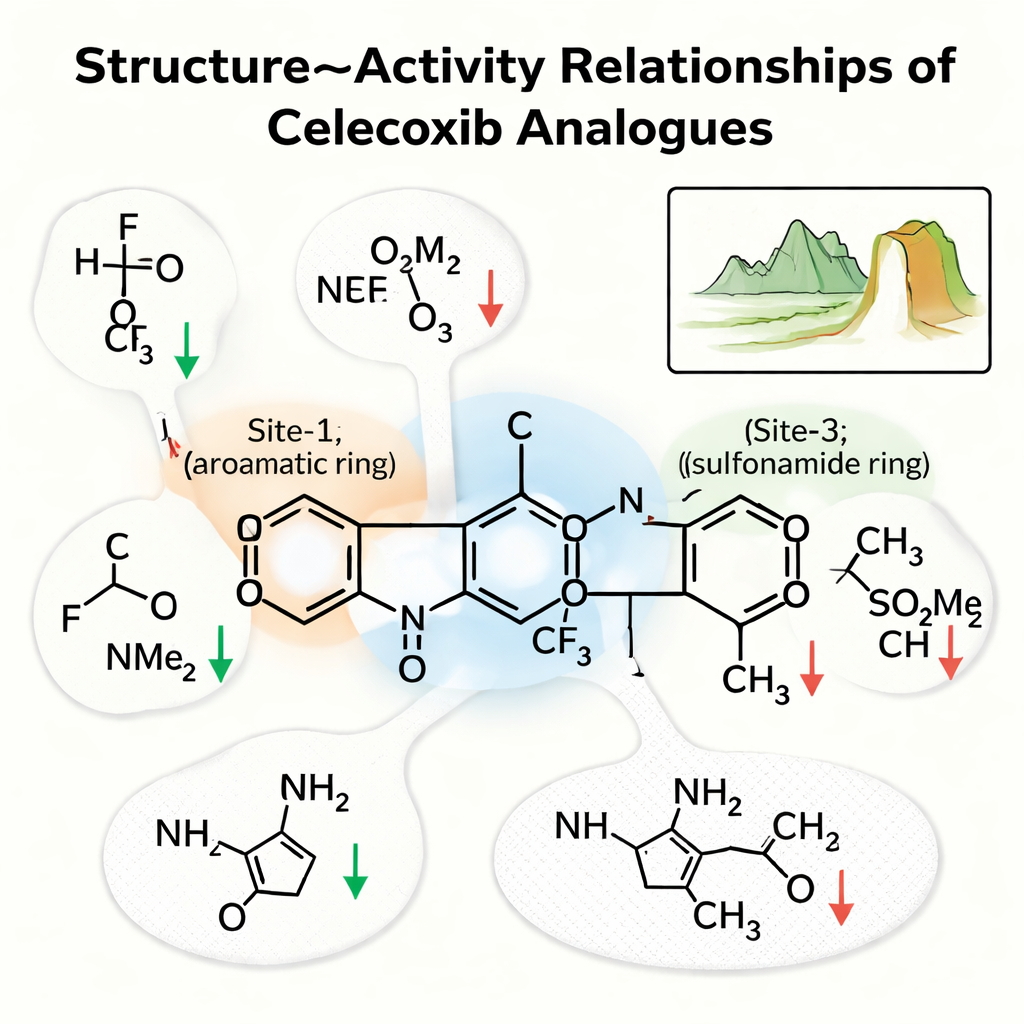
Scogliere nel paesaggio chimico
Per andare oltre le semplici tendenze, gli autori hanno costruito un "landscape struttura–attività", che chiede quanto salti la potenza del farmaco quando la struttura cambia di poco. In questa visione, la maggior parte dei composti simili al celecoxib giace su dolci colline: modificarli — per esempio spostando un alogeno o aggiungendo un piccolo gruppo flessibile — sposta la potenza su o giù in modi prevedibili. Ma alcune coppie formano nette "scogliere di attività", in cui una piccola modifica, come sostituire un gruppo metile con un trifluorometile o aggiungere un singolo atomo di fluoro, provoca un guadagno o una perdita drammatica di attività. Lo studio ha inoltre eseguito simulazioni complete di dinamica molecolare — filmati virtuali dei complessi farmaco‑enzima in movimento — che hanno confermato che i migliori analoghi rimangono stabili nella tasca per centinaia di nanosecondi.
Guidare la prossima generazione di analgesici più sicuri
Per un non specialista, il messaggio principale è che nella progettazione dei farmaci i dettagli minuti hanno un’importanza enorme. Due composti che sembrano quasi identici sulla carta possono differire di mille volte nella forza con cui bloccano COX-2, semplicemente perché un atomo in più migliora l’adattamento in una tasca microscopica o interrompe un contatto chiave. Mappando sistematicamente quali cambiamenti aiutano o danneggiano ciascuno dei tre siti chiave del celecoxib, e mettendo in evidenza le pericolose "scogliere" dove piccole modifiche hanno effetti sproporzionati, questo lavoro computazionale offre una mappa per i chimici. Indica la via verso nuovi farmaci antinfiammatori che mantengono l’efficacia analgesica del celecoxib spingendo ulteriormente verso sicurezza e selettività.
Citazione: Grewal, S., Ghosh, B., Narayan, U. et al. Computational strategies for unraveling insights from known inhibitors for further lead optimization: A case study on Celecoxib analogues. Sci Rep 16, 6720 (2026). https://doi.org/10.1038/s41598-026-37798-z
Parole chiave: inibitori COX-2, analoghi del celecoxib, farmaci antinfiammatori, progettazione di farmaci computazionale, relazioni struttura-attività