Clear Sky Science · it
Una strategia multidimensionale abilita la scalabilità della diversità del metaboloma nelle fermentazioni microbiche
Perché piccoli ritocchi alla “fabbrica” contano per i nuovi farmaci
Molti dei farmaci odierni derivano da composti naturali prodotti da batteri e funghi. Ma trasformare un promettente risultato di laboratorio in un candidato farmacologico spesso fallisce in un passaggio sorprendentemente terreno: coltivare lo stesso microbo in un contenitore diverso o su scala maggiore. Questo studio pone una domanda semplice ma cruciale — come mantenere stabile e diversificata la produzione chimica di un microbo quando lo si trasferisce da piccole piastre di prova a flaconi più grandi e bioreattori? La risposta potrebbe accelerare la ricerca della prossima generazione di antibiotici e altre terapie.
Tre modi per coltivare lo stesso microbo
I ricercatori si sono concentrati su un batterio del suolo, Streptomyces griseochromogenes, noto per produrre molti “metaboliti secondari” — piccole molecole con potenziale farmacologico. Hanno confrontato tre sistemi di coltura comuni usati nella fase iniziale della scoperta: flaconi agitati con baffling, piastre microtiter “a fiore” da 48 pozzetti e un bioreattore a serbatoio agitato. In ciascun sistema hanno misurato la crescita, la forma e la struttura cellulare e, cosa cruciale, il profilo dei segnali chimici rilevati dalla spettrometria di massa, usata qui come impronta del metaboloma secreto dal batterio. Hanno applicato inizialmente una regola ingegneristica classica: mantenere la disponibilità di ossigeno costante tra i sistemi e aspettarsi comportamenti simili. Invece, hanno rilevato che curve di crescita, forme cellulari e impronte chimiche differivano nettamente da un recipiente all’altro.
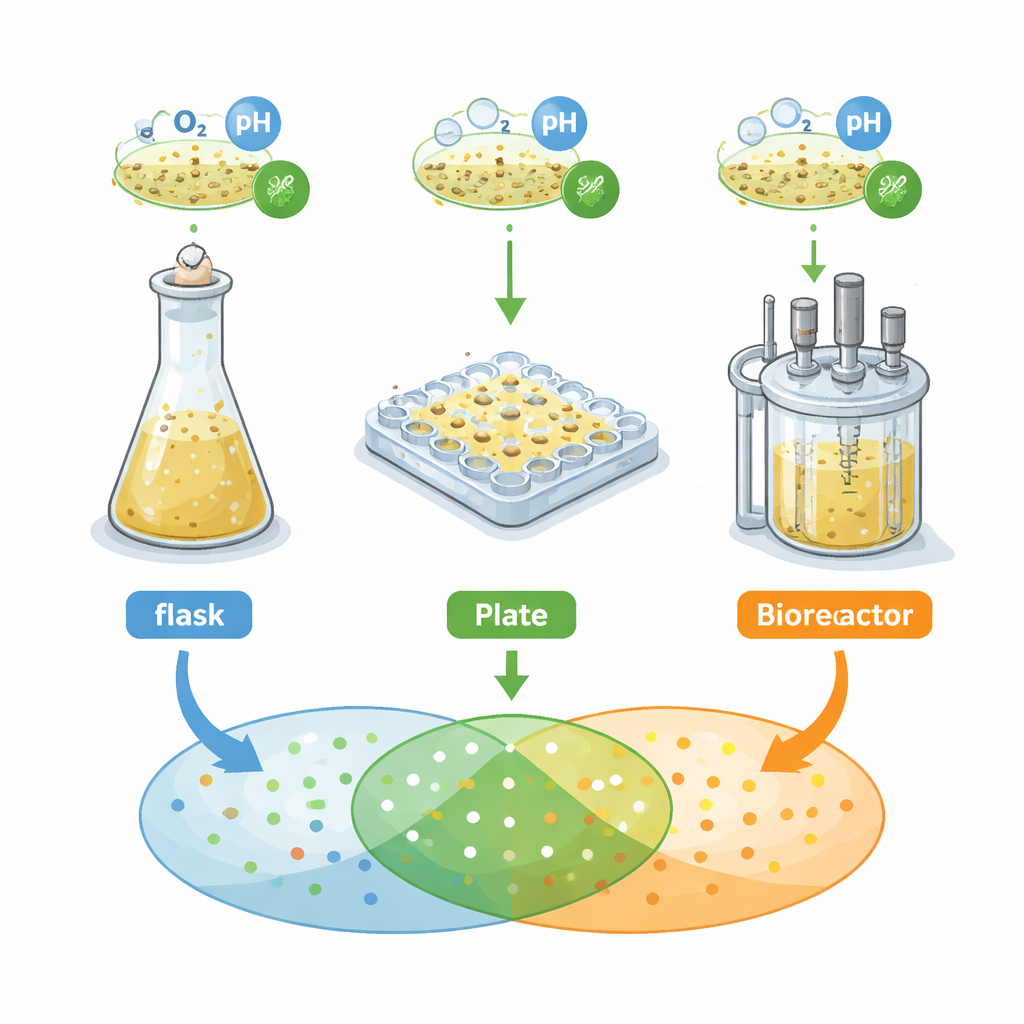
Quando una regola non basta
Far coincidere solo l’ossigeno ha prodotto “impronte metaboliche” molto diverse — gli insiemi di segnali di massa corrispondenti a singole molecole. Solo circa il 18 percento di questi segnali era condiviso tra i tre sistemi. Le piastre microtiter hanno generato molte più firme distintive rispetto a flaconi o al bioreattore. Il gruppo ha quindi provato un altro approccio monodimensionale, variando o la quantità di etanolo nel terreno (una piccola molecola che può indurre i batteri a produrre più metaboliti) o la velocità di agitazione, che altera l’apporto di ossigeno alla coltura. Questi aggiustamenti unidimensionali hanno migliorato modestamente la sovrapposizione delle impronte chimiche, ma solo di circa un ulteriore 18 percento. In altre parole, ricette semplici come “aumentare l’ossigeno” o “aggiungere etanolo” non garantivano che un metabolita osservato in un microscopico pozzetto si presentasse in modo affidabile in un fermentatore più grande.
Come la forma cellulare guida la diversità chimica
Per chiarire cosa fosse davvero determinante, gli autori hanno aggregato i dati di 80 coltivazioni diverse e utilizzato un metodo statistico che cerca fattori nascosti che modellano i risultati. Questa analisi ha evidenziato due temi principali: il sistema di coltura stesso e la morfologia cellulare — se il batterio cresceva come pellet compatti, come reti miceliali allentate o come filamenti finemente dispersi. Le condizioni che producevano morfologie simili tendevano a generare impronte metaboliche più affini e facilitavano la “scalatura” delle molecole dai sistemi piccoli a quello agitato. Selezionando deliberatamente set di condizioni che determinavano forme cellulari comparabili in tutti e tre i sistemi, i ricercatori hanno aumentato la sovrapposizione delle caratteristiche chimiche di circa il 50 percento rispetto al solo adattamento dell’ossigeno secondo la regola classica.
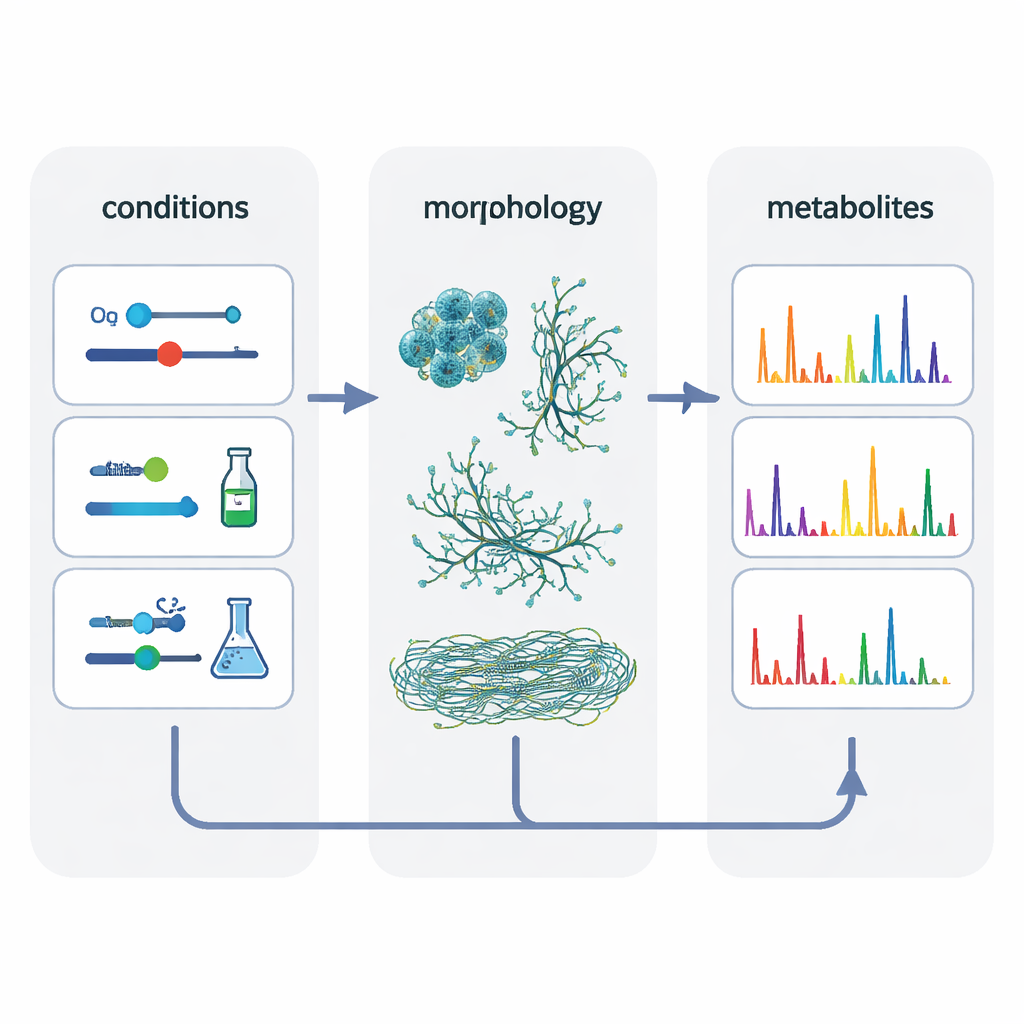
Famiglie chimiche nascoste e molecole specifiche del sistema
Oltre al semplice conteggio dei segnali, il team ha costruito reti molecolari che raggruppano caratteristiche di massa correlate in famiglie di metaboliti strutturalmente affini. Le famiglie ampie spesso contenevano almeno un membro presente in ogni sistema di coltura, suggerendo una chimica di base robusta ai cambiamenti di scala. Ma molte famiglie più piccole — e alcune singole molecole — apparivano soltanto in un tipo di recipiente. Le piastre di polistirene microtiter in particolare hanno prodotto la varietà più ricca di composti, inclusi molti varianti di siderofori leganti il ferro chiamati desferrioxamine e diversi peptidi non ribosomiali. Gli autori suggeriscono che stress sottili in queste piastre, come livelli più elevati di specie reattive dell’ossigeno, possano spingere i batteri a diversificare la loro chimica, mentre il bioreattore ben miscelato favorisce un set più limitato di strutture “core”.
Cosa significa per la scoperta di nuovi prodotti naturali
Per i team di scoperta farmacologica il messaggio è chiaro: non ci si può affidare a una singola regola ingegneristica o a una condizione “ottimale” se si vuole sia una ricca diversità chimica sia una scalabilità affidabile. È necessaria invece una strategia multidimensionale che consideri il tipo di recipiente, il trasferimento di ossigeno, gli additivi come l’etanolo e, cosa importante, il monitoraggio in tempo reale della morfologia cellulare. Usare piastre microtiter che imitino caratteristiche chiave dei bioreattori e sintonizzare le condizioni per ottenere forme di crescita simili può aumentare molto la probabilità che molecole promettenti scoperte a scala microlitro ricompaiano quando coltivate a litri. Questo approccio aiuta a trasformare colpi iniziali fragili in candidati robusti e riproducibili, aumentando le probabilità che nuovi prodotti naturali sopravvivano al percorso dal banco alla farmacia.
Citazione: Lindig, A., Fataeri, M., Hubmann, G. et al. Multidimensional strategy enables scalable metabolome diversity in microbial fermentations. Sci Rep 16, 4084 (2026). https://doi.org/10.1038/s41598-026-37748-9
Parole chiave: scoperta di prodotti naturali, fermentazione di Streptomyces, metabolomica, scalatura in bioreattore, metaboliti secondari