Clear Sky Science · it
Targeting sinergico dell’asse ARID2–MYC con pomalidomide e panobinostat supera la resistenza intrinseca agli IMiD nel mieloma multiplo
Perché questa ricerca è importante per i pazienti
Il mieloma multiplo è un cancro delle cellule produttrici di anticorpi nel midollo osseo che è diventato più trattabile ma resta raramente curabile. Molti pazienti alla fine smettono di rispondere ai farmaci standard, riducendo le opzioni terapeutiche. Questo studio indaga il motivo per cui la combinazione di due classi di farmaci già esistenti—gli IMiD come il pomalidomide e gli inibitori dell’istone deacetilasi (HDAC) come il panobinostat—può agire insieme per uccidere le cellule di mieloma, anche quando il tumore è già resistente agli IMiD da soli. Comprendere questa cooperazione a livello molecolare può orientare combinazioni terapeutiche migliori e permettere a più pazienti di beneficiare di farmaci già disponibili.
Due classi di farmaci datate, una nuova collaborazione
Nelle ultime due decadi, gli IMiD e altri farmaci mirati hanno notevolmente esteso la sopravvivenza delle persone con mieloma multiplo. Gli IMiD agiscono in modo inusuale: invece di limitarsi a bloccare una proteina, causano il marcataggio di specifiche proteine per la distruzione, cancellandole di fatto dalla cellula. In questo modo indeboliscono segnali di sopravvivenza chiave su cui le cellule di mieloma fanno affidamento. Gli inibitori delle HDAC come il panobinostat funzionano diversamente: allentano il fitto impacchettamento del DNA, rimodellando in modo ampio quali geni sono attivi o spenti. Come agenti singoli, gli inibitori delle HDAC hanno effetti modesti e possono causare effetti collaterali, ma i trial clinici avevano suggerito che abbinarli agli IMiD produce una risposta anticancro molto più forte, anche in pazienti la cui malattia non risponde più agli IMiD da soli. Il motivo molecolare di questa sinergia, tuttavia, era rimasto poco chiaro.
Un punto di pressione comune: abbassare MYC
I ricercatori hanno testato sistematicamente combinazioni di diversi IMiD con vari inibitori delle HDAC su una serie di linee cellulari di mieloma, usando un sistema di punteggio standardizzato per misurare quanto le combinazioni fossero più potenti rispetto a ciascun farmaco da solo. Hanno scoperto che pomalidomide più panobinostat mostrava una sinergia particolarmente forte nella maggior parte dei modelli cellulari, e che questo effetto dipendeva da una proteina chiamata cereblon, che gli IMiD sfruttano per indirizzare le loro “vittime” proteiche alla distruzione. Analizzando l’attività genica globale, il gruppo ha rilevato che panobinostat e un altro inibitore HDAC ad azione ampia spegnevano in modo marcato MYC, un gene maestro della crescita spesso descritto come il “motore oncogenico” nelle cellule tumorali, e che gli IMiD esercitavano una pressione addizionale sullo stesso nodo. Quando gli scienziati costrinsero le cellule di mieloma a continuare a produrre MYC da una fonte insensibile ai farmaci, l’effetto potente della coppia di farmaci scomparve in gran parte, dimostrando che l’abbassamento di MYC è centrale per la loro cooperazione.
Superare la resistenza con una via alternativa
Alcune cellule di mieloma sono intrinsecamente resistenti agli IMiD: anche se gli obiettivi iniziali attesi vengono distrutti, MYC e altri segnali di sopravvivenza non vengono adeguatamente spenti, così le cellule continuano a proliferare. In uno di questi modelli resistenti, la via IMiD standard che collega gli obiettivi precoci a MYC era “disaccoppiata”. Il team si è chiesto se esistesse una via alternativa che potesse comunque collegare gli IMiD a MYC. Si sono concentrati su ARID2, componente di una grande macchina di rimodellamento del DNA chiamata complesso SWI/SNF. Lavori precedenti avevano mostrato che il pomalidomide può marcare ARID2 per la distruzione e che ciò contribuisce ad abbassare MYC. Nelle cellule resistenti, il pomalidomide da solo riduceva ARID2 solo modestamente, in parte perché la cellula aumentava la produzione di ARID2 in risposta. Quando veniva aggiunto il panobinostat, questo sopprimeva il gene ARID2 stesso, superando tale circuito di retroazione. Insieme, i due farmaci riducevano fortemente la proteina ARID2 e poi MYC, portando a un potente effetto citotossico anche nelle linee resistenti agli IMiD.
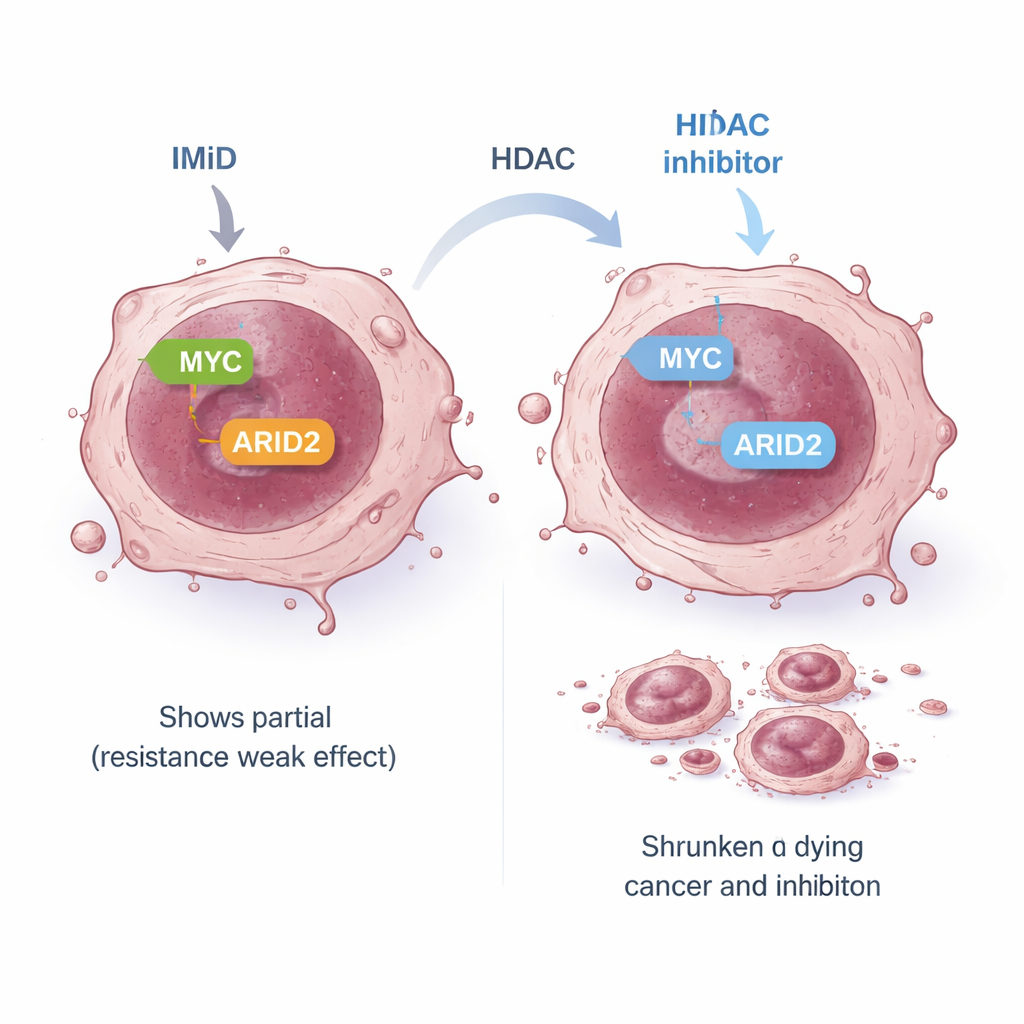
Mettere a nudo una vulnerabilità più ampia nelle cellule tumorali
Poiché ARID2 è solo un membro del complesso SWI/SNF, gli autori si sono chiesti se l’intero complesso potesse costituire un punto debole terapeutico. Hanno scoperto che gli inibitori delle HDAC riducono i livelli di diversi componenti dello SWI/SNF, e che una piccola molecola separata progettata per bloccare i motori centrali del complesso (BRG1/BRM) da sola può rallentare la crescita delle cellule di mieloma e ridurre MYC. Importante, questo inibitore dello SWI/SNF funzionava anche in sinergia con pomalidomide e panobinostat, e una combinazione a tre farmaci abbassava ulteriormente ARID2 e MYC mentre sopprimeva fortemente la proliferazione cellulare. Indagando quali specifiche deacetilasi (HDAC) fossero coinvolte, i ricercatori hanno evidenziato HDAC1 come un attore chiave che aiuta a sostenere la via ARID2–MYC, mentre altre HDAC sembrano influenzare MYC attraverso percorsi paralleli.
Cosa significa per il futuro del trattamento del mieloma
Per i non specialisti, il messaggio centrale è che le cellule di mieloma sembrano dipendere da un “nodo di controllo della crescita” condiviso centrato su MYC, e che esistono più strade che conducono a quel nodo. La terapia IMiD standard colpisce principalmente una di queste strade; in alcuni tumori resistenti, quella strada è bloccata e MYC resta attivo. Questo studio mostra che una via alternativa—tramite ARID2 e il complesso SWI/SNF—rimane percorribile, e che usare panobinostat insieme al pomalidomide può chiuderla. Combinando deliberatamente farmaci che agiscono su MYC da più direzioni, i clinici potrebbero essere in grado di superare alcune forme di resistenza intrinseca riducendo potenzialmente le dosi di ciascun medicinale. Sebbene siano necessari ulteriori studi preclinici e clinici, i risultati forniscono un progetto più chiaro per ideare combinazioni basate sui meccanismi per i pazienti con mieloma multiplo difficili da trattare.
Citazione: Yamamoto, J., Asatsuma-Okumura, T., Ito, T. et al. Synergistic targeting of the ARID2–MYC axis by pomalidomide and panobinostat overcomes intrinsic IMiD resistance in multiple myeloma. Sci Rep 16, 7375 (2026). https://doi.org/10.1038/s41598-026-37740-3
Parole chiave: mieloma multiplo, resistenza ai farmaci, pomalidomide, panobinostat, MYC