Clear Sky Science · it
Meccanismo e divergenza evolutiva di una nuova idrolasi per polivinil alcol ossidato in Stenotrophomonas rhizophila QL-P4
Perché una comune plastica “verde” rimane ancora in natura
Il polivinil alcol, o PVA, è presente in tutto, dalle capsule per detersivo alla carta e ai rivestimenti tessili. Spesso viene commercializzato come ecocompatibile perché, in teoria, i microrganismi possono degradarlo. Eppure in fiumi, suoli e oceani questo materiale simile alla plastica si decompone molto lentamente e può persistere per decenni come frammenti micro- e nanoplastici. Questo studio esamina da vicino uno degli strumenti naturali per affrontare il PVA: un enzima recentemente scoperto in un batterio del suolo che può scindere questo polimero ostinato in pezzi più piccoli e sicuri.
Un piccolo aiutante del suolo con un grande compito
Precedenti ricerche avevano isolato un batterio chiamato Stenotrophomonas rhizophila QL-P4 dal suolo montano in Cina e avevano scoperto che può crescere utilizzando il PVA come fonte di nutrimento. Nel nuovo lavoro i ricercatori si sono concentrati su un singolo gene sospetto, denominato BAY15_0160, che sembrava poter codificare per un enzima capace di tagliare il PVA ossidato. Eliminando attentamente questo gene, reinserendolo e inducendo la sua sovraespressione nel batterio, hanno dimostrato che BAY15_0160 è essenziale per una degradazione efficiente del PVA. Quando il gene è stato rimosso, il microrganismo ha perso circa il 40% della sua capacità di consumare PVA; ripristinarlo ha riportato le prestazioni, confermando che il suo prodotto è un attore chiave nella via di degradazione.
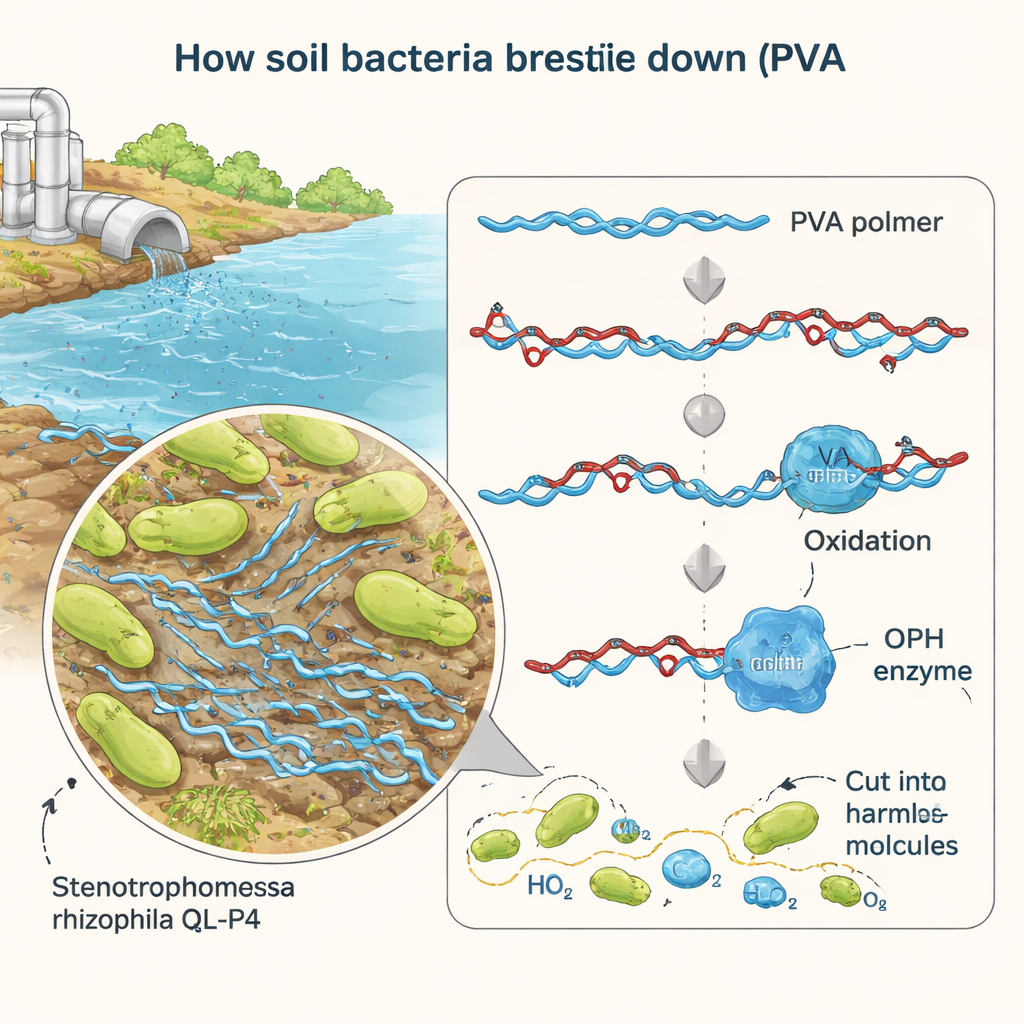
Misurare come lavora l’enzima
Per studiare l’enzima nel dettaglio, il team lo ha prodotto in grandi quantità usando ceppi di laboratorio di Escherichia coli. Hanno purificato la proteina, che è risultata essere di circa 35 kilodalton, e ne hanno testato l’attività sotto diverse condizioni. Utilizzando una molecola di prova semplice che rilascia un colorante giallo quando viene tagliata, hanno monitorato la velocità d’azione dell’enzima a varie temperature e valori di acidità. L’enzima è stato più attivo intorno alla temperatura ambiente (30 °C) e a pH neutro, simile a quello di molte acque naturali. In queste condizioni miti ha mostrato un’elevata efficienza catalitica, cioè ogni molecola di enzima può processare molte molecole di substrato al secondo—una notizia incoraggiante per possibili applicazioni di bonifica sul campo.
Avvicinarsi alle forbici molecolari
Gli enzimi sono le piccole macchine della natura, e la loro forma determina cosa possono fare. I ricercatori hanno usato programmi di predizione allo stato dell’arte, RoseTTAFold e AlphaFold, per costruire modelli tridimensionali dell’enzima che taglia il PVA, ora riconosciuto come una nuova idrolasi per PVA ossidato, o OPH. Entrambi gli strumenti hanno concordato sul fatto che l’enzima presenta il classico ripiegamento “alfa/beta idrolasi” presente in molte cesoie biologiche. Al suo centro si trova un breve motivo—spesso scritto come Gly–X–Ser–X–Gly—che aiuta a posizionare un trio di aminoacidi (serina, aspartato e istidina) per attaccare i legami chimici. Simulazioni al computer hanno mostrato frammenti di PVA ossidato incuneati in questa scanalatura, con la serina chiave che probabilmente effettua il primo taglio della catena.
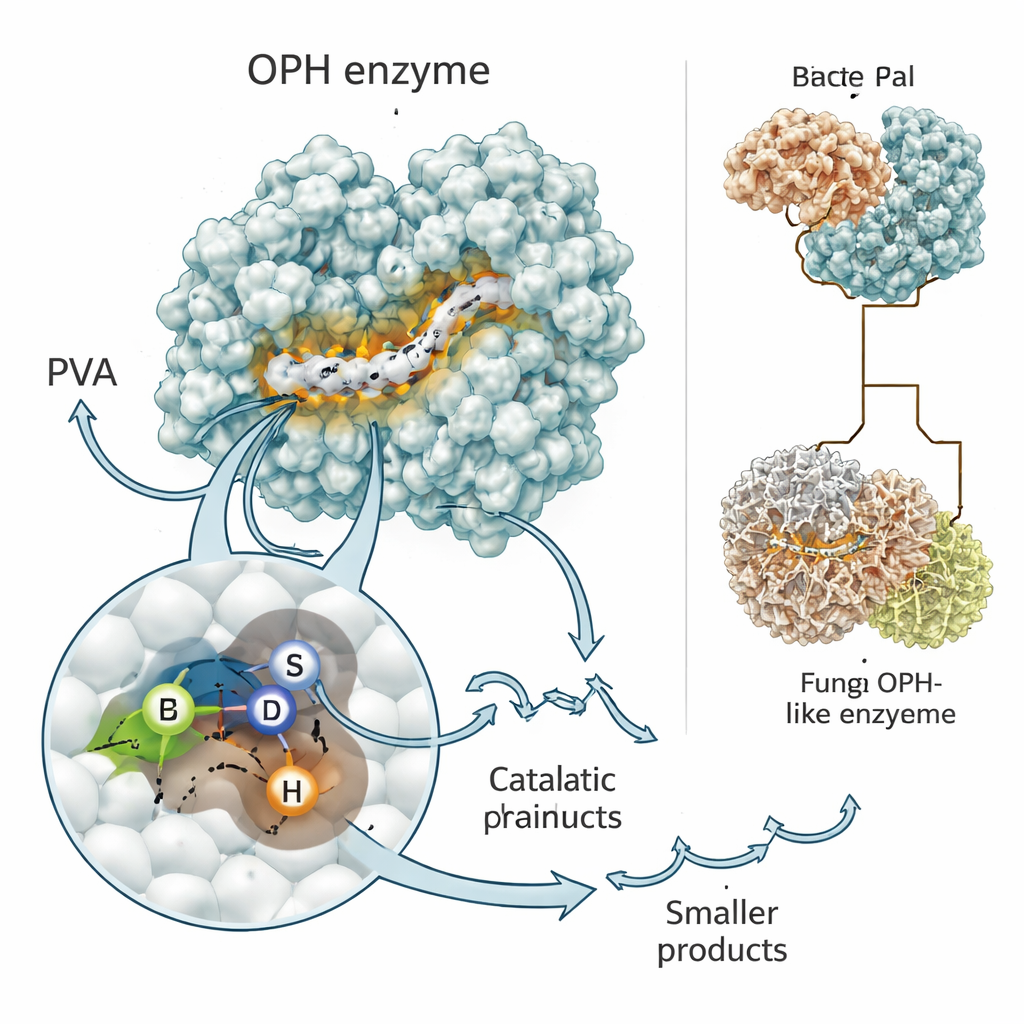
Segnali, interruttori e svolte evolutive
Il team ha anche esplorato quali parti dell’enzima sono assolutamente necessarie per la sua funzione nel batterio. Una regione vicino all’inizio della proteina agisce come un codice postale, indirizzando l’enzima all’esterno della cellula dove si trova effettivamente il polimero PVA. Un’altra regione contiene il motivo catalitico che afferra e scinde i legami carbonio–carbonio della plastica. Quando gli scienziati hanno ingegnerizzato versioni del gene prive sia del segmento segnale sia del motivo del sito attivo, il batterio continuava a produrre RNA del gene ma non riusciva più a digerire efficacemente il PVA. Confrontando molti batteri e funghi, hanno trovato parenti di questo enzima che condividono la stessa regione centrale “tagliente” ma differiscono nelle parti aggiuntive, inclusa una notevole versione fungina che fonde il dominio tagliante con un trasportatore integrato, suggerendo una strategia di importazione e digestione ancora più efficiente in ambienti estremi come le rocce antartiche.
Cosa significa per la bonifica dell’inquinamento da plastica
Per i non specialisti, il messaggio principale è che gli scienziati stanno imparando come alcuni microrganismi degradano naturalmente una plastica considerata biodegradabile che altrimenti rimane in ambiente per troppo tempo. Questo studio individua un singolo enzima, OPH di S. rhizophila QL-P4, come una potente cesoia molecolare che opera in condizioni miti e mira a un passaggio cruciale nella degradazione del PVA. Comprendendo la sua struttura, le condizioni operative e i suoi parenti evolutivi, i ricercatori possono iniziare a progettare ceppi microbici migliori o miscele enzimatiche adatte per impianti di trattamento delle acque reflue, effluenti industriali o suoli contaminati. A lungo termine, tali conoscenze ci avvicinano a soluzioni pratiche basate sulla biologia per gestire i rifiuti di plastica anziché lasciarli accumulare nell’ambiente.
Citazione: Zhou, Y., Bold, N., Feng, J. et al. Mechanism and evolutionary divergence of a novel oxidized polyvinyl alcohol hydrolase in Stenotrophomonas rhizophila QL-P4. Sci Rep 16, 6411 (2026). https://doi.org/10.1038/s41598-026-37715-4
Parole chiave: polivinil alcol, biodegradazione, inquinamento da plastica, enzimi microbici, bonifica biologica