Clear Sky Science · it
Una dieta ad alto contenuto di grassi rimodella le reti di regolazione genica nell’area preoptica
Perché il cervello conta nel diabete
La maggior parte delle persone pensa al diabete come a un problema di pancreas e zucchero nel sangue, ma anche il cervello è profondamente implicato. Questo studio esplora come una dieta ricca di grassi e un potente trattamento sperimentale modifichino l’attività genica in una piccola ma importante area cerebrale chiamata area preoptica. Mappando quali cellule cerebrali si “resettono” quando il diabete va in remissione, i ricercatori sperano di indicare direttive per nuove terapie che sfruttino la capacità intrinseca del cervello di contribuire al controllo della glicemia.
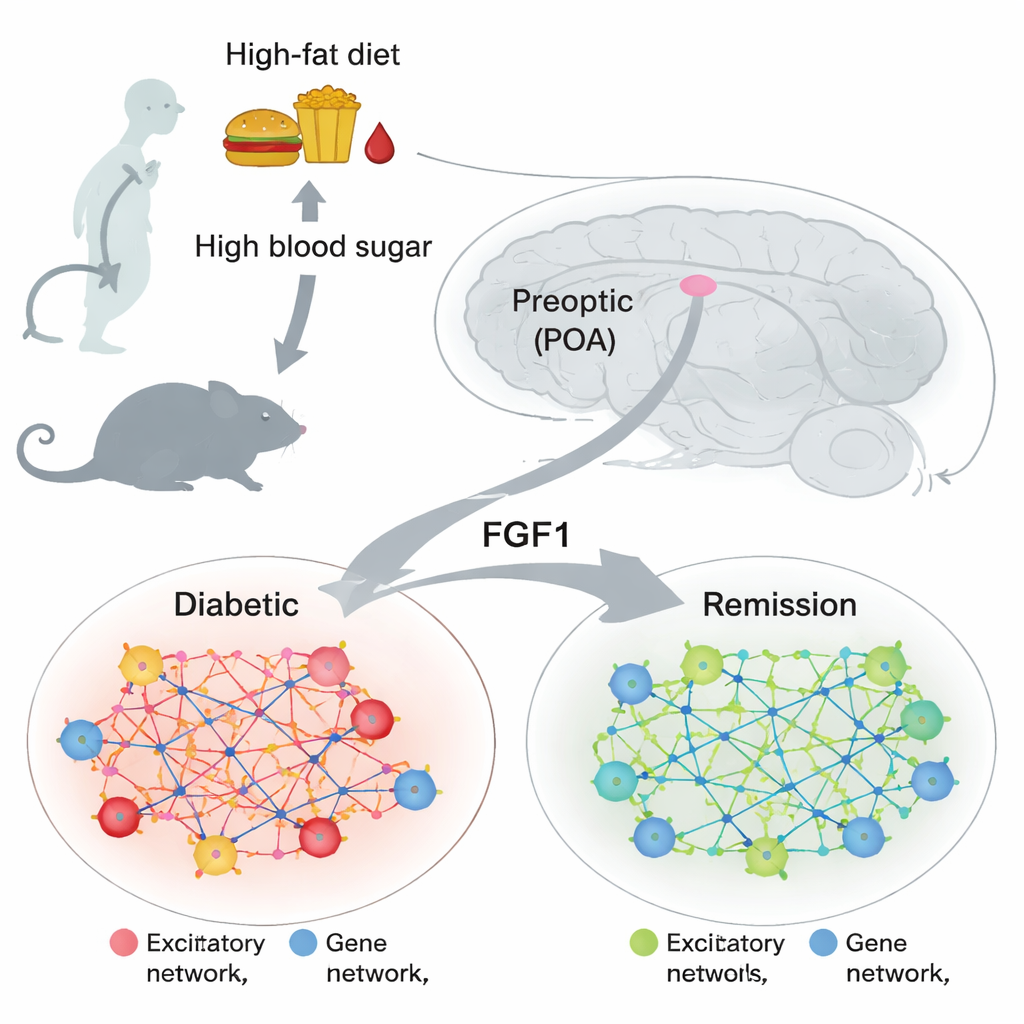
Un piccolo centro cerebrale con grande influenza metabolica
L’area preoptica si trova nella parte anteriore dell’ipotalamo, una porzione del cervello che regola la temperatura corporea, il sonno, l’alimentazione e i segnali ormonali. Studi precedenti hanno mostrato che le cellule di questa regione possono influenzare come il corpo gestisce il glucosio e risponde al calore, ma il loro ruolo nel diabete era poco compreso. Nel contempo, altri lavori hanno rilevato che una singola dose di una proteina chiamata fattore di crescita dei fibroblasti 1 (FGF1), somministrata nel cervello, può indurre la remissione prolungata in topi obesi diabetici. Questo ha sollevato una domanda chiave: quali cellule cerebrali e programmi genici cambiano quando la glicemia si normalizza, e cambi simili si osservano anche nell’area preoptica?
Leggere l’attività genica cellula per cellula
Per rispondere, il team ha utilizzato il sequenziamento dell’RNA a singola cellula, una tecnica che misura quali geni sono attivi in migliaia di cellule individuali contemporaneamente. Hanno rianalizzato un dataset esistente proveniente da topi la cui condizione diabetica era andata in remissione dopo il trattamento con FGF1, concentrandosi sui neuroni dell’ipotalamo. Con strumenti statistici hanno identificato gruppi di geni che aumentavano o diminuivano insieme quando gli animali passavano dallo stato diabetico alla remissione. Questi “moduli di remissione” funzionano come impronte di recupero: invece di seguire un singolo gene alla volta, catturano spostamenti coordinati attraverso molti geni all’interno di specifici tipi neuronali.
Dieta ricca di grassi, cellule cerebrali e riduzione del consumo energetico
I ricercatori hanno quindi confrontato questi moduli di remissione con l’attività genica in un altro dataset che campionava cellule dell’area preoptica di topi normali. Hanno prima separato i neuroni in due classi ampie: cellule eccitatorie, che tendono ad aumentare l’attività nei loro circuiti, e cellule inibitorie, che la attenuano. Nei topi diabetici trattati con FGF1, entrambi i tipi neuronali hanno mostrato ampie riduzioni nei geni legati alla produzione di energia—soprattutto quelli coinvolti nella fosforilazione ossidativa, nella respirazione cellulare e nel macchinario mitocondriale che alimenta le cellule attive. Nei neuroni eccitatori, un ampio modulo genico “turchese” collegato all’uso di energia e all’attività sinaptica è risultato fortemente attenuato in remissione, suggerendo che queste cellule diventano meno esigenti dal punto di vista metabolico quando la glicemia viene riportata sotto controllo.
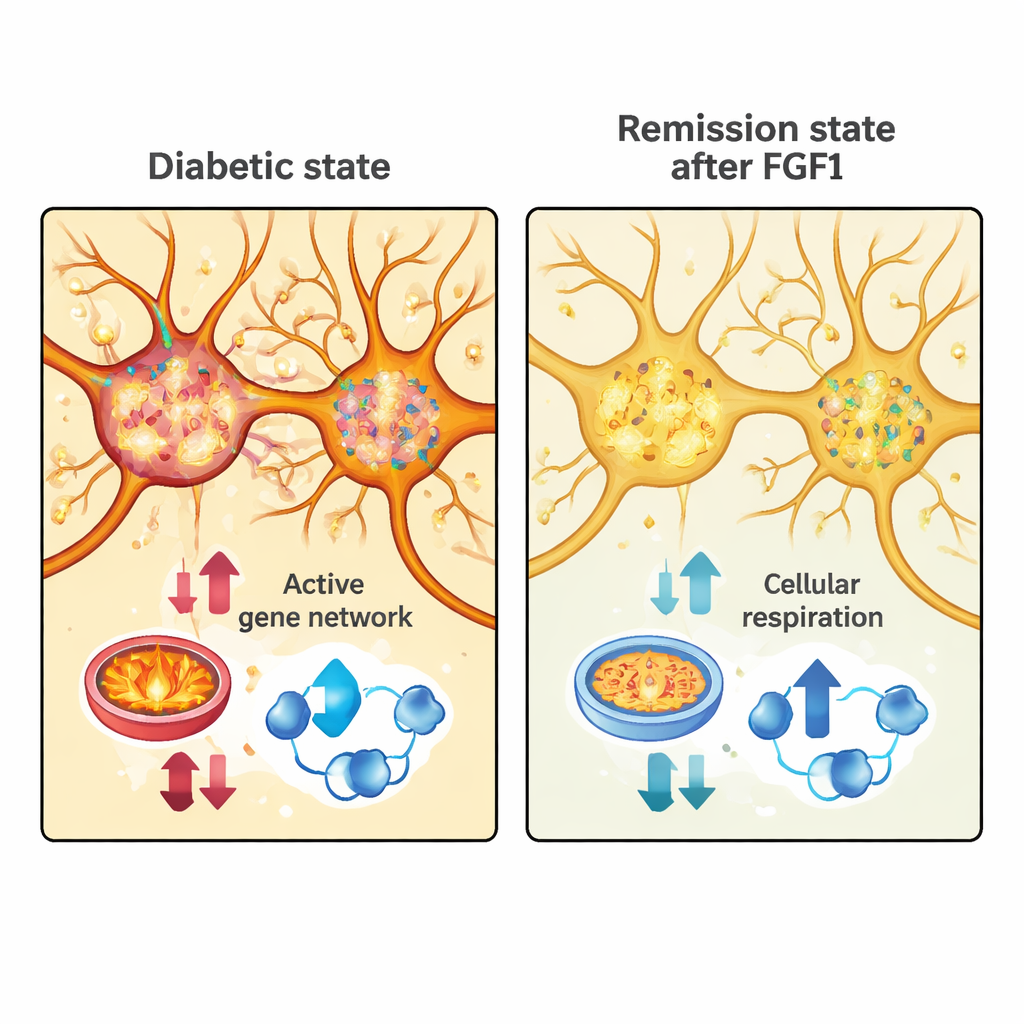
Rintracciare le firme di remissione a gruppi neuronali specifici
Successivamente, il team si è chiesto se questi schemi genici legati alla remissione corrispondessero a popolazioni cellulari particolari nell’area preoptica. Unendo computazionalmente i due dataset, hanno riscontrato che alcuni cluster di neuroni preoptici esprimevano molti degli stessi geni che cambiavano con la remissione indotta da FGF1. Hanno individuato diversi geni—come Trpc4, Dgkg e Ryr3—che si trovavano all’incrocio di queste analisi. Utilizzando un metodo microscopico altamente sensibile chiamato RNAscope, hanno dimostrato che questi geni sono effettivamente espressi in zone distinte dell’area preoptica del topo, per lo più in sottoregioni dorsali. Questo li convalida come marcatori reali di gruppi neuronali specifici che potrebbero partecipare alla risposta cerebrale alle malattie metaboliche.
Cosa significa per i futuri trattamenti del diabete
Per i non specialisti, il risultato principale è che il diabete non è soltanto un problema di zucchero nel sangue—è anche un problema di reti cerebrali. Lo studio mostra che quando il diabete entra in remissione nei topi, alcuni neuroni preoptici passano a uno stato a minore consumo energetico e modificano la loro attività genica in modi coordinati. Definendo questi moduli di remissione e collegandoli a tipi cellulari concreti e geni marker, il lavoro fornisce una mappa per esperimenti futuri: i ricercatori possono ora indirizzare questi neuroni specifici per testare come influenzano il controllo del glucosio, l’obesità e le complicanze correlate. A lungo termine, una migliore comprensione di questi circuiti cerebrali potrebbe aiutare a ispirare terapie che integrino o persino sostituiscano organi in difficoltà sfruttando il controllo intrinseco del cervello sul metabolismo.
Citazione: Lazaro, O., Beimfohr, C., App, B. et al. High fat diet remodels the gene regulatory networks in the preoptic area. Sci Rep 16, 7042 (2026). https://doi.org/10.1038/s41598-026-37692-8
Parole chiave: cervello e diabete, area preoptica, dieta ricca di grassi, reti geniche, remissione FGF1