Clear Sky Science · it
Identificazione in tutto il trascrittoma di varianti deleterie in geni candidati legati alla paratubercolosi bovina
Geni nascosti dietro una malattia bovina costosa
La paratubercolosi bovina, nota anche come malattia di Johne, indebolisce silenziosamente la salute e la produttività dei greggi lattieri in tutto il mondo, costando agli allevatori centinaia di milioni di dollari ogni anno e sollevando preoccupazioni per possibili legami con disturbi intestinali umani. Questo studio scava sotto il cofano genetico delle vacche Holstein per porre una domanda semplice ma cruciale: quali differenze genetiche possono aiutare alcuni animali a resistere all’infezione mentre altri soccombono? Leggendo l’RNA — le copie operative dei geni — nel sangue e nei tessuti intestinali, i ricercatori hanno tracciato come sottili cambiamenti nel DNA in geni chiave del sistema immunitario possano indirizzare l’evoluzione della malattia.
Perché questa malattia bovina è importante
La paratubercolosi è causata dal batterio Mycobacterium avium sottospecie paratuberculosis (MAP). Le vacche si infettano tipicamente nei primi stadi di vita, ma i segni clinici spesso compaiono anni dopo. Nelle fasi silenti e subcliniche gli animali appaiono sani ma possono eliminare bassi livelli di batteri e produrre meno latte. Nelle fasi cliniche sviluppano diarrea cronica, grave perdita di peso e cali marcati della produzione di latte. I tassi di infezione a livello di mandria possono superare il 50% in molte regioni, incluse parti d’Europa e del Nord America, creando una sfida economica e di benessere animale. Poiché il batterio potrebbe anche agire come fattore ambientale scatenante per malattie infiammatorie umane come il morbo di Crohn, cresce la pressione per migliorare le strategie di controllo nel bestiame.
Leggere il genoma operativo
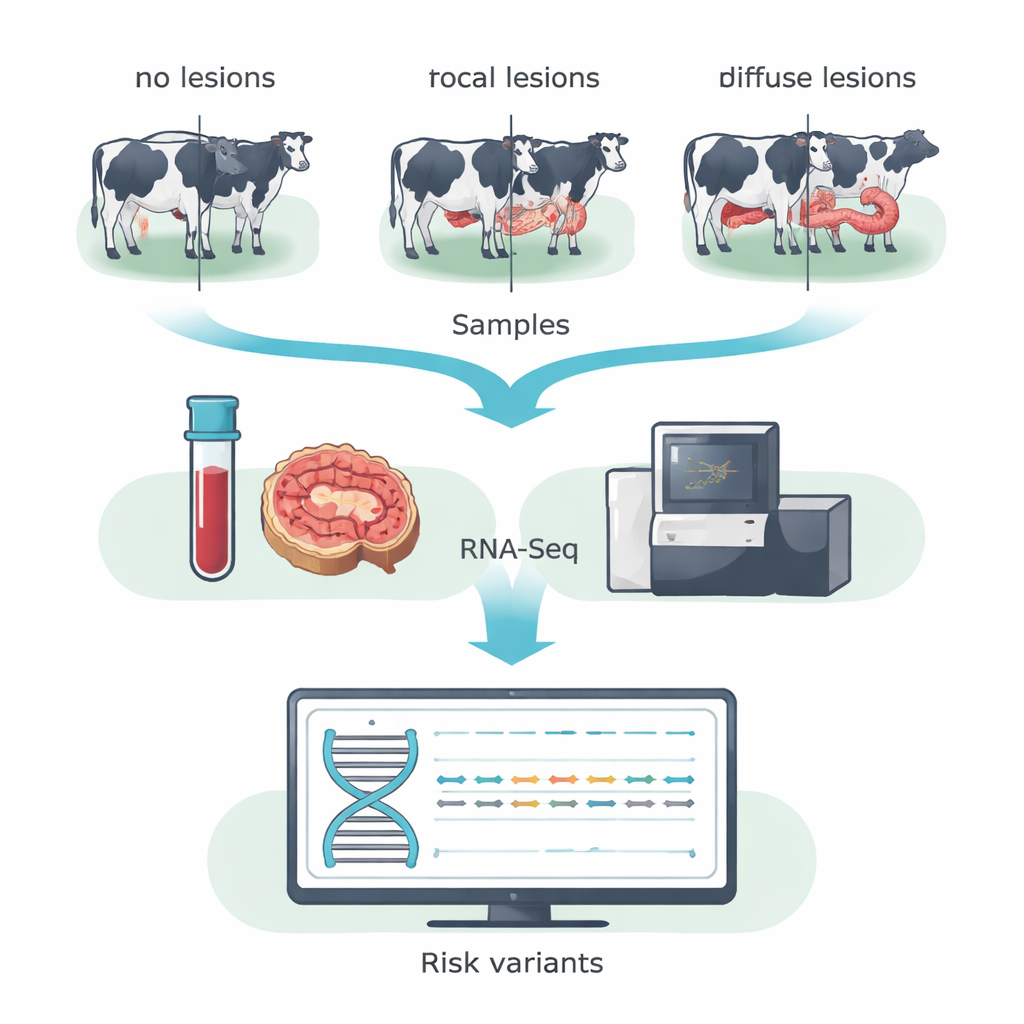
Invece di scandagliare l’intera sequenza del DNA, il team ha usato il sequenziamento dell’RNA (RNA-Seq) per concentrarsi sui geni effettivamente attivi nell’animale. Hanno raccolto sangue e campioni dalla valvola ileocecale — una regione intestinale fortemente colpita dal MAP — da 14 vacche Holstein in una mandria da latte spagnola. Basandosi sull’esame microscopico dei tessuti intestinali, le vacche sono state raggruppate in tre categorie: animali senza lesioni rilevabili, animali con lesioni piccole e localizzate (focali) tipiche di un’infezione subclinica prolungata, e animali con lesioni severe e diffuse associate alla malattia clinica. Unendo i dati di sangue e intestino per ciascun gruppo, i ricercatori hanno aumentato la capacità di rilevare cambiamenti di una singola lettera nel DNA dei geni espressi, noti come SNP codificanti.
Trovare cambiamenti dannosi in geni immunitari chiave
Da centinaia di migliaia di varianti, il team si è concentrato su quelle che alterano la sequenza proteica e sono previste come dannose per la funzione proteica — le cosiddette varianti deleterie. Hanno applicato filtri rigorosi per garantire alta confidenza, poi hanno usato strumenti di predizione consolidati per segnalare i cambiamenti a rischio. Questo processo di selezione ha rivelato 31 varianti di questo tipo uniche nelle vacche senza lesioni, 15 uniche nelle vacche con lesioni focali e 31 uniche nelle vacche con lesioni diffuse. Molte ricadevano in geni che guidano il modo in cui le cellule immunitarie riconoscono ed eliminano le infezioni, regolano la morte cellulare e gestiscono il metabolismo. Un candidato di spicco è stata la famiglia genica BOLA, la versione bovina del complesso maggiore di istocompatibilità di classe II, che aiuta le cellule immunitarie a presentare frammenti batterici ai linfociti T. Diverse varianti potenzialmente dannose in BOLA sono state trovate in tutti e tre i gruppi di vacche, suggerendo che versioni specifiche di BOLA possano inclinare gli animali verso resistenza, infezione controllata o infiammazione dannosa.
Dalle varianti del DNA alle vie patologiche
Per capire cosa potessero significare in pratica questi cambiamenti genici, i ricercatori hanno esaminato quali vie biologiche risultassero arricchite in ciascun gruppo. Le vacche senza lesioni mostravano varianti alterate in geni legati all’elaborazione degli antigeni, al traffico vescicolare e all’equilibrio immunitario intestinale, inclusi BOLA, AP3B1 e CHGA. Questi cambiamenti potrebbero favorire una digestione efficiente dei batteri all’interno delle cellule immunitarie e un ambiente intestinale stabile che limita i danni. Nelle vacche con lesioni focali, le varianti dannose si sono raggruppate in geni (ORMDL3 e KANK2) che attenuano la morte cellulare programmata e regolano il metabolismo cellulare, potenzialmente aiutando l’ospite a mantenere basso il numero di batteri durante una lunga fase subclinica. Nelle vacche con lesioni diffuse, i geni interessati indicavano vie immunitarie iperattivate come la differenziazione delle cellule Th1/Th2 e la presentazione dell’antigene, insieme a rotte di trasporto della bile e di risposta ai farmaci. Qui, i geni alterati della famiglia BOLA potrebbero guidare una reazione infiammatoria forte e talvolta auto‑danneggiante, riecheggiando schemi osservati in molte malattie autoimmuni e infiammatorie umane.
Indizi per allevare greggi più resilienti
Oltre a chiarire come diverse varianti genetiche modellino la risposta immunitaria al MAP, lo studio ha anche collegato questi cambiamenti rischiosi a regioni conosciute del genoma bovino associate a tratti di salute, inclusa la suscettibilità alla paratubercolosi e ad altre infezioni. Pur richiedendo ancora validazione in greggi più ampi e non potendo essere usate al momento come marcatori diagnostici autonomi, offrono un catalogo promettente di varianti e geni candidati. In termini semplici, il lavoro suggerisce che alcune vacche portano versioni geniche che le aiutano a controllare silenziosamente l’infezione, mentre altre portano versioni che favoriscono un’infiammazione incontrollata e malattia grave. In futuro, tali informazioni potrebbero supportare la selezione genetica e test che spostino i greggi verso una maggiore resistenza naturale, riducendo sia le perdite economiche sia la necessità di misure di controllo della malattia intensive.
Citazione: Badia-Bringué, G., Lam, S., Cánovas, Á. et al. Whole-transcriptome identification of deleterious variants in candidate genes linked to bovine paratuberculosis. Sci Rep 16, 6243 (2026). https://doi.org/10.1038/s41598-026-37675-9
Parole chiave: paratubercolosi bovina, genetica della malattia di Johne, immunità del bestiame da latte, sequenziamento RNA, selezione per resistenza alle malattie