Clear Sky Science · it
La segnalazione dell'interferone di tipo I definisce una nuova firma di malattia nei cheratinociti umani con xeroderma pigmentoso C
Perché la luce del sole può essere così pericolosa per alcune persone
Per la maggior parte di noi la luce del sole significa calore e vitamina D. Ma per le persone con una rara condizione genetica chiamata xeroderma pigmentoso C (XP‑C), anche una modesta esposizione alla luce diurna può provocare gravi danni cutanei e un rischio estremamente elevato di cancro della pelle. Questo studio va oltre il noto difetto nella riparazione del DNA in XP‑C e scopre un livello nascosto di segnalazione simile a quella immunitaria iperattiva all'interno delle loro cellule cutanee, offrendo nuovi indizi sul perché la loro pelle sia così vulnerabile e infiammata dopo l'esposizione al sole.
Quando la riparazione del DNA fallisce nella pelle
Le nostre cellule cutanee riparano costantemente i danni al DNA causati dai raggi UVB del sole. Una proteina chiamata XPC è uno dei primi “sensori” che individua le lesioni indotte dall'UV e avvia una grande squadra di riparazione. In XP‑C, mutazioni nel gene XPC compromettono questo primo passo di allerta, così i danni da UV si accumulano invece di essere riparati. I pazienti con XP‑C sviluppano tumori cutanei migliaia di volte più spesso rispetto alla popolazione generale e devono evitare la luce solare con rigore. Pur essendo ben noto questo difetto nella riparazione del DNA, era molto meno chiaro come esso riorganizzi i sistemi di comunicazione interni delle cellule, in particolare quelli che controllano l'infiammazione.
Esaminare i segnali cellulari nel tempo
Per affrontare il problema, i ricercatori hanno ingegnerizzato cheratinociti umani — le principali cellule dello strato esterno della pelle — privi completamente di XPC e li hanno confrontati con cellule normali altrimenti identiche. Hanno esposto entrambi i tipi cellulari a un livello di UVB attentamente selezionato, simile a una dose reale di moderata scottatura. Poi hanno esaminato le cellule in due fasi. Un'ora dopo l'irradiazione hanno misurato l'attività di numerosi enzimi detti chinasici tirosina proteiche, che attivano o disattivano i segnali aggiungendo piccoli tag fosfato. Ventiquattro ore dopo hanno usato spettrometria di massa avanzata per ottenere un'istantanea ampia di migliaia di proteine e vedere quali aumentavano o diminuivano in abbondanza. Questo approccio in due fasi ha permesso di tracciare sia i primi “segnali di allarme” sia le successive “risposte a valle” nelle cellule.
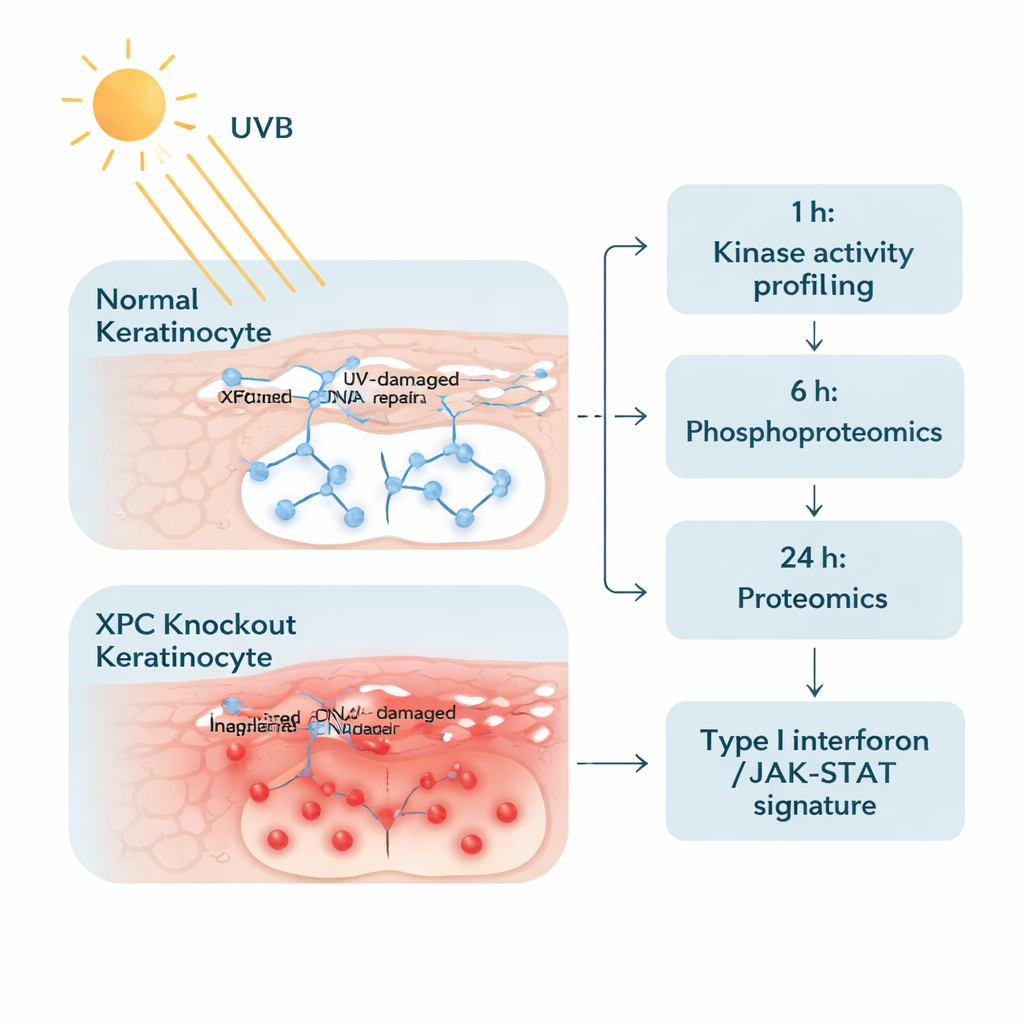
Si accende una via infiammatoria
Lo screening iniziale delle chinasi ha rivelato che i cheratinociti privi di XPC rispondono all'UVB con un’ondata di fosforilazione su oltre cento siti rispetto alle cellule normali. In particolare, molte di queste modifiche si sono concentrate nella via di segnalazione JAK/STAT — una via di comunicazione centrale solitamente utilizzata da messaggeri immunitari come gli interferoni. Marcatori associati a JAK1, JAK2, JAK3, TYK2 e alle proteine STAT erano più attivi nelle cellule XP‑C, già prima dell'UVB, e sono ulteriormente aumentati dopo l'irradiazione. Ciò suggerisce che le cellule erano predisposte in uno stato di “alta allerta”, pronte ad amplificare messaggi infiammatori non appena incontravano lo stress indotto dall'UV.
Geni di allarme in stile interferone nelle cellule della pelle
La successiva e più ampia indagine proteica ha confermato ed esteso questo quadro. Nelle cellule con knockout di XPC, soprattutto dopo l'UVB, centinaia di proteine risultavano alterate, e un grande gruppo corrispondeva a geni normalmente attivati dagli interferoni di tipo I — gli stessi segnali antivirali che il nostro organismo usa per combattere le infezioni. Proteine come MX1, MX2, IFIT1, IFIT2, IFIT3, ISG15, OAS1 e IRF9, classici “geni stimolati da interferone”, risultavano fortemente aumentate. Analisi di rete e di via hanno ricondotto queste proteine alla segnalazione JAK/STAT e agli interferoni di tipo I come tema dominante. Esperimenti di follow‑up con western blot hanno confermato che proteine STAT chiave erano maggiormente fosforilate e che queste proteine sensibili all'interferone venivano prodotte a livelli molto più alti nelle cellule XP‑C rispetto ai cheratinociti normali, sia a riposo sia, in particolare, dopo l'UVB.
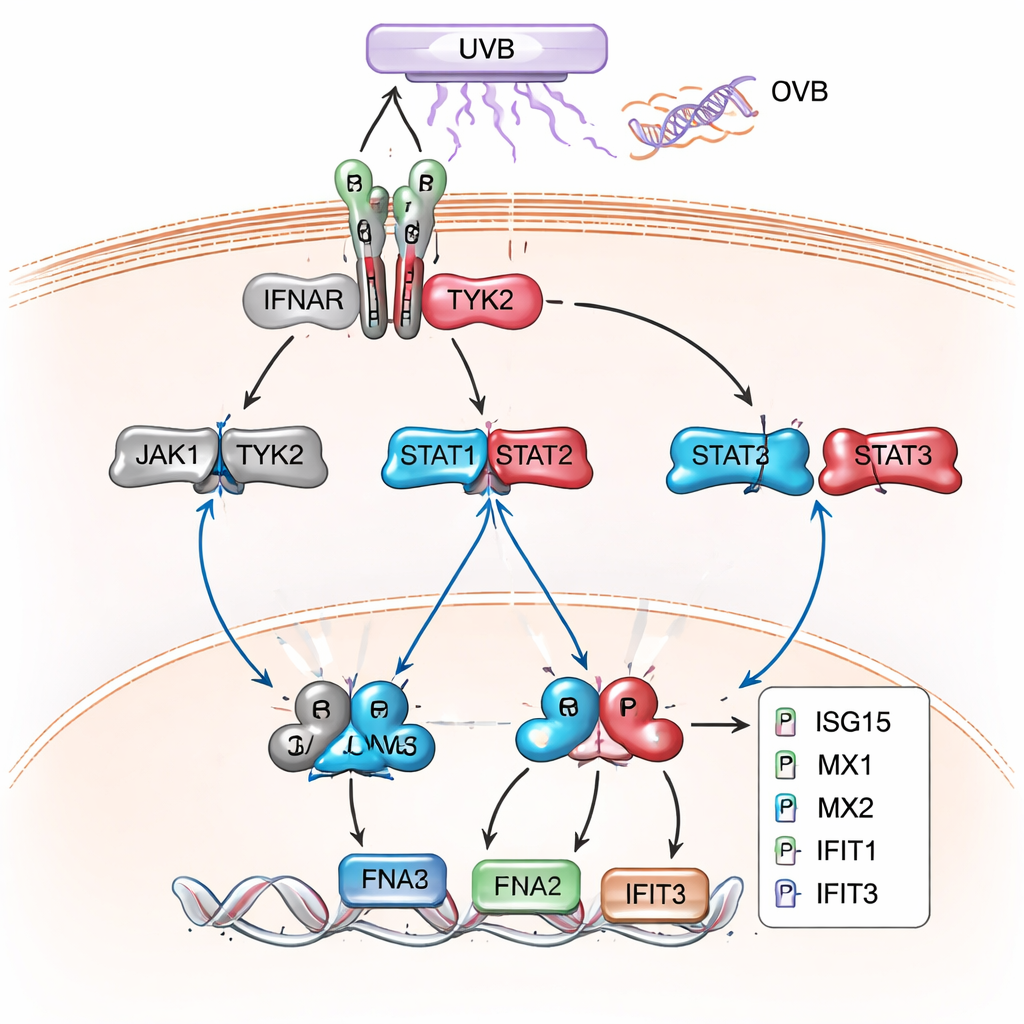
Cosa significa per i pazienti e per i futuri trattamenti
Nel complesso, questi risultati mostrano che XP‑C non è solo una malattia dovuta a una riparazione del DNA difettosa; è anche caratterizzata da uno stato infiammatorio persistente, simile a quello indotto dagli interferoni, all'interno delle cellule cutanee, guidato attraverso la via JAK/STAT e intensificato dalla luce UV. Per un lettore non specialistico, questo significa che i cheratinociti XP‑C si comportano come se stessero costantemente combattendo un'infezione invisibile ogni volta che vedono la luce del sole, sovrapponendo un'infiammazione cronica ai danni del DNA non riparati. Pur non testando direttamente terapie, lo studio solleva la possibilità che farmaci calibrati che prendono di mira JAK/STAT o circuiti infiammatori correlati potrebbero un giorno aiutare a ridurre i danni scatenati dall'UV in XP‑C e forse in altre condizioni infiammatorie della pelle che condividono questa firma molecolare.
Citazione: Nasrallah, A., Rezvani, HR., Belmudes, L. et al. Type I interferon signaling defines a novel disease signature in xeroderma pigmentosum C human keratinocytes. Sci Rep 16, 6559 (2026). https://doi.org/10.1038/s41598-026-37662-0
Parole chiave: xeroderma pigmentoso, cancro della pelle, riparazione del DNA, segnalazione dell'interferone, via JAK STAT