Clear Sky Science · it
Wnt-3a aggrava la produzione di TNF-α nelle microglia stimolate con LPS indipendentemente dalla via canonica β-catenina
Perché l’infiammazione cerebrale è importante
Molti disturbi cerebrali, inclusa la malattia di Parkinson, sono ormai noti per coinvolgere infiammazione cronica. In questo processo, le cellule immunitarie residenti del cervello, chiamate microglia, possono passare da ruoli protettivi a uno stato iperattivato che danneggia i neuroni vicini. Questo studio pone una domanda attuale: una molecola di segnalazione chiamata Wnt‑3a, a lungo ritenuta dai più dotata di effetti calmanti e protettivi, può in certe condizioni peggiorare l’infiammazione? La risposta risulta più complessa del previsto e mette in luce perché la stessa molecola possa risultare utile in un contesto e dannosa in un altro.
Un messaggero con due facce
Le proteine Wnt sono una famiglia di messaggeri chimici che guidano lo sviluppo cerebrale, mantengono le cellule cerebrali nell’adulto e modulano come le cellule rispondono a lesioni. Uno dei membri meglio studiati, Wnt‑3a, è solitamente associato a una via di segnalazione “canonica” che stabilizza una proteina chiamata β‑catenina all’interno delle cellule. In molti sistemi l’attivazione di questa via sembra attenuare l’infiammazione e sostenere la sopravvivenza neuronale, perciò alcuni ricercatori si sono chiesti se potenziare Wnt‑3a possa proteggere i neuroni dopaminergici vulnerabili nella malattia di Parkinson. Tuttavia, le Wnt possono anche segnalare attraverso vie alternative, “non canoniche”, che possono invece promuovere infiammazione, e quale via predomini può dipendere dal tipo cellulare e dal suo stato.
Quando le cellule calme restano calme
Per esplorare queste possibilità, i ricercatori hanno studiato microglia primarie coltivate da cervelli di topo. Hanno iniziato osservando microglia in uno stato riposante, omeostatico, ed esponendole solo a Wnt‑3a. In queste condizioni di quiete, Wnt‑3a non ha aumentato il rilascio di molecole infiammatorie chiave come TNF‑α o IL‑1β. Pur essendo stata attivata parte della segnalazione intracellulare, le microglia non hanno adottato uno stato fortemente infiammatorio. Questo suggerisce che in un cervello sano e non infiammato, l’aggiunta di Wnt‑3a da sola possa avere scarso impatto diretto sulla produzione infiammatoria delle microglia.
Quando le cellule infiammate vengono spinte oltre
Il quadro è cambiato drasticamente una volta che le microglia sono state prima attivate in uno stato infiammatorio usando il lipopolisaccaride batterico (LPS), uno strumento standard per simulare l’infezione in laboratorio. Come previsto, LPS da solo ha indotto un forte aumento della produzione di TNF‑α. Ma quando Wnt‑3a è stato aggiunto insieme a LPS, le microglia hanno rilasciato quantità significativamente maggiori di TNF‑α rispetto al solo LPS, mentre l’IL‑1β non è aumentata ulteriormente. Misurazioni dettagliate hanno mostrato che questo aumento di TNF‑α non derivava da una maggiore attivazione della via infiammatoria NFκB né da una attivazione aggiuntiva della via canonica β‑catenina. Bloccare la via β‑catenina con una proteina chiamata DKK1 non ha eliminato l’impennata di TNF‑α indotta da Wnt‑3a, indicando che la via “anti‑infiammatoria” attesa non era responsabile.
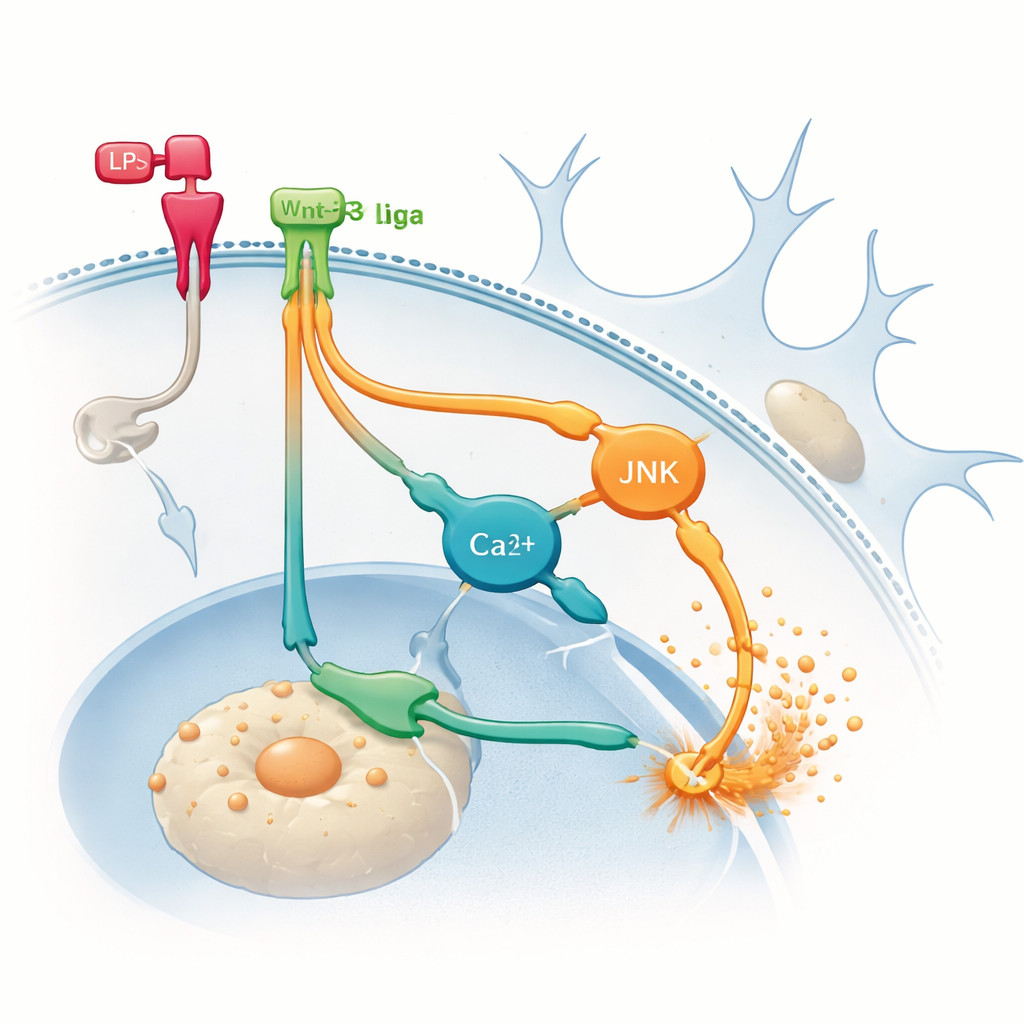
Vie nascoste che alimentano il fuoco
Per individuare l’origine della infiammazione aggiuntiva, il gruppo si è concentrato sulle vie non canoniche alternative che le Wnt possono usare. Hanno bloccato farmacologicamente due rami di segnalazione all’interno delle microglia: uno che coinvolge la proteina JNK e un altro legato a variazioni dei livelli di calcio intracellulare. Inibire uno di questi rami ha ridotto la produzione di TNF‑α indotta da LPS e, cosa importante, ha impedito a Wnt‑3a di aumentare ulteriormente il TNF‑α. Questi risultati suggeriscono che, una volta che le microglia sono già infiammate, Wnt‑3a può passare a utilizzare principalmente vie non canoniche che amplificano i segnali infiammatori anziché calmarli. In altre parole, lo stesso messaggero può percorrere strade interne diverse a seconda dello stato iniziale della cellula, con esiti molto differenti.
Test in un modello di Parkinson
I ricercatori hanno quindi chiesto se questo comportamento di Wnt‑3a nelle microglia si traducesse in effetti maggiori sui neuroni in un cervello vivente. Hanno infuso Wnt‑3a direttamente nei ventricoli cerebrali di topi trattati con la tossina MPTP, un modello ampiamente usato per replicare il danno ai neuroni dopaminergici e l’attivazione microgliale simili al Parkinson. Come previsto, MPTP ha ridotto il numero di neuroni dopaminergici e aumentato il numero di microglia in una regione del mesencefalo critica per il movimento. Tuttavia, l’aggiunta di Wnt‑3a non ha ulteriormente peggiorato la perdita neuronale né ha modificato in modo significativo i conteggi microgliali rispetto agli animali trattati con veicolo. In questo contesto in vivo complesso, Wnt‑3a non ha né salvato né chiaramente aggravato gli effetti dannosi della tossina nel periodo di osservazione studiato.
Cosa significa per le terapie future
Nel complesso, lo studio mostra che Wnt‑3a non è un interruttore semplice per l’infiammazione cerebrale. Nelle microglia quiescenti ha scarso effetto, ma nelle cellule già infiammate può aumentare selettivamente il rilascio di TNF‑α attraverso vie di segnalazione non canoniche, indipendentemente dalla classica via β‑catenina. Allo stesso tempo, l’aggiunta di Wnt‑3a in un modello murino simile al Parkinson non ha protetto né chiaramente danneggiato i neuroni dopaminergici nel breve termine. Per chi lavora a potenziali terapie, il messaggio chiave è che modulare la segnalazione Wnt richiederà un’attenta considerazione del contesto cellulare. Terapie basate su Wnt‑3a o molecole correlate potrebbero essere utili in alcune situazioni ma rischiare di ritorcersi contro se, involontariamente, intensificassero un’infiammazione dannosa.
Citazione: Federici, G., Stayte, S., Rentsch, P. et al. Wnt-3a exacerbates production of TNF-α in LPS stimulated microglia independent of the β-catenin canonical pathway. Sci Rep 16, 8222 (2026). https://doi.org/10.1038/s41598-026-37653-1
Parole chiave: infiammazione cerebrale, microglia, segnalazione Wnt, malattia di Parkinson, TNF-alpha