Clear Sky Science · it
Le popolazioni di APOL1 nella membrana plasmatica resistono alla rapida degradazione proteica
Perché il «trucco della sparizione» di una proteina renale è importante
Una larga quota delle forme gravi di malattia renale nelle persone di recente ascendenza africana è stata ricondotta a due varianti di un unico gene, APOL1. Eppure gli scienziati faticano ancora a spiegare esattamente come questo gene danneggi le cellule renali senza compromettere la maggior parte dei portatori. Questo studio pone una domanda apparentemente semplice ma dalle grandi implicazioni: una volta che la proteina APOL1 è stata sintetizzata all’interno delle cellule, quanto tempo rimane e dove è più stabile? Le risposte rivelano una doppia personalità sorprendente: APOL1 viene rapidamente distrutta all’interno della cellula ma rimane ostinatamente stabile quando è inserita nella superficie esterna della cellula, un indizio che potrebbe indirizzare future terapie.
Gene di rischio con doppio taglio
Il gene APOL1 contribuisce a proteggere l’uomo da alcuni parassiti, un vantaggio evolutivo che probabilmente spiega perché le sue varianti di rischio, chiamate G1 e G2, sono comuni nelle popolazioni africane. Sfortunatamente, le persone che ereditano due copie di queste varianti affrontano un rischio marcatamente aumentato di disturbi renali raggruppati come malattie renali mediate da APOL1. Lavori precedenti hanno mostrato che quando i livelli di APOL1 aumentano—spesso in risposta all’infiammazione—la proteina può diventare tossica, specialmente nelle delicate cellule filtranti renali note come podociti. Ma la maggior parte degli studi si è concentrata su ciò che attiva APOL1. Molto meno si sapeva su come le cellule la spengono di nuovo, per esempio degradando la proteina.
Seguire una proteina fragile all’interno delle cellule
Per esplorare la stabilità di APOL1, i ricercatori hanno ingegnerizzato linee cellulari umane per produrre versioni fluorescenti dell’APOL1 e del suo parente più vicino, APOL2. Questo ha permesso di osservare quanto di ciascuna proteina si accumulasse o scomparisse in diverse condizioni usando western blotting, microscopia e citometria a flusso. Hanno bloccato la principale macchina cellulare di demolizione delle proteine, il proteasoma, e separatamente hanno bloccato la nuova sintesi proteica. Quando i proteasomi sono stati inibiti, i livelli di APOL1 sono aumentati rapidamente, dimostrando che normalmente viene degradato a ritmo sostenuto. Quando la sintesi proteica è stata interrotta, i livelli di APOL1 sono calati rapidamente. In netto contrasto, APOL2 è cambiato di poco con entrambi i trattamenti, rivelandosi una proteina molto più stabile. È importante notare che l’alto turnover di APOL1 era lo stesso per la versione normale (G0) e per le versioni di rischio renale (G1 e G2), e valeva per diverse forme naturali di APOL1 che differiscono nel modo in cui si collocano nelle membrane.
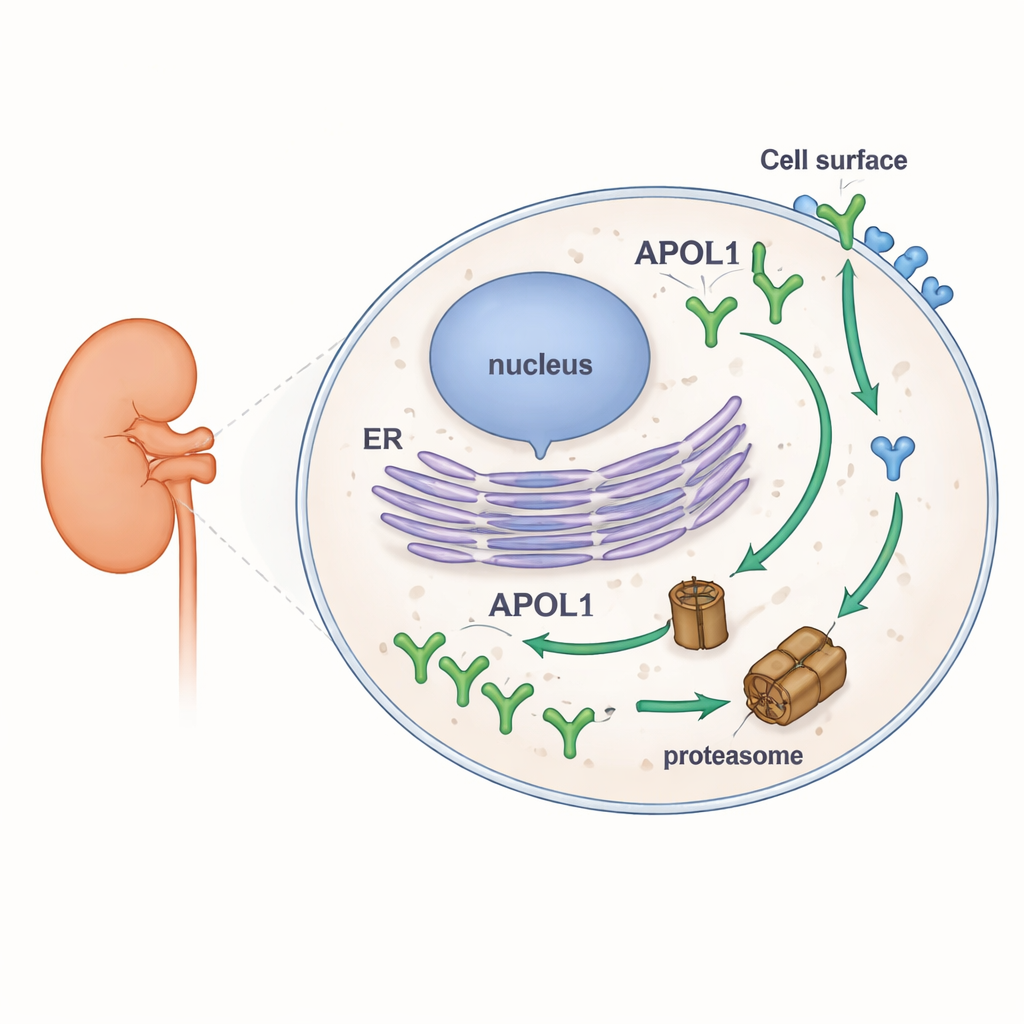
Indizi di sequenza e la storia di due quartieri
Approfondendo la struttura della proteina, il team ha usato strumenti computazionali per scandagliare APOL1 e APOL2 alla ricerca di segmenti flessibili e non strutturati noti come regioni intrinsecamente disordinate. Tali regioni spesso fungono da segnali di «mangiami» per il proteasoma. Hanno identificato due regioni candidate forti in APOL1 che erano in gran parte assenti in APOL2. Per testare se l’estremità anteriore unica di APOL1 contribuisse alla sua fragilità, hanno creato ibridi: un APOL1 accorciato privo dei primi 59 amminoacidi e un chimerico APOL2 contenente quel segmento di APOL1. L’aggiunta del pezzo N-terminale di APOL1 ad APOL2 rese APOL2 soggetto a degradazione più rapida, mentre l’APOL1 troncato rimase instabile, suggerendo che più di una parte di APOL1 favorisce la rapida demolizione. Nel complesso, questi risultati collegano gli insoliti segmenti flessibili di APOL1 al suo rapido turnover, senza legare questo comportamento specificamente alle varianti che causano la malattia.
Proteina ostinata sulla superficie cellulare
La scoperta più sorprendente emerse quando gli autori distinsero tra APOL1 all’interno della cellula e APOL1 sulla superficie cellulare. Usando anticorpi che riconoscono solo la porzione di APOL1 esposta all’esterno, hanno misurato separatamente i livelli superficiali dai livelli totali. All’interno della cellula, APOL1 si comportava come previsto: si accumulava quando i proteasomi erano bloccati e spariva rapidamente quando si fermava la nuova sintesi. L’APOL1 superficiale, invece, è rimasta sostanzialmente immobile in entrambe le condizioni. Una volta che le molecole di APOL1 raggiungevano la membrana plasmatica, si sono dimostrate altamente resistenti alla rapida degradazione. Inoltre, sebbene le varianti di rischio producessero meno APOL1 totale rispetto alla versione normale, i loro livelli superficiali erano simili. Questo suggerisce che le forme di rischio e quella normale vengano eliminate a ritmi comparabili all’interno della cellula, ma che le popolazioni inserite nella membrana—che si pensa formino canali ionici e guidino la tossicità—vengano preservate in tutte le varianti.
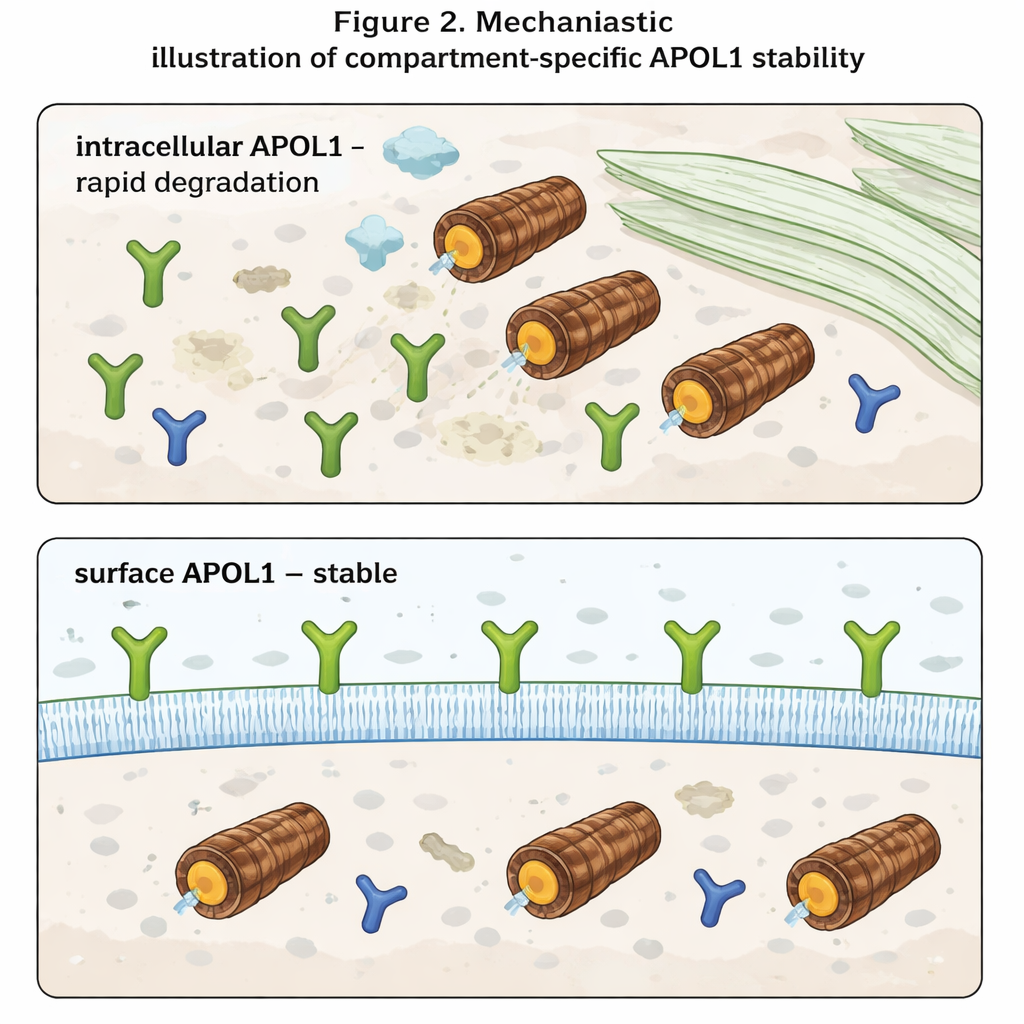
Cosa significa per futuri trattamenti
Per i non specialisti, il messaggio principale è che APOL1 si comporta in modo molto diverso a seconda di dove si trova. All’interno della cellula è una proteina di breve durata, rapidamente riconosciuta e distrutta. Sulla superficie cellulare diventa a lunga vita e relativamente protetta, anche quando la macchina di degradazione della cellula è alterata. Poiché la malattia sembra insorgere quando i canali APOL1 sulla superficie disturbano l’equilibrio di ioni come sodio e potassio, le terapie potrebbero dover puntare meno sui livelli totali di APOL1 e più su quanto ne raggiunge e persiste nella membrana plasmatica. Strategie che riducano il traffico di APOL1 verso la superficie o che destabilizzino selettivamente la popolazione superficiale potrebbero, in linea di principio, attenuare il danno renale senza bloccare completamente le funzioni immunitarie benefiche del gene.
Citazione: Höffken, V., Alvermann, L., Niggemeier, D. et al. APOL1 plasma membrane pools resist rapid protein degradation. Sci Rep 16, 6718 (2026). https://doi.org/10.1038/s41598-026-37647-z
Parole chiave: APOL1, malattia renale, degradazione proteica, membrana plasmatica, proteasoma