Clear Sky Science · it
Modello per la descrizione delle interazioni tra ellagitannini e ioni Fe(II)
Perché i composti vegetali nei mangimi animali sono importanti
I batteri resistenti agli antibiotici rappresentano una preoccupazione crescente sia per gli allevatori sia per la sanità pubblica. Molti di questi microrganismi difficili da trattare emergono nel bestiame, dove gli antibiotici sono ancora ampiamente usati nei mangimi. Questo studio esamina i tannini — composti naturali di origine vegetale — come valida alternativa. In particolare, spiega come un gruppo speciale di tannini derivati dal legno di castagno possa legare il ferro in modi che potrebbero privare i batteri di un nutriente essenziale per la loro crescita.
Difensori naturali nascosti negli alberi
I tannini sono molecole vegetali amare che danno a un vino rosso la sua astringenza e sono state impiegate per secoli nella concia delle pelli e nella produzione di inchiostri. Si trovano in abbondanza in molti mangimi e alimenti e sono generalmente sicuri per animali e persone. Alcuni tipi, detti ellagitannini, sono particolarmente interessanti perché possiedono molte piccole “mani” chimiche in grado di aggrapparsi a ioni metallici come il ferro. L’estratto di legno di castagno, già utilizzato nei mangimi, contiene diversi ellagitannini, inclusi due grandi composti chiamati roburina A e roburina D. Lavori precedenti avevano mostrato che parenti più semplici di questi composti possono legare il ferro e ostacolare l’accesso dei batteri a questo elemento essenziale.
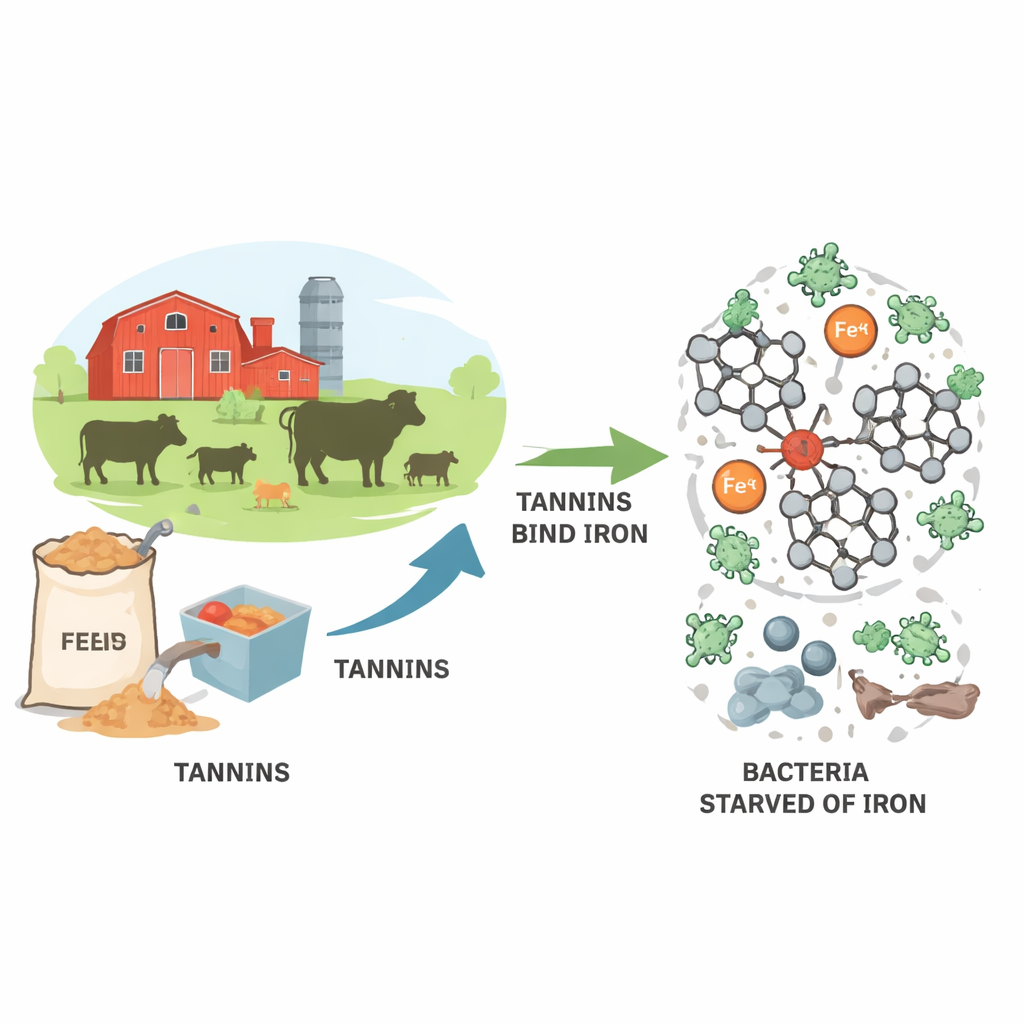
Privare i batteri del loro metallo preferito
I batteri non possono prosperare senza ferro. Lo usano per alimentare la respirazione, costruire il DNA e svolgere molte reazioni enzimatiche. Nell’intestino degli animali o nei terreni di coltura lo ottengono normalmente tramite piccole molecole che producono per catturare il ferro. Gli ellagitannini interferiscono con questo processo formando complessi stretti con gli ioni di ferro, «blindando» di fatto il metallo e impedendone l’accesso ai batteri. Gli autori si sono concentrati sul ferro nella sua forma Fe(II), lo stato che viene rapidamente catturato dai tannini in soluzione acquosa prima di ossidarsi lentamente a Fe(III). Isolando roburina A e D dall’estratto di castagno e studiandole in soluzioni attentamente controllate, il gruppo ha potuto seguire quanto efficacemente questi grandi tannini rimuovono il ferro dalla fase liquida.
Investigare come i tannini afferrano il ferro
Per capire i dettagli, i ricercatori hanno prima esaminato come le roburine acquistano e perdono protoni (un processo chiamato equilibrio acido–base) al variare del pH. Usando spettroscopia nell’ultravioletto-visibile, hanno seguito come l’assorbimento di luce delle roburine cambiava attraverso diversi livelli di pH. Questi spostamenti hanno rivelato che roburina A e D si comportano in modo simile ai loro cugini più piccoli, vescalagin e castalagin, ma con circa il doppio dei siti in grado di perdere un protone e partecipare poi al legame con il ferro. Successivamente hanno miscelato tannini e ferro in rapporti variabili e, ancora una volta tramite assorbimento di luce, hanno costruito i cosiddetti grafici di Job, che mostrano quale proporzione di mescolamento produce la massima formazione del complesso ferro–tannino. Da questi dati hanno dedotto che ogni molecola di roburina può legare sei ioni Fe(II) — il doppio della capacità dei più piccoli ellagitannini.
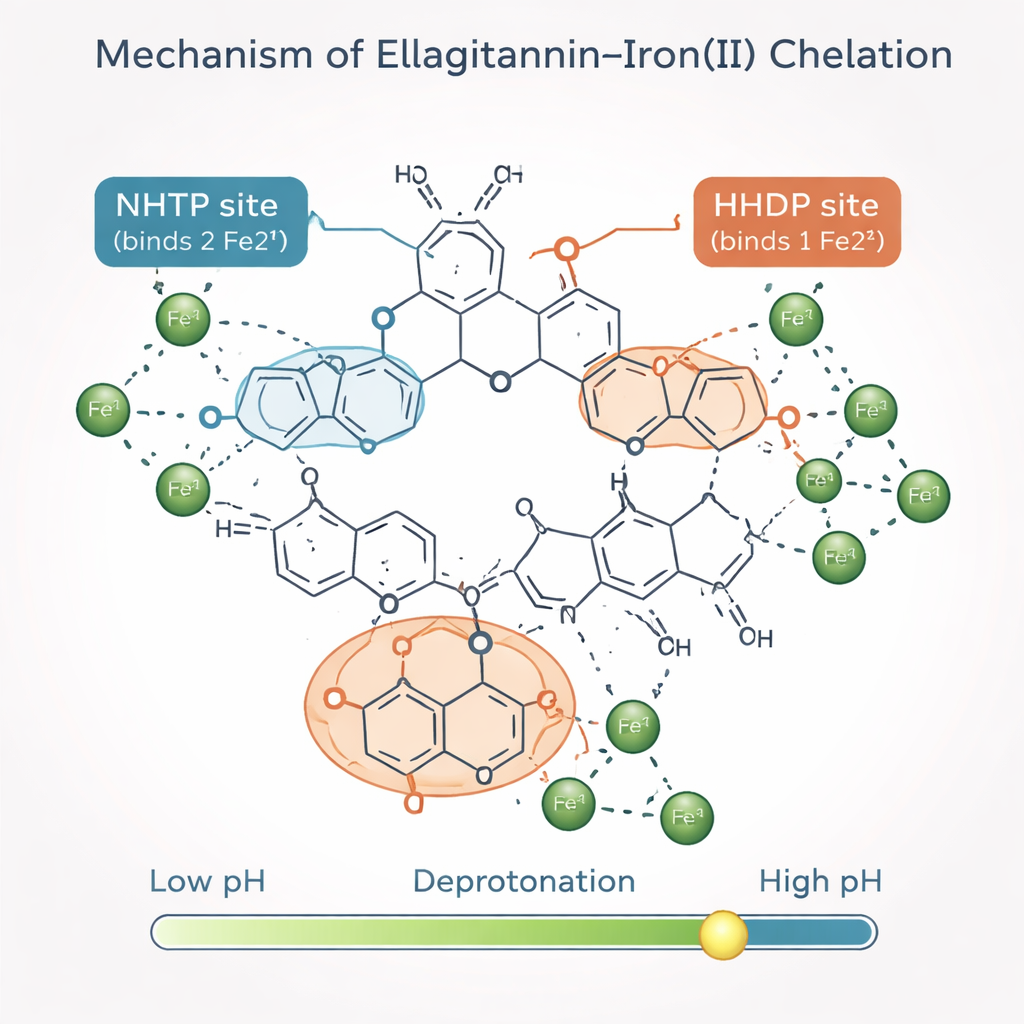
Una mappa predittiva dei punti caldi per il legame con il ferro
Oltre a quantificare quanti ioni di ferro possono essere catturati, gli autori hanno voluto capire quali «moduli» strutturali degli ellagitannini svolgono il lavoro. Hanno costruito un modello matematico che tratta ogni molecola di ellagitannino come una collezione di blocchi costitutivi ripetuti. Due moduli chiave, chiamati gruppi NHTP e HHDP, offrono ciascuno siti specifici di legame per il ferro una volta che hanno perso i loro protoni più acidi. Combinando le nuove misure con precedenti dati di risonanza magnetica nucleare e spettroscopia, il gruppo ha mostrato che ogni gruppo NHTP lega tipicamente due ioni di ferro, mentre ogni gruppo HHDP ne lega uno. Con pochi parametri aggiustabili, il loro modello ha riprodotto accuratamente i grafici di Job sperimentali non solo per gli ellagitannini più semplici ma anche per le roburine più grandi che non erano state utilizzate per tarare il modello.
Implicazioni per un’agricoltura più sostenibile
In termini pratici, questo lavoro traduce la complessa chimica dei tannini e del ferro in un insieme di regole utilizzabili. Mostra che contando le unità NHTP e HHDP in un ellagitannino, gli scienziati possono prevedere quanti ioni di ferro una data molecola catturerà in un intervallo di condizioni lievemente acide. Poiché gli estratti di castagno ricchi di roburine sequestrano più ferro rispetto ai tannini più piccoli o agli acidi vegetali semplici, sono candidati promettenti per limitare la disponibilità di ferro ai batteri dannosi nell’intestino degli animali da allevamento. Sebbene siano necessarie ulteriori ricerche — in particolare su altre strutture di tannini e su forme diverse del ferro — questo modello aiuta a orientare la progettazione e la selezione di additivi vegetali per mangimi che potrebbero ridurre la dipendenza dagli antibiotici convenzionali e sostenere una produzione zootecnica più sostenibile e «green».
Citazione: Frešer, F., Hostnik, G. & Bren, U. Model for the description of interactions between ellagitannins and Fe(II) ions. Sci Rep 16, 6631 (2026). https://doi.org/10.1038/s41598-026-37616-6
Parole chiave: ellagitannini, chelazione del ferro, tannini nei mangimi animali, alternative agli antibiotici, estratto di legno di castagno