Clear Sky Science · it
L'inattivazione di LIMK2 sopprime la differenziazione dei fibroblasti dermici indotta da stimoli meccanici e la resistenza all'apoptosi
Perché alcune cicatrici crescono in modo incontrollato
La maggior parte dei tagli e delle ferite chirurgiche lascia una linea sottile e piatta. Ma in alcune persone il processo di guarigione accelera in eccesso, formando cicatrici spesse e rilevate chiamate cicatrici ipertrofiche o cheloidi che possono prudere, far male e limitare il movimento. Questo studio indaga perché le cellule cutanee ordinarie a volte diventano produttrici di cicatrici troppo aggressive e individua un singolo interruttore molecolare, chiamato LIMK2, che potrebbe essere modulato per impedire alle cicatrici di crescere fuori controllo.
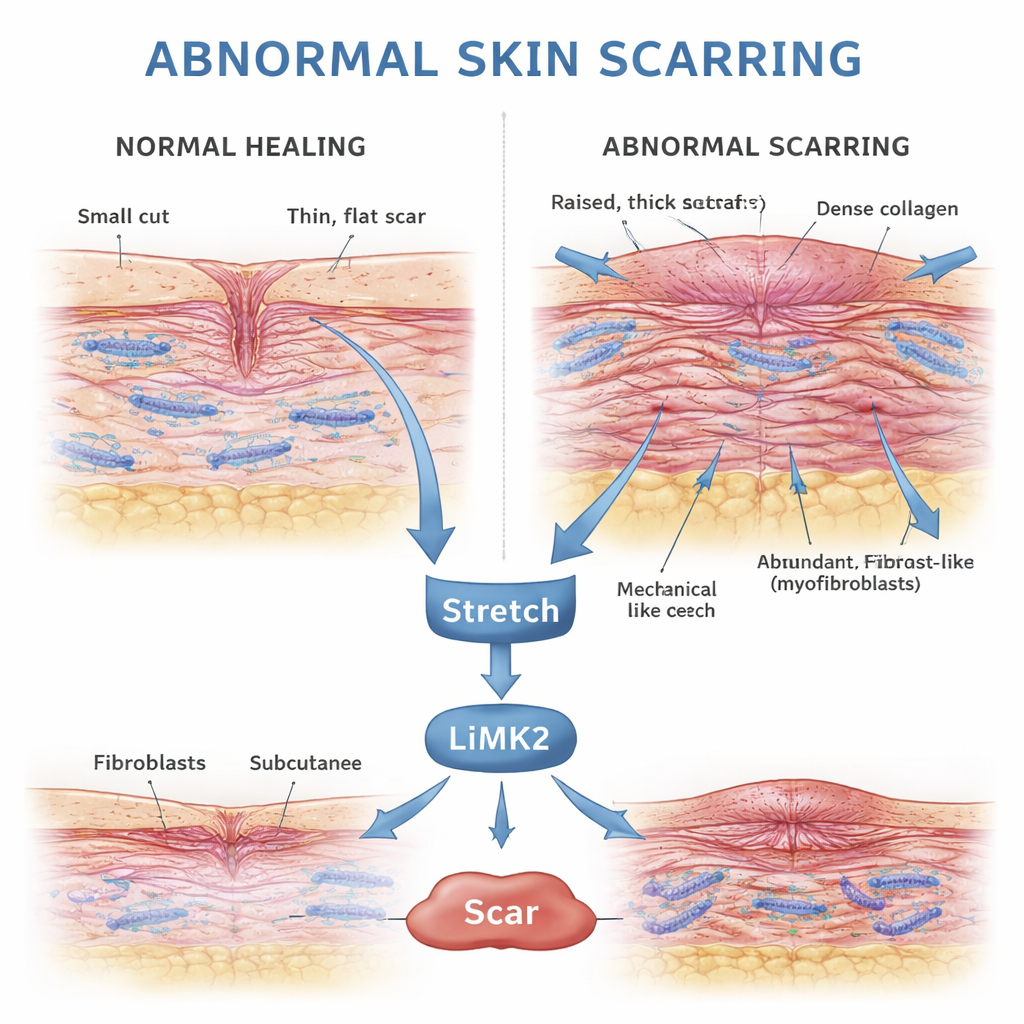
Come la pelle guarisce normalmente dopo un danno
Quando la pelle è danneggiata, l’organismo avvia un programma di riparazione accuratamente temporizzato. I fibroblasti — cellule “operarie” dello strato profondo della pelle — migrano nella ferita, si moltiplicano e depositano collagene, lo scheletro proteico del nuovo tessuto. Molti di questi fibroblasti si trasformano temporaneamente in una forma più robusta e contrattilе detta miofibroblasti, che aiuta ad avvicinare i margini della ferita. Una volta che la superficie si è chiusa e il nuovo tessuto si è stabilizzato, questi miofibroblasti dovrebbero andare incontro a morte programmata tramite un processo controllato noto come apoptosi, lasciando dietro di sé una cicatrice modesta e flessibile.
Quando le forze quotidiane peggiorano le cicatrici
Le cicatrici anomale spesso compaiono dove la pelle è costantemente sottoposta a trazione — sul petto, sulle spalle o nella parte inferiore dell’addome. Questa osservazione ha portato i ricercatori a sospettare che le forze meccaniche, come lo stiramento e la tensione su una ferita in via di guarigione, possano spingere i fibroblasti a restare attivi troppo a lungo. Studi precedenti hanno mostrato che lo stiramento di queste cellule in laboratorio aumenta una proteina chiamata α-SMA, marcatore dei miofibroblasti, e attiva geni che aiutano le cellule a resistere all’apoptosi. Il nuovo studio si concentra su LIMK2, una componente chiave di una via di segnalazione meccanica all’interno delle cellule che collega lo stiramento fisico ai cambiamenti dello scheletro interno formato dai filamenti di actina.
Un interruttore chiave per le cellule che formano cicatrici
Per testare il ruolo di LIMK2, i ricercatori hanno utilizzato fibroblasti dermici umani provenienti da pelle normale e da tessuto cheloide. Hanno introdotto in alcune cellule una versione inattiva di LIMK2, lasciando altre inalterate o dotandole di una versione sempre attiva come controlli. Quando le cellule sono state stirate meccanicamente, i fibroblasti normali hanno risposto come previsto: rapido aumento della cofilina fosforilata e fibre di actina più robuste, incremento di α-SMA, maggiore produzione di collagene e livelli più elevati di Bcl-2, una proteina che protegge dalla morte cellulare, insieme a livelli ridotti della proteina pro-apoptotica BAX. In netto contrasto, i fibroblasti con LIMK2 inattivo sono cambiati molto poco sotto stiramento. Non hanno aumentato α-SMA, non hanno incrementato Bcl-2 né ridotto BAX e hanno mostrato meno collagene. Queste cellule hanno anche contratto i gel di collagene meno intensamente e si sono mosse più lentamente in un saggio che mimava una ferita, suggerendo una minore forza di trazione e ridotta capacità di invadere i tessuti circostanti.
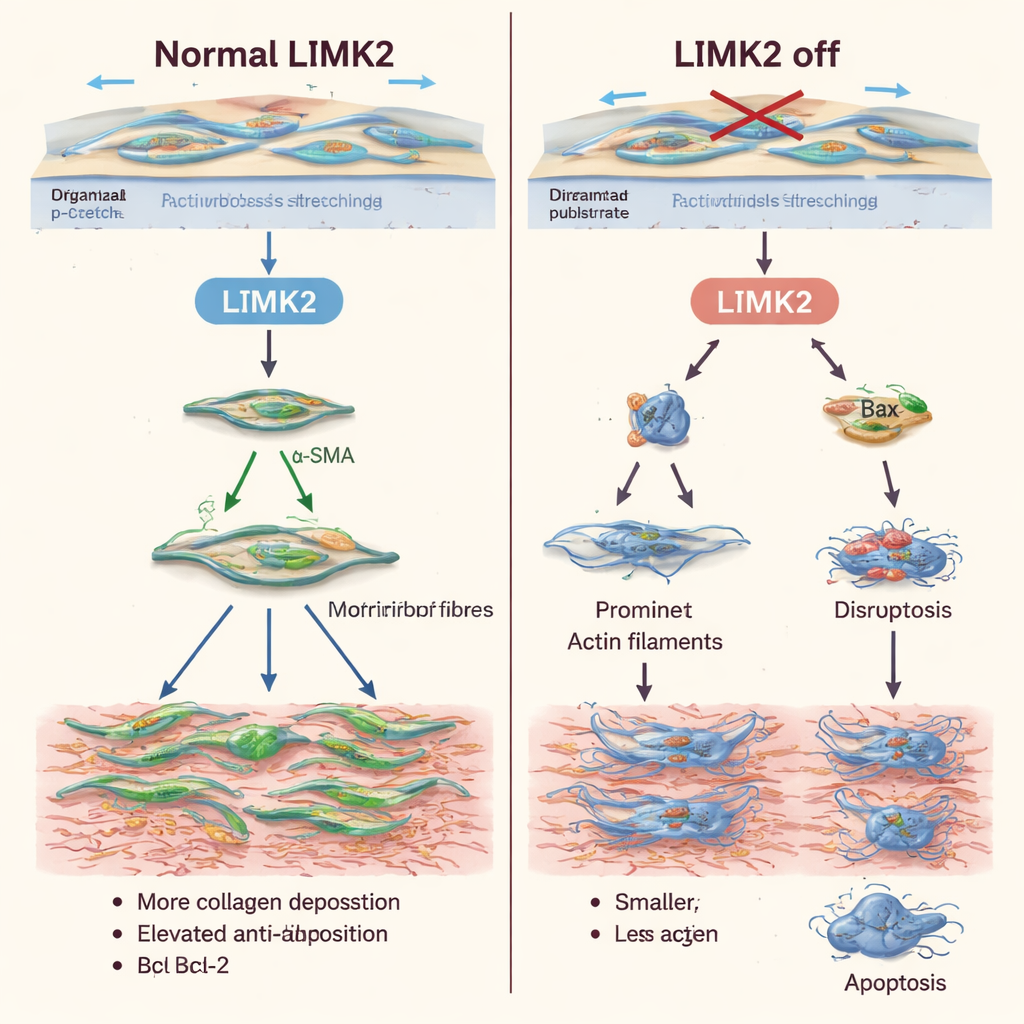
Rendere più facile eliminare le cellule cicatriziali ostinate
Oltre a modificare il comportamento dei fibroblasti sotto stiramento, l’inattivazione di LIMK2 li ha resi più inclini alla morte e meno propensi a proliferare. Le cellule con LIMK2 inattivo hanno mostrato livelli basali più alti di apoptosi, e lo stiramento meccanico — normalmente un segnale di sopravvivenza — non le ha più protette. Citometria a flusso e colorazioni fluorescenti hanno confermato che più cellule erano in fasi precoci o tardive della morte programmata. Allo stesso tempo, il conteggio delle cellule e i test di marcatura del DNA hanno rivelato che queste cellule si dividevano molto meno del normale. Pattern simili sono apparsi quando il gruppo ha utilizzato latrunculina A, un farmaco che altera i filamenti di actina, a sostegno dell’idea che LIMK2 agisca principalmente controllando l’impalcatura interna della cellula.
Cosa potrebbe significare per i futuri trattamenti delle cicatrici
I risultati suggeriscono che LIMK2 si trova a un crocevia in cui forze meccaniche, sopravvivenza cellulare e attività di costruzione della cicatrice si intersecano. Quando LIMK2 è attivo, lo stiramento spinge i fibroblasti verso uno stato di miofibroblasto robusto e persistente: si contraggono con forza, resistono alla morte e producono collagene in eccesso, tutti fattori che favoriscono cicatrici spesse e rilevate. Spegnere LIMK2 inverte gran parte di questo — i fibroblasti diventano meno contrattili, meno mobili, meno prolifici e più inclini all’apoptosi. Per i pazienti, questo indica un futuro in cui creme, iniezioni o medicazioni che bloccano in modo mirato LIMK2 o i cambiamenti dell’actina a valle potrebbero aiutare le ferite ad alto rischio a guarire con cicatrici più piatte e confortevoli.
Citazione: Ishii, M., Kuroda, K., Otani, N. et al. LIMK2 inactivation suppresses mechanical stimulation-induced dermal fibroblast differentiation and resistance to apoptosis. Sci Rep 16, 7453 (2026). https://doi.org/10.1038/s41598-026-37610-y
Parole chiave: cicatrici cheloidi, guarigione delle ferite, fibroblasti, tensione meccanica, apoptosi