Clear Sky Science · it
Cambiamenti nell'attività di EGFR dopo l'editing CRISPR/Cas9 del dominio di legame di EGF
Perché riprogettare un segnale del cancro è importante
Il carcinoma cervicale dipende spesso da un potente interruttore di crescita chiamato recettore del fattore di crescita epidermico (EGFR). Molti tumori presentano enormi quantità di questi recettori, tuttavia i farmaci mirati a spegnerli hanno aiutato solo una parte dei pazienti. Questo studio ha posto una domanda fondamentale con grandi implicazioni terapeutiche: cosa succede se si elimina la capacità di EGFR di catturare il suo segnale di crescita preferito, il fattore di crescita epidermico (EGF), senza rimuovere il recettore stesso?
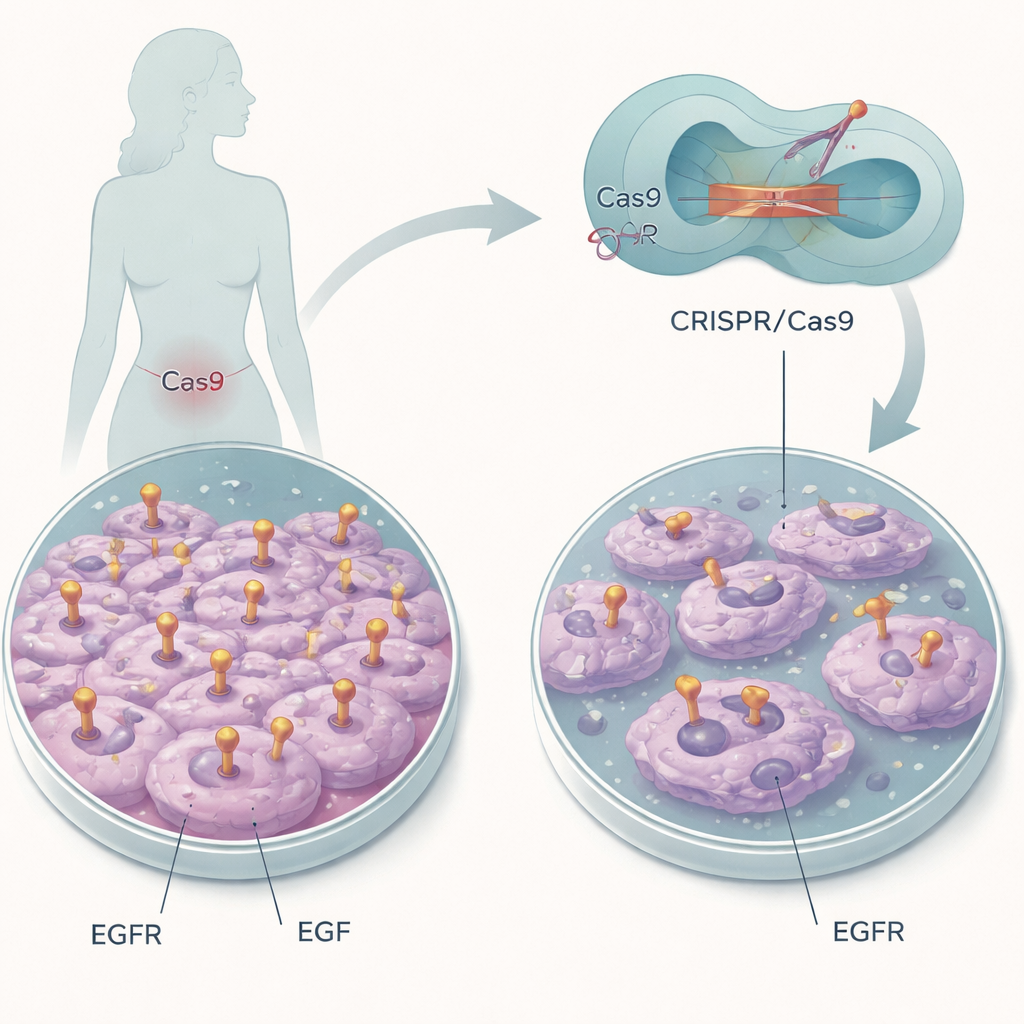
Spegnere un “interruttore” molecolare
I ricercatori si sono concentrati su una linea cellulare di carcinoma cervicale che contiene grandi quantità di EGFR altrimenti normale. Invece di distruggere il gene, hanno usato l'editing genomico CRISPR/Cas9 come un bisturi molecolare per modificare solo pochi amminoacidi nella tasca di legame di EGF di EGFR. Due posizioni in particolare, chiamate L14 e Y45, aiutano l'EGF ad ancorarsi al recettore. Sostituendo questi mattoni con altri diversi, il gruppo mirava a mantenere EGFR presente ma cieco all'EGF, permettendo di isolare il ruolo di questa singola interazione nel comportamento delle cellule tumorali.
Costruire linee cellulari tumorali su misura
In un primo passo, il team ha testato queste mutazioni in cellule usando plasmidi che producono transitoriamente EGFR normale o alterato. L'EGF marcato con fluorescenza ha rivelato che tutte le forme mutanti legavano molto meno ligando rispetto al recettore normale, specialmente quando L14 e Y45 erano modificati insieme. I ricercatori hanno poi introdotto queste modifiche direttamente nel genoma delle cellule tumorali con CRISPR/Cas9, generando diverse nuove cloni cellulari. Alcuni portavano una singola mutazione, altri la doppia mutazione su una copia di EGFR e cambiamenti inattivanti sull'altra. La modellazione al computer delle forme proteiche risultanti ha mostrato che queste alterazioni deformavano il sito di legame abbastanza da indebolire o abolire l'ancoraggio di EGF, coerentemente con i test di legame.
Quando il recettore si sposta ma le cellule sopravvivono
Immagini dettagliate hanno rivelato che i recettori editati si comportavano in modo molto diverso all'interno della cellula. Nelle cellule tumorali non editate, EGFR si trova sulla superficie cellulare, cattura l'EGF e poi si muove verso l'interno mentre viene chimicamente attivato tramite fosforilazione. Nei cloni portatori della doppia mutazione, il legame con EGF è praticamente scomparso ed EGFR non è più visibile sulla membrana; invece, la piccola quantità di recettore rimanente si accumulava all'interno della cellula. Anche una singola modifica Y45 ha ridotto sostanzialmente il legame e abbassato i livelli complessivi di EGFR. Eppure, nonostante questa interruzione della via EGF–EGFR descritta sui manuali, le cellule tumorali sono rimaste vitali e hanno continuato a proliferare in coltura con solo cambiamenti modesti nei loro schemi del ciclo cellulare.
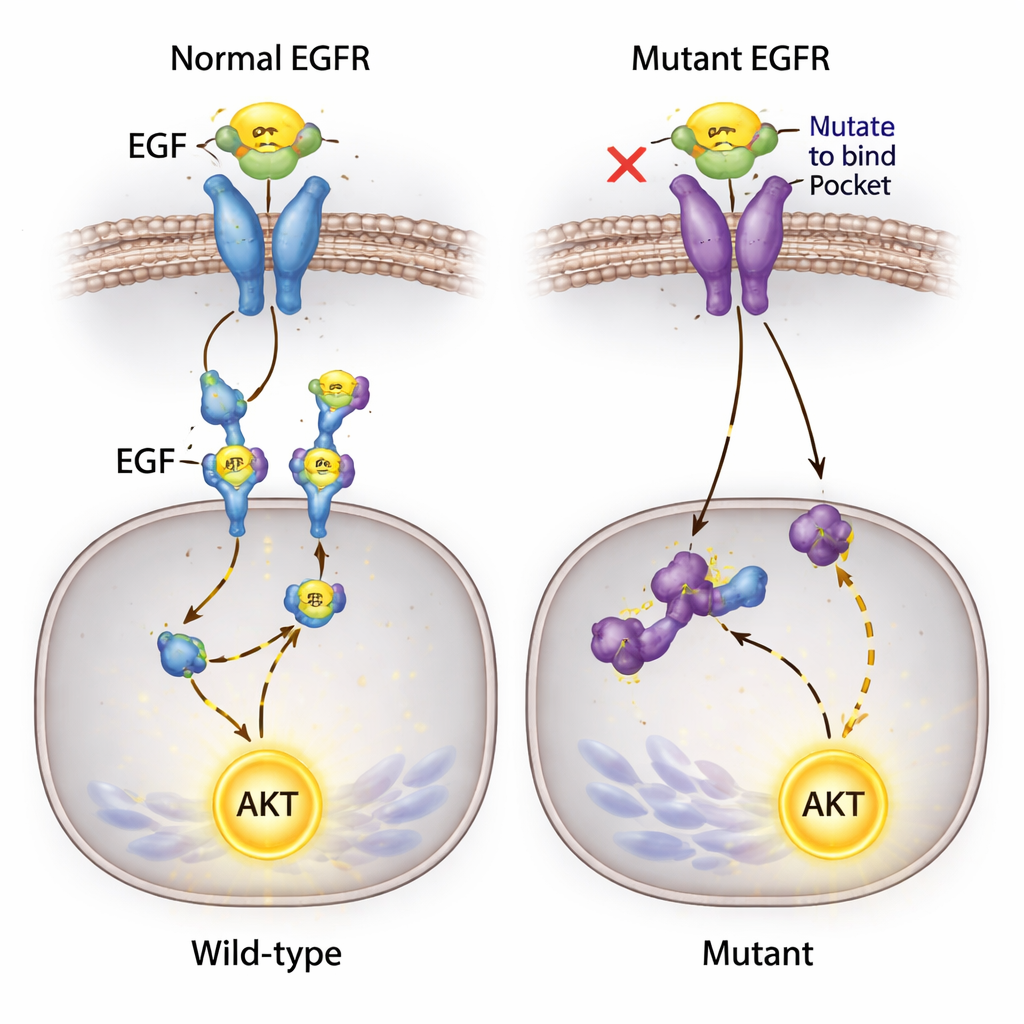
Un segnale inaspettato che non si arresta
Una delle scoperte più sorprendenti ha riguardato AKT, una proteina chiave che promuove la sopravvivenza cellulare e che di solito viene attivata a valle di EGFR. I ricercatori si aspettavano che bloccare il legame EGF–EGFR spegnesse questa via. Invece, quando hanno aggiunto EGF al terreno di coltura, AKT è diventata fortemente attivata in tutte le linee cellulari—incluse quelle in cui l'EGF non poteva più legarsi a EGFR e dove la fosforilazione del recettore era indistinguibile. Poiché queste cellule portano una nota mutazione in un altro gene di segnalazione, PIK3CA, il team sospetta che rotte alternative possano consentire all'EGF di alimentare l'attivazione di AKT, possibilmente attraverso altri recettori di superficie o mutazioni preesistenti, aggirando l'EGFR editato.
Cambiamenti genetici nascosti e terapie future
Per assicurarsi che CRISPR non stesse causando modifiche involontarie diffuse, gli scienziati hanno sequenziato l'intero genoma delle nuove linee cellulari. Hanno confermato che le mutazioni desiderate in EGFR erano presenti e non hanno trovato evidenze di tagli nei siti off‑target previsti per le guide CRISPR. Tuttavia, hanno rilevato molte mutazioni spontanee sparse nel genoma, alcune delle quali potrebbero influenzare il comportamento cellulare. Questo sottolinea che anche quando CRISPR colpisce l'indirizzo previsto, il DNA naturalmente instabile delle cellule tumorali può complicare l'interpretazione dei risultati sperimentali e la progettazione di terapie genetiche precise.
Cosa significa per i pazienti
Per un lettore non specialista, il messaggio principale è che semplicemente bloccare la stretta di mano tra EGF ed EGFR—even in modo molto preciso a livello atomico—non arresta automaticamente i comandi di “crescita e sopravvivenza” delle cellule tumorali. Lo studio mostra che le cellule tumorali possono riorientare segnali chiave come l'attivazione di AKT intorno a un recettore bloccato, e che l'editing CRISPR va valutato con attenzione in genomi così instabili. Queste linee cellulari ingegnerizzate forniscono ora un potente modello di laboratorio per cercare le vie di riserva che sostengono i tumori dipendenti da EGFR, informazioni che potrebbero alla fine portare a terapie combinate che prendano di mira sia EGFR sia i suoi complici nascosti.
Citazione: Popović, J., Hahut, A., Torres, G.E. et al. Changes in EGFR activity following CRISPR/Cas9-editing of the EGF binding domain. Sci Rep 16, 6797 (2026). https://doi.org/10.1038/s41598-026-37579-8
Parole chiave: EGFR, cancro cervicale, CRISPR, segnalazione EGF, via AKT