Clear Sky Science · it
Coniugazione del DNA su superfici plastiche funzionalizzate per il sequenziamento iterativo e sequenziale a singola molecola
Conservare i dati di domani in minuscoli filamenti
Immaginate di eseguire il backup delle vostre foto, dei libri o dei registri scientifici in una forma che potrebbe durare per secoli e stare in un granello più piccolo di un chicco di sabbia. Il DNA — la stessa molecola che porta i nostri geni — emerge come un candidato potente per un’archiviazione a densità ultra-elevata e di lunga durata. Questo articolo esplora un nuovo modo per “parcheggiare” i dati su DNA in modo sicuro all’interno di comuni provette di plastica da laboratorio, per poi leggerli più e più volte senza distruggere le molecole originali.
Un nuovo tipo di «chiavetta» per i dati
I dischi rigidi e le memorie flash odierni si usurano, e immagazzinano molto meno informazioni per grammo rispetto a quanto teoricamente può fare il DNA. I ricercatori hanno già dimostrato come tradurre file digitali in sequenze di “lettere” del DNA. Ma ogni volta che quei filamenti vengono copiati o sequenziati, una parte del materiale originale viene consumata, come inchiostro che si sfuma dopo troppe fotocopie. In questo studio, gli autori hanno trasformato la semplice provetta PCR — già comune nei laboratori di biologia — in un dispositivo fisico di archiviazione riutilizzabile. Hanno attaccato chimicamente filamenti di DNA che trasportavano dati codificati alla superficie interna della provetta, in modo che il DNA restasse fissato mentre venivano ripetutamente generate e lette copie. 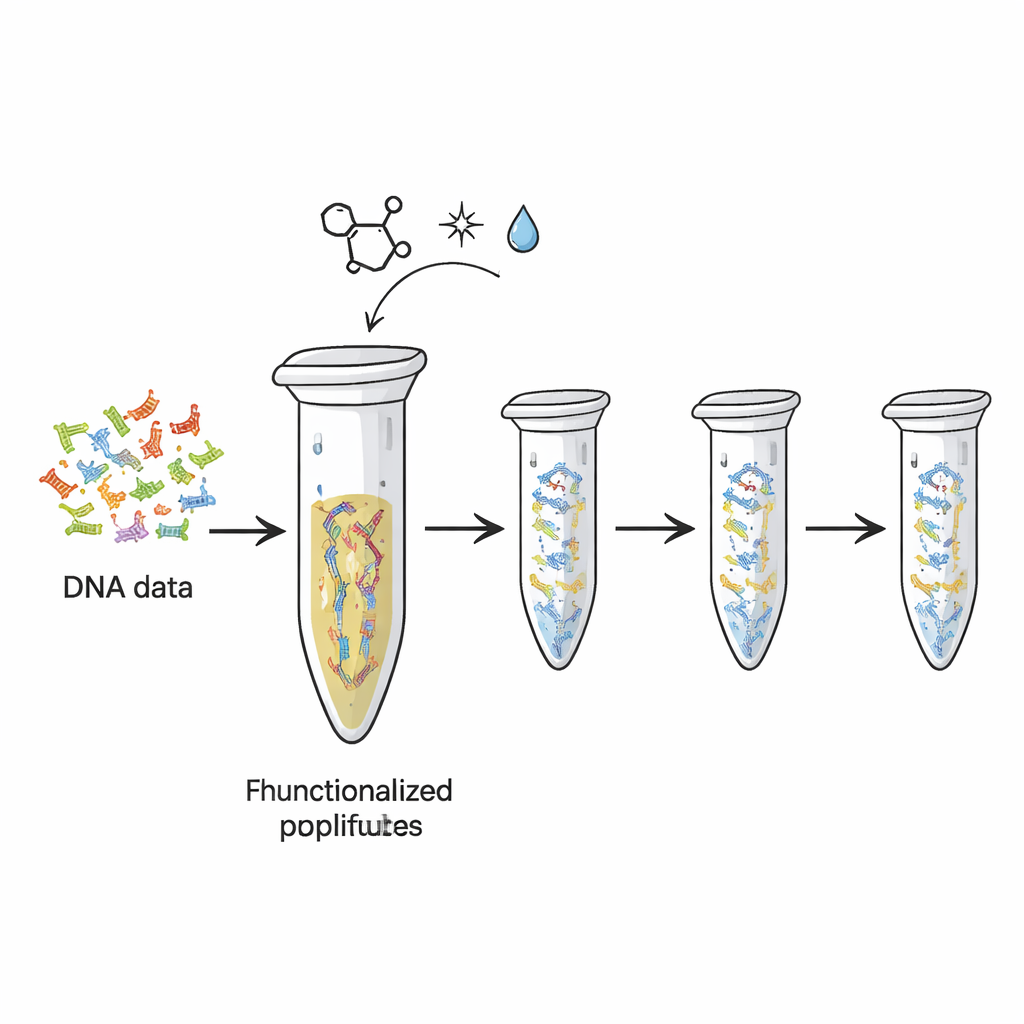
Fissare il DNA sulla plastica con la chimica click
Il gruppo si è affidato a un tipo di ‘chimica click’ altamente specifica — una serie di reazioni apprezzate per essere veloci, affidabili e delicate. Per prima cosa hanno aggiunto code chimiche speciali alle estremità dei filamenti di DNA che rappresentavano diversi “file” di dati. Queste code, basate su una molecola chiamata TCO, sono progettate per legarsi a gruppi corrispondenti (MTz) che erano stati innestati sulla superficie plastica della provetta. Quando le due componenti si incontrano, formano un legame covalente stabile, fissando di fatto il DNA alla plastica. I test con un frammento di DNA di controllo hanno mostrato che dopo l’incubazione quasi tutto il DNA era scomparso dalla soluzione, indicando che era stato immobilizzato sulla parete della provetta. La piattaforma poteva contenere dell’ordine di centinaia di femtomoli di DNA, suggerendo una capacità sufficiente per set di dati pratici.
Recuperare «file» digitali su richiesta
Per verificare se questo DNA legato alla superficie si comportasse ancora come un archivio utilizzabile, i ricercatori hanno codificato testo e altri dati in un pool di circa 15.000 brevi filamenti di DNA, raggruppati in 18 “gruppi di file”. Ogni gruppo poteva essere copiato selettivamente usando la propria coppia di primer — brevi sequenze iniziali che indirizzano il macchinario di copia verso i bersagli corretti. Il team ha eseguito ripetutamente reazioni PCR standard nella stessa provetta, scegliendo ogni volta un diverso gruppo di file da amplificare. Dopo ogni ciclo hanno rimosso il DNA copiato, pulito la provetta con enzimi che digeriscono i prodotti residui in soluzione e sono passati al file successivo. Il sequenziamento con nanopore del materiale copiato ha mostrato che la maggior parte dei gruppi di file è stata recuperata con elevata accuratezza, e la contaminazione incrociata da corsi precedenti è rimasta estremamente bassa, tipicamente intorno all’1% o meno.
Verso un metodo di lettura più delicato
C’era però un problema: ripetendo la PCR sulla stessa provetta fino a 18 volte, la quantità di DNA recuperata diminuiva progressivamente. La PCR si basa su rapidi cicli di riscaldamento e raffreddamento, e gli autori hanno dedotto che le alte temperature ripetute stavano danneggiando il DNA immobilizzato o il suo legame con la plastica, anche se i test di controllo suggerivano che il DNA non si stava semplicemente lavando via in soluzione. Per risolvere il problema hanno utilizzato la ricombinase polymerase amplification (RPA), un metodo più recente che funziona a una singola e relativamente bassa temperatura, vicina a quella corporea. Usando la RPA su provette appena rivestite di DNA, hanno nuovamente interrogato tutti e 18 i gruppi di file in sequenza. Questa volta le rese sono state elevate — circa 60 ng/µL — e non hanno mostrato la stessa tendenza al calo. Il profilo di quali filamenti venivano favoriti o svantaggiati durante la copia corrispondeva anche strettamente a quanto osservato quando il DNA era libero in soluzione. 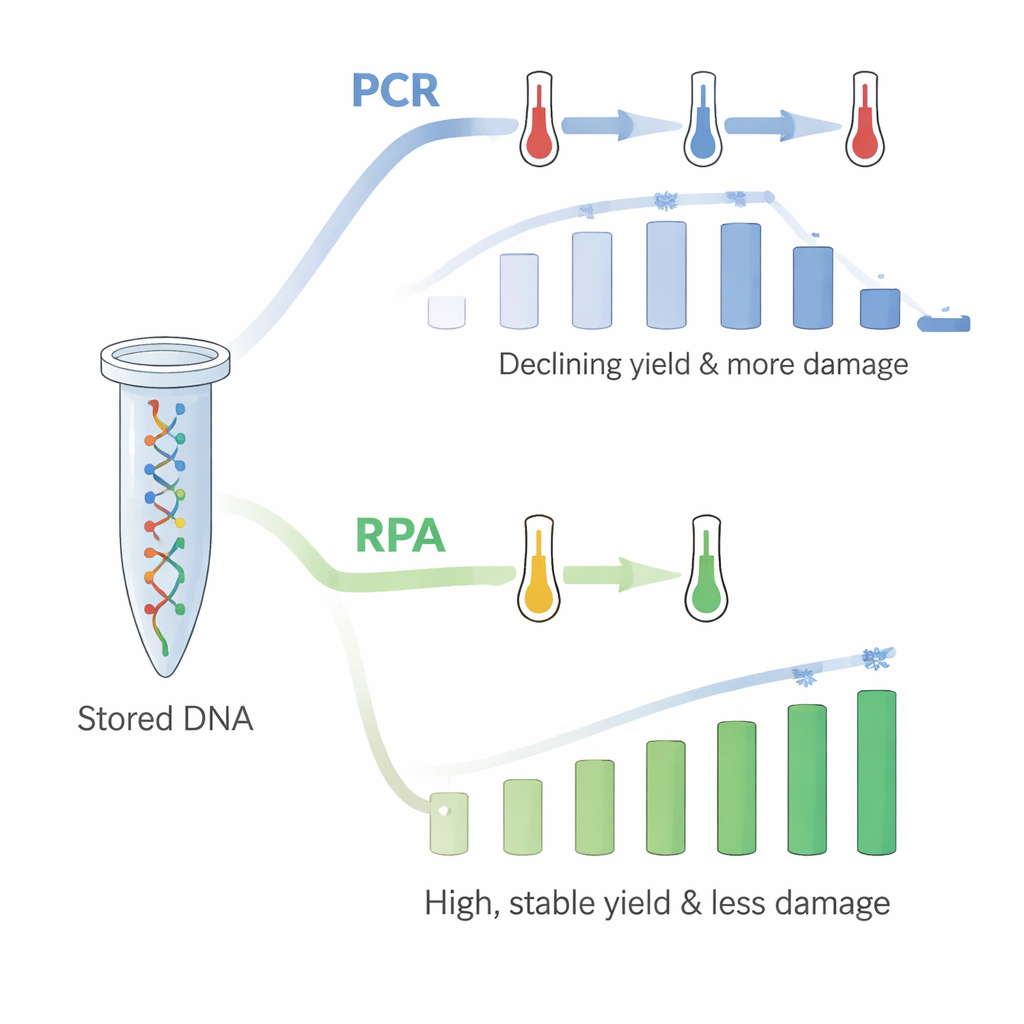
Verso una memoria su DNA portatile e duratura
Combinando la chimica click robusta con metodi di copiatura a bassa temperatura, questo lavoro indica una via pratica per trasformare semplici provette di plastica in cartucce di dati su DNA riutilizzabili. Il DNA resta fisicamente bloccato alla provetta, dove può essere interrogato ripetutamente per file specifici senza consumare le molecole originali, specialmente usando il metodo più delicato RPA. Per i non specialisti, il messaggio chiave è che il DNA non è solo il codice della vita — può anche funzionare come un mezzo di memorizzazione digitale compatto e durevole. Metodi come questo ci avvicinano a un futuro in cui i backup a lungo termine potrebbero risiedere non su dischi in rotazione, ma in molecole ingegnerizzate che riposano silenziosamente su uno scaffale di laboratorio.
Citazione: Roy, S., Ji, H.P. & Lau, B.T. DNA conjugation on functionalized plastic surfaces for sequential, iterative single molecule sequencing. Sci Rep 16, 6467 (2026). https://doi.org/10.1038/s41598-026-37575-y
Parole chiave: archiviazione dati su DNA, chimica click, coniugazione su superfici plastiche, amplificazione tramite ricombinasi e polimerasi, sequenziamento nanopore