Clear Sky Science · it
L’amplificazione del numero di copie guida la sovraespressione di IFI30 e l’attivazione immunitaria coordinata, identificando un nuovo bersaglio diagnostico e terapeutico nell’adenocarcinoma gastrico
Perché una proteina dello stomaco conta
Il cancro gastrico è uno dei tumori più letali al mondo, in gran parte perché spesso viene scoperto in fase avanzata e può essere difficile da trattare. Questo studio si concentra su una proteina poco conosciuta chiamata IFI30, presente nelle cellule che aiutano il sistema immunitario a riconoscere le minacce. Tracciando come IFI30 venga alterata nei tumori gastrici e come influenzi le difese dell’organismo, i ricercatori suggeriscono che potrebbe diventare uno strumento potente per una diagnosi più precoce e per la scelta di terapie personalizzate più efficaci.
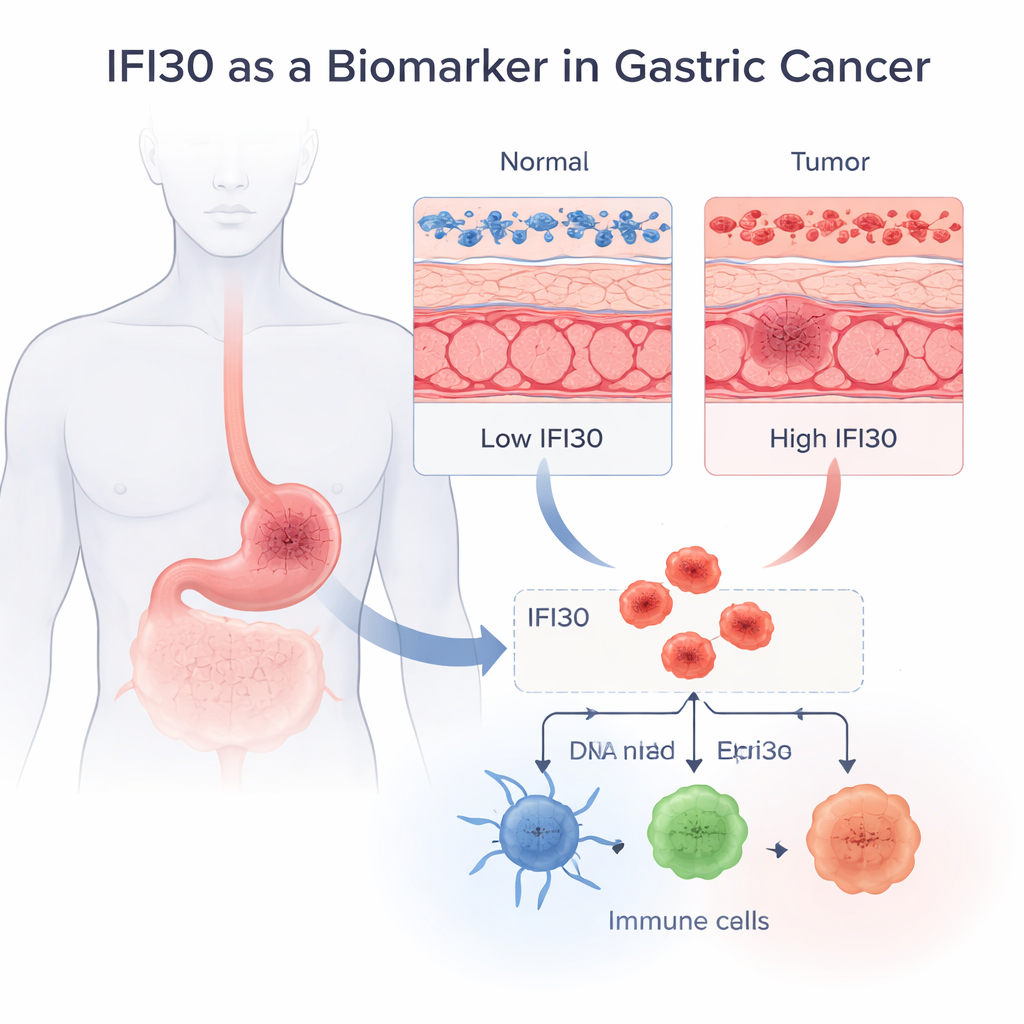
Un segnale nascosto nei tumori gastrici
Il team ha iniziato ponendosi una domanda fondamentale: IFI30 è presente a livelli diversi nei tessuti gastrici sani rispetto a quelli tumorali? Utilizzando grandi banche dati pubbliche che aggregano l’attività genica di migliaia di campioni, hanno trovato che IFI30 è costantemente molto più elevato nell’adenocarcinoma gastrico — il tipo più comune di cancro dello stomaco — rispetto alla mucosa gastrica normale. Questo risultato è stato confermato in più gruppi indipendenti di pazienti e sia a livello di RNA sia di proteina. Quando gli autori hanno valutato quanto bene IFI30 da solo potesse distinguere tessuto tumorale da tessuto sano, la performance è stata notevole: un’accuratezza diagnostica (AUC) di 0,92, considerata eccellente per un singolo marcatore. Immagini al microscopio hanno inoltre collocato IFI30 nel sistema di riciclo intracellulare, dove gli antigeni vengono processati per il riconoscimento immunitario.
Modifiche del DNA che aumentano IFI30
Successivamente, i ricercatori hanno indagato perché IFI30 sia così elevato in questi tumori. Analizzando i genomi tumorali provenienti da The Cancer Genome Atlas, hanno scoperto che copie extra del gene IFI30 — note come amplificazioni del numero di copie — rappresentano il principale motore della sua sovraespressione. I tumori con amplificazione di IFI30 tendevano a mostrare maggiore instabilità genomica complessiva e spesso portavano mutazioni note del cancro come TP53 e PIK3CA. Con l’aumentare del numero di copie di IFI30, saliva anche il livello di RNA corrispondente, suggerendo un collegamento diretto tra le alterazioni strutturali del DNA e la maggiore produzione di questa proteina. Ciò dipinge IFI30 non come un semplice spettatore, ma come parte di un quadro più ampio di biologia tumorale aggressiva.
Crosstalk immunitario attorno al tumore
Poiché IFI30 è coinvolto nel processamento del materiale che le cellule immunitarie presentano come “manifesti” ai linfociti T, il team ha esplorato dove esattamente si trova nel microambiente tumorale. Il sequenziamento single-cell, che legge i geni a livello di singole cellule, ha mostrato che IFI30 è particolarmente arricchito nelle cellule dendritiche, nei macrofagi e nei linfociti T CD8 — attori chiave nell’avvio e nel mantenimento dell’immunità anti-tumorale. Analisi di rete hanno rivelato una fitta comunicazione tra cellule immunitarie ricche di IFI30 e le cellule tumorali e di supporto circostanti. I tumori con alto IFI30 mostravano una forte attivazione di vie legate alla presentazione degli antigeni, a segnali infiammatori e a molecole di comunicazione che attraggono e organizzano le cellule immunitarie. Allo stesso tempo, questi tumori presentavano caratteristiche di invasione e stress, come accelerazione del ciclo cellulare, rimodellamento tissutale e adattamento a bassi livelli di ossigeno, evidenziando il ruolo di IFI30 all’incrocio tra attacco e difesa nel cancro.
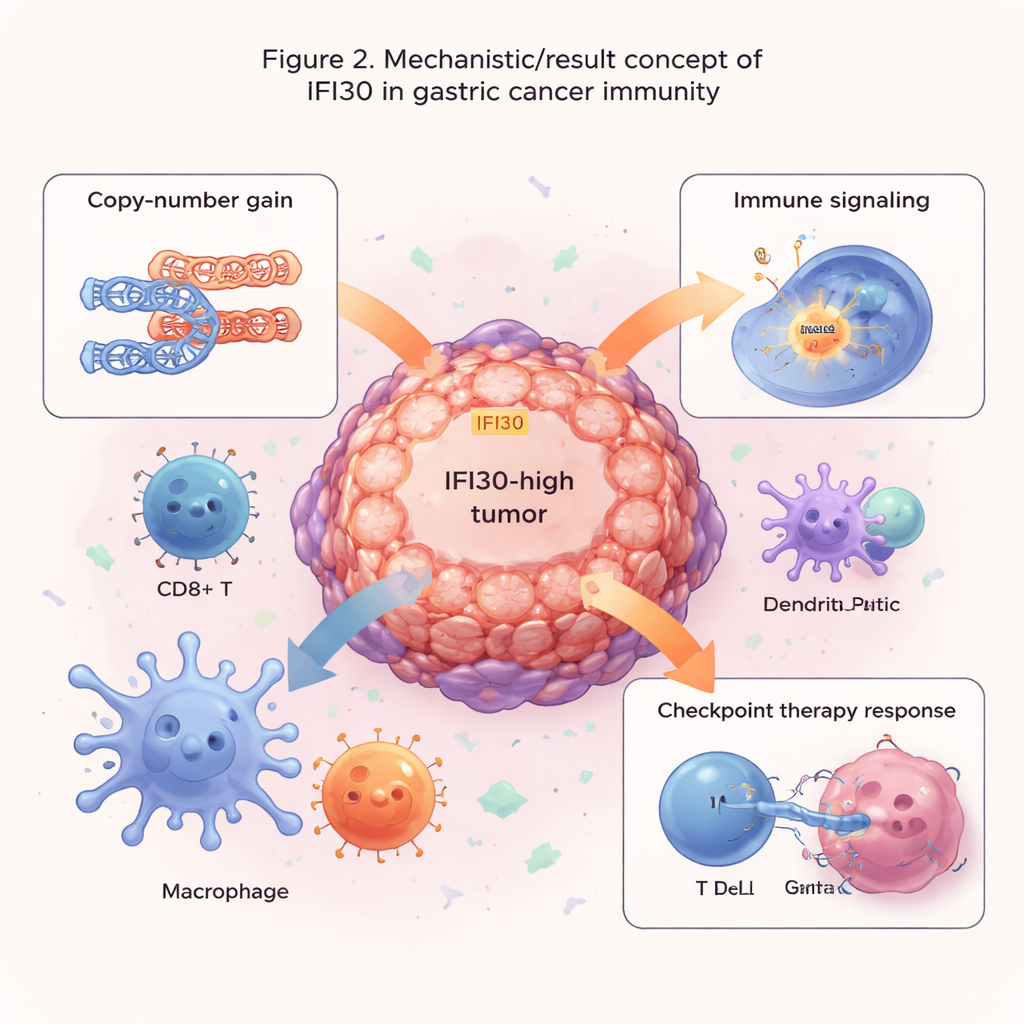
Indizi per la scelta dei farmaci e l’immunoterapia
Gli autori hanno poi verificato se IFI30 potesse aiutare a prevedere la risposta dei tumori ai trattamenti. Abbinando i livelli di IFI30 a grandi dataset di risposta ai farmaci, hanno osservato che i tumori con IFI30 elevato tendono a resistere ad alcuni medicinali che mirano alla divisione cellulare o a una via di crescita comune (MAPK), ma sembrano più sensibili ai farmaci che bloccano la segnalazione EGFR e PI3K/AKT. È rilevante che i livelli di IFI30 fossero strettamente correlati con PD-L1, un importante freno sui linfociti T che è bersaglio degli inibitori del checkpoint attuali. In diversi studi di immunoterapia, i pazienti i cui tumori esprimevano livelli più alti di IFI30 erano più propensi a rispondere al blocco del checkpoint rispetto a quelli con livelli bassi. Un punteggio basato su IFI30 ha superato misure già consolidate come il burden mutazionale tumorale e PD-L1 da solo, ed è risultato particolarmente arricchito nei tumori con alta instabilità dei microsatelliti, un sottogruppo già noto per rispondere meglio all’immunoterapia.
Dal banco di laboratorio a un possibile nuovo bersaglio
Per verificare se IFI30 sia solo un marcatore o contribuisca anche alla crescita tumorale, il gruppo ha ridotto i suoi livelli in linee cellulari di cancro gastrico usando strumenti genetici. Quando IFI30 è stato silenziato, le cellule tumorali crescevano più lentamente, indicando un ruolo diretto nel sostenere la proliferazione tumorale. Nel complesso, i dati suggeriscono che IFI30 è sia un indicatore dell’attività immunitaria sia un contributore al comportamento maligno. Per i pazienti, questo significa che una semplice misura di IFI30 potrebbe un giorno aiutare i medici a rilevare il cancro gastrico con maggiore affidabilità, prevedere chi potrebbe beneficiare di determinati farmaci mirati o immunoterapie e forse guidare nuovi trattamenti che bloccano direttamente o indirettamente le azioni tumor-promotrici di IFI30.
Citazione: Liu, Q., Yuan, W., Zhaowang, R. et al. Copy-number amplification drives IFI30 overexpression and coordinated immune activation, identifying a novel diagnostic and therapeutic target in gastric adenocarcinoma. Sci Rep 16, 6945 (2026). https://doi.org/10.1038/s41598-026-37574-z
Parole chiave: cancro gastrico, IFI30, biomarcatore, immunità tumorale, immunoterapia