Clear Sky Science · it
Analisi computazionale degli idruri X2CaZnH6 (X = K, Rb e Cs) per lo stoccaggio di idrogeno
Idrogeno in una scatola
L’idrogeno è spesso celebrato come un combustibile pulito del futuro, ma conservarlo in modo sicuro e compatto resta un ostacolo importante. Questo studio esplora una nuova famiglia di materiali cristallini che possono ospitare l’idrogeno all’interno del loro reticolo atomico, un po’ come l’acqua in una spugna. Progettando questi composti al computer prima che qualcuno li sintetizzi in laboratorio, gli autori mostrano come potrebbero fungere da combustibili solidi per tecnologie a idrogeno di prossima generazione.
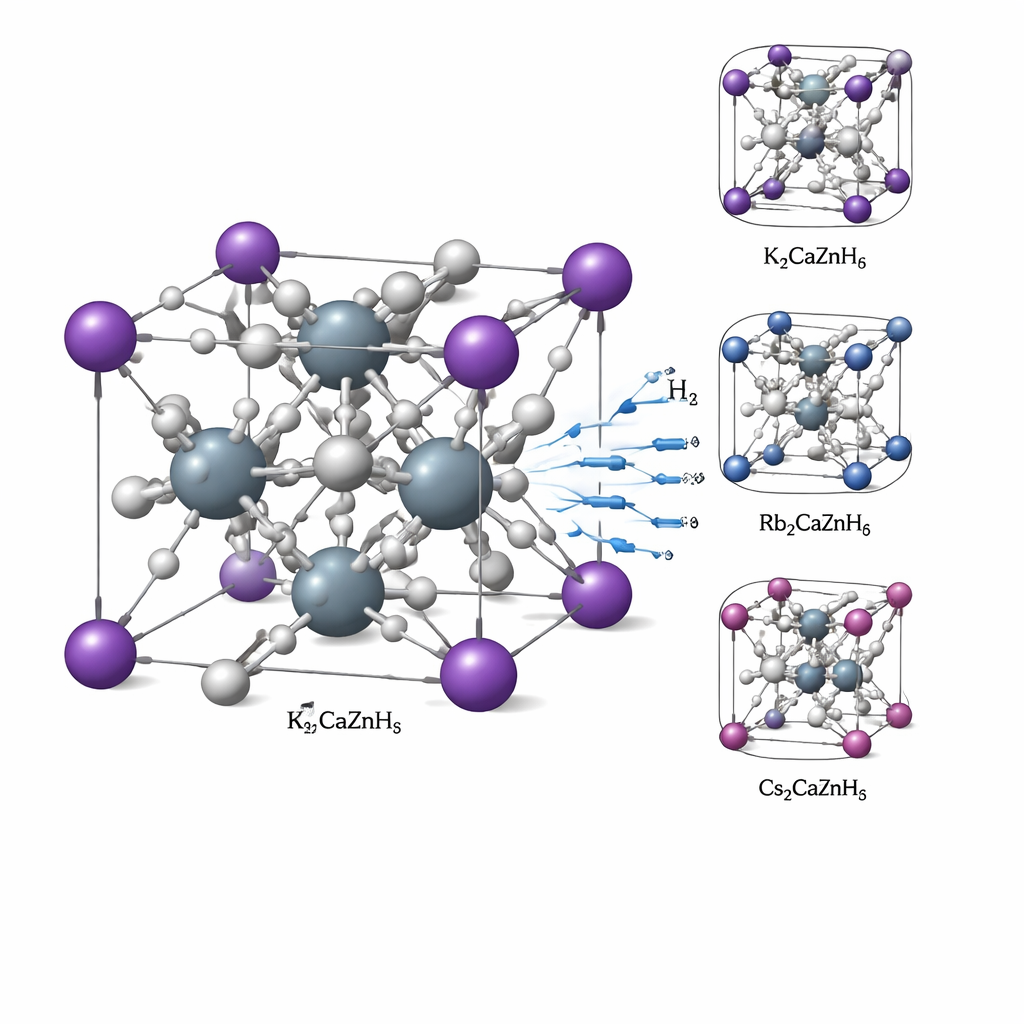
Un cristallo costruito come un reticolo 3D
I materiali esaminati sono idruri a doppia perovskite, con formula X2CaZnH6, dove X può essere potassio (K), rubidio (Rb) o cesio (Cs). Tutti e tre formano una struttura semplice a forma di cubo in cui gli atomi pesanti occupano posizioni ben definite e gli atomi di idrogeno si trovano negli spazi circostanti. Mediante calcoli quantomeccanici, gli autori confermano che questi cristalli sono strutturalmente affidabili: gli atomi si incastrano con le dimensioni appropriate, l’energia complessiva del materiale è sufficientemente bassa da favorirne la formazione spontanea e le vibrazioni atomiche non indicano instabilità nascoste. Test meccanici condotti in silico mostrano che i cristalli sono rigidi ma non eccessivamente fragili, un equilibrio che li aiuta a mantenere la forma pur consentendo piccoli riarrangiamenti durante l’assorbimento o il rilascio dell’idrogeno.
Quanta idrogeno possono contenere?
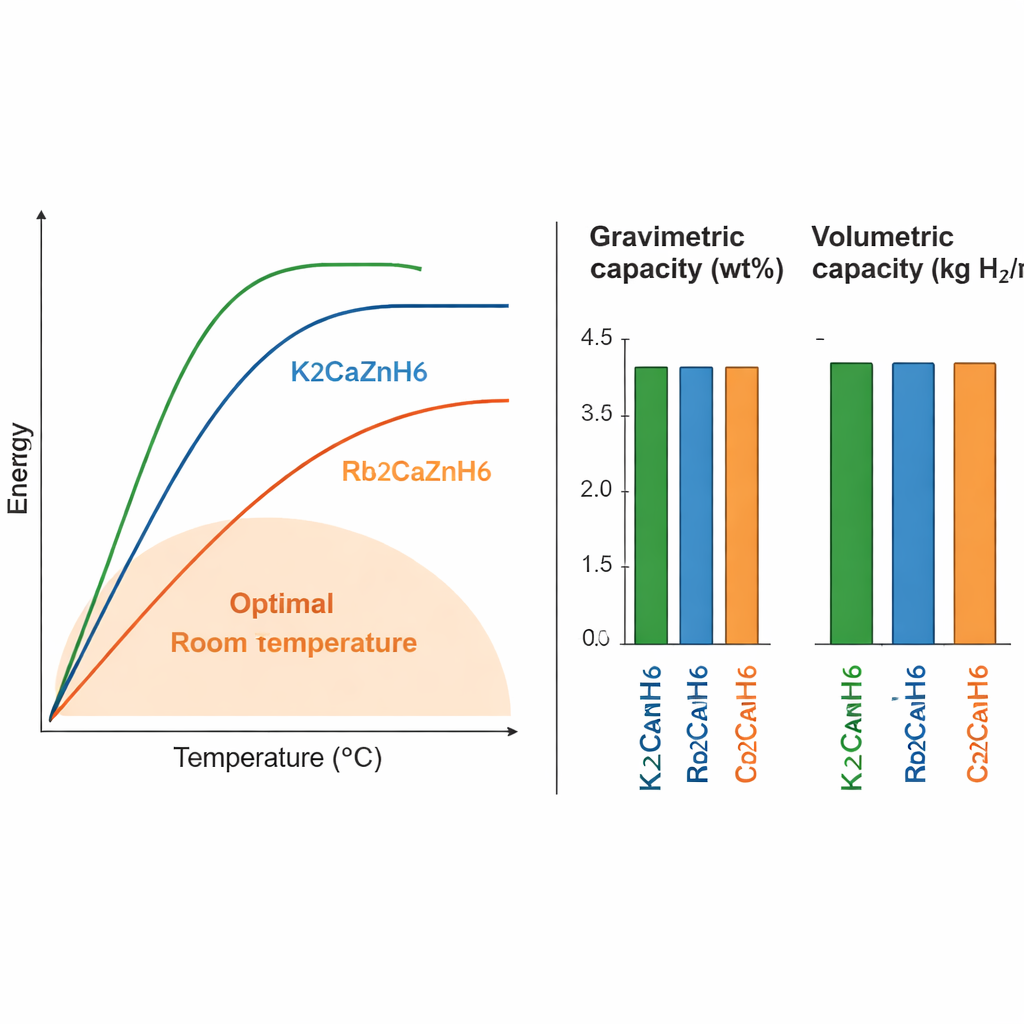
Per qualsiasi materiale di stoccaggio, due numeri chiave sono quanto idrogeno può contenere in peso (capacità gravimetrica) e in volume (capacità volumetrica), oltre alla temperatura a cui l’idrogeno può essere rilasciato. I tre composti studiati qui immagazzinano tra circa l’1,6% e il 3,2% del loro peso in idrogeno, e circa 15–18 chilogrammi di idrogeno per metro cubo di materiale. La variante a base di potassio, K2CaZnH6, contiene il massimo idrogeno ma richiede temperature più elevate (circa 658 K, o 385 °C) per rilasciarlo. La versione al cesio immagazzina leggermente meno idrogeno e richiede comunque temperature piuttosto alte. Il composto a base di rubidio, Rb2CaZnH6, si distingue: rilascia idrogeno intorno a 385 K (circa 110 °C), un intervallo molto più vicino a quanto considerato pratico per dispositivi reali, pur mantenendo una densità di stoccaggio ragionevole.
Perché contano atomi ed elettroni
Per capire il comportamento di questi materiali, gli autori analizzano come gli elettroni sono condivisi tra gli atomi e come ciò influisce sul legame chimico. In tutti e tre i composti, potassio, rubidio o cesio fungono da donatori di elettroni, mentre zinco, calcio e idrogeno attraggono elettroni. Gli atomi di idrogeno acquisiscono una carica parzialmente negativa e i loro legami con calcio e zinco sono in larga parte ionici con un certo grado di carattere covalente. Questo tipo di legame tende a trattenere l’idrogeno abbastanza saldamente da evitarne la dispersione, ma abbastanza debolmente da permetterne il rilascio mediante riscaldamento quando necessario. Importante è che gli atomi di idrogeno non formano forti legami H–H all’interno del cristallo, il che significa che l’idrogeno è immagazzinato come atomi separati anziché come molecole preformate, favorevole per un rilascio controllato.
Luce, elettricità e resistenza
Questi cristalli sono anche semiconduttori, con un modesto gap energetico tra stati elettronici occupati e vuoti. Ciò significa che possono interagire con la luce su un’ampia gamma di lunghezze d’onda, specialmente nelle regioni visibili e ultraviolette dello spettro. I calcoli mostrano forte assorbimento della luce e significativa conducibilità ottica, aprendo la possibilità che la luce possa aiutare a innescare il rilascio dell’idrogeno, una sorta di stoccaggio assistito dal solare. Allo stesso tempo, i materiali soddisfano i criteri standard di stabilità meccanica: resistono a compressione, taglio e frattura entro limiti ragionevoli, e le loro vibrazioni atomiche a temperatura ambiente restano ben comportate nei test di riscaldamento simulati al computer. Insieme, queste caratteristiche indicano un reticolo robusto in grado di sopportare ripetuti cicli di carica e scarica dell’idrogeno.
Cosa significa per i sistemi energetici futuri
In termini pratici, lo studio individua tre nuovi materiali “spugna per l’idrogeno” che sono stabili, abbastanza resistenti e capaci di immagazzinare idrogeno in un solido compatto. Sebbene il contenuto di idrogeno in peso non raggiunga ancora gli obiettivi più ambiziosi, lo stoccaggio volumetrico è promettente, e il composto a base di rubidio in particolare opera a temperature compatibili con molti sistemi pratici. Poiché il loro comportamento può essere regolato semplicemente sostituendo un elemento alcalino con un altro, questi idruri a doppia perovskite offrono una piattaforma flessibile per progettare combustibili solidi migliori a base di idrogeno e, potenzialmente, per combinare lo stoccaggio con il controllo mediante luce nelle future tecnologie per l’energia pulita.
Citazione: Al-Zoubi, N., Almahmoud, A., Almahmoud, A. et al. Computational analysis of X2CaZnH6 (X = K, Rb and Cs) hydrides for hydrogen storage. Sci Rep 16, 6889 (2026). https://doi.org/10.1038/s41598-026-37564-1
Parole chiave: stoccaggio di idrogeno, idruri metallici, doppio perovskite, energia a stato solido, combustibili puliti