Clear Sky Science · it
Un approccio con ligasi biotina divisa rivela proteine associate all’alfa‑sinucleina oligomerica durante l’aggregazione
Perché contano le proteine ammassate nel cervello
Nella malattia di Parkinson e in condizioni correlate, una proteina cerebrale normalmente utile chiamata alfa‑sinucleina può aggregarsi in depositi appiccicosi noti come corpi di Lewy. Questi depositi compaiono decenni prima dei sintomi e sono una caratteristica definitoria osservata all’autopsia, tuttavia non sappiamo ancora quali altre proteine favoriscano il passaggio dell’alfa‑sinucleina da uno stato innocuo a aggregati pericolosi. Questo studio utilizza un ingegnoso "marcatore di prossimità" molecolare per mappare quali proteine si trovano vicino all’alfa‑sinucleina mentre passa da singole molecole a piccoli ammassi, offrendo nuovi indizi su come inizia la malattia e quali vie potrebbero essere bersagliate per rallentarla o prevenirla.
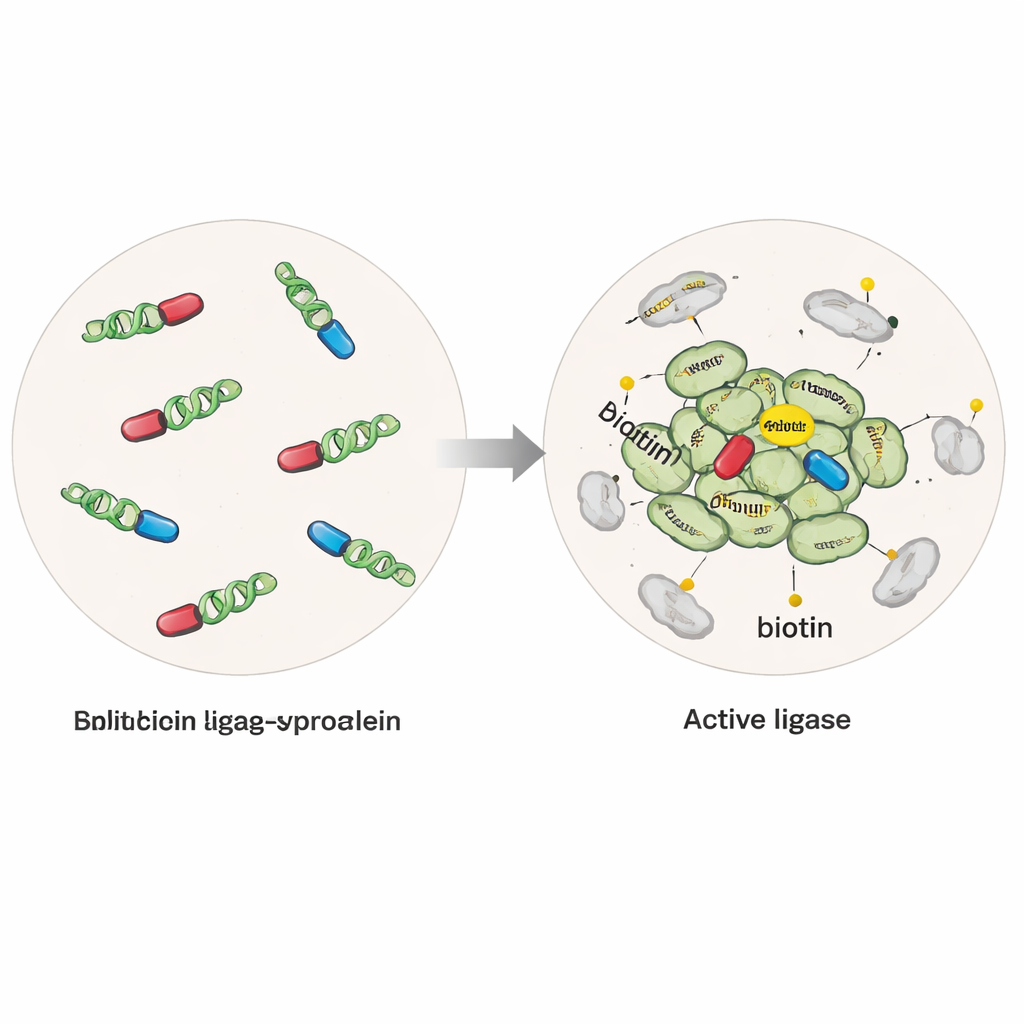
Un “marcatore” molecolare che illumina i vicini
I ricercatori hanno ingegnerizzato cellule umane per esprimere l’alfa‑sinucleina fusa a un enzima modificato in grado di attaccare un piccolo tag di biotina su qualsiasi proteina entro pochi miliardesimi di metro. In una versione l’enzima era integro e attivo ogni volta che era presente l’alfa‑sinucleina, catturando proteine vicine sia alle singole molecole sia agli ammassi. In una seconda versione più selettiva, detta "divisa", l’enzima era tagliato in due metà inattive, ciascuna attaccata a una diversa molecola di alfa‑sinucleina. Solo quando le molecole di alfa‑sinucleina si univano in multimeri od oligomeri le metà si ricongiungevano in un enzima attivo, attivando la marcatura specificamente attorno a questi aggregati precoci. Aggiungendo alle cellule fibrille di alfa‑sinucleina purificate, il gruppo poteva inoltre indurre aggregazione simile a quella patologica e confrontare stati normali e patologici.
Costruire una mappa delle proteine vicine
Dopo aver dato il tempo necessario alla marcatura, il gruppo ha isolato tutte le proteine etichettate con biotina e le ha identificate mediante spettrometria di massa, una tecnica che pesa e conta le proteine con alta precisione. In tutte le condizioni hanno trovato 1.277 proteine distinte e, dopo un filtraggio accurato, le hanno ristrette a 581 che molto probabilmente erano realmente vicine all’alfa‑sinucleina. Confrontando i sistemi con enzima integro e diviso, hanno potuto distinguere le proteine che si associano principalmente a molecole singole da quelle che preferiscono i multimeri. Hanno anche confrontato cellule con e senza fibrille aggiunte per vedere come l’ambiente proteico locale dell’alfa‑sinucleina cambi una volta che l’aggregazione è scatenata.
Percorsi cellulari chiave richiamati negli ammassi
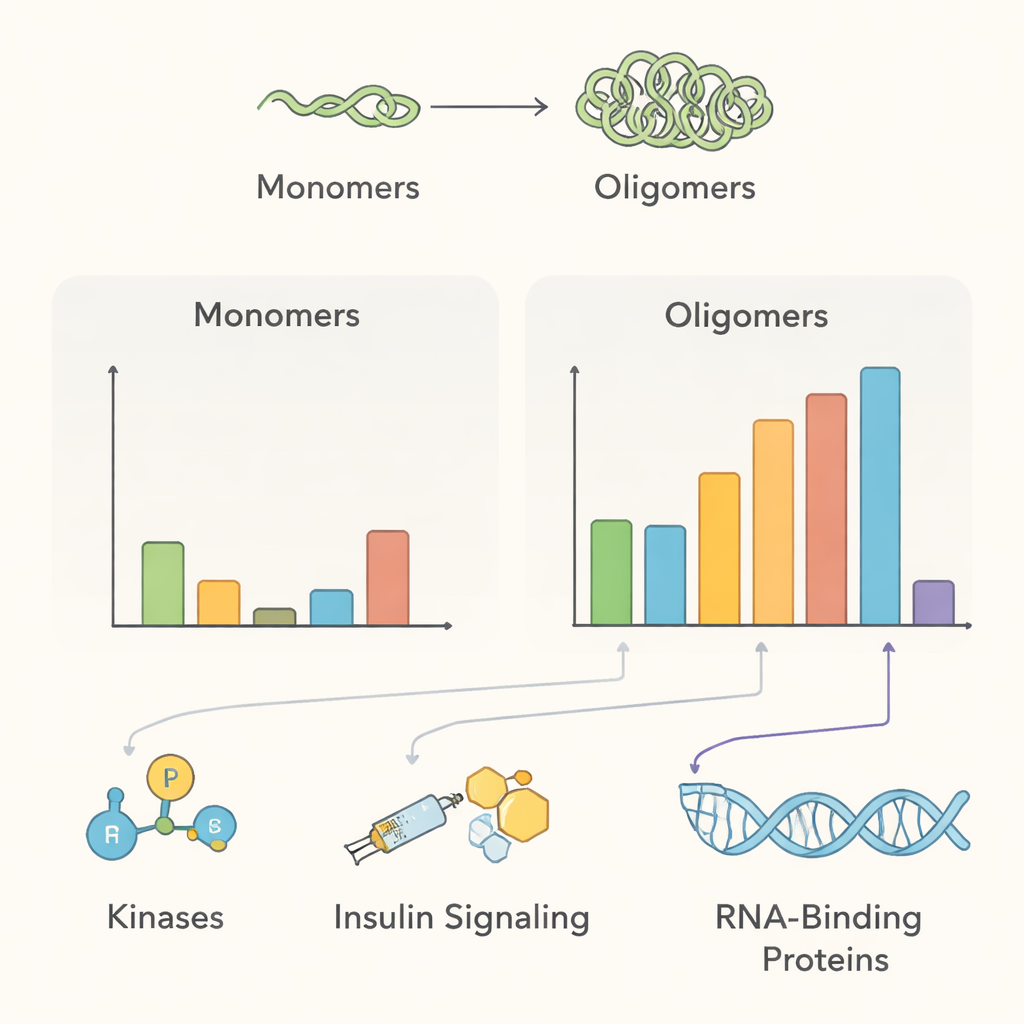
Lo schizzo dell’interattoma risultante evidenzia diversi temi biologici principali. In condizioni normali, l’alfa‑sinucleina multimerica si trovava vicino a numerose proteine coinvolte nel traffico delle membrane e ad enzimi che modificano proteine—coerente con il suo ruolo proposto nell’aiutare i neuroni a gestire le vescicole sinaptiche e mantenere il controllo della qualità proteica. Diversi enzimi che aggiungono gruppi fosfato, inclusi le chinasi PAK4, RIPK2 e MAP4K4, risultavano arricchiti vicino ai multimeri sani ma sembravano perdere contatto una volta formati gli aggregati, suggerendo che la perturbazione di queste relazioni potrebbe favorire le forme proteiche legate alla malattia. Il gruppo ha rilevato anche proteine collegate alla segnalazione del fattore di crescita simile all’insulina, a supporto delle correlazioni cliniche tra resistenza all’insulina e malattia di Parkinson, e ha scoperto che l’aggregazione recluta proteine coinvolte nello smaltimento delle proteine danneggiate, come la famiglia di chaperoni 14‑3‑3 e componenti specifici delle vie di degradazione cellulare.
Ponti inaspettati verso altri disturbi cerebrali
Oltre alla malattia di Parkinson, i dati mettono in luce una sorprendente connessione con la sclerosi laterale amiotrofica (SLA) e la demenza frontotemporale (FTD). Una proteina legante l’RNA chiamata FUS, che si localizza in modo errato e aggregate in quelle condizioni, è risultata vicina all’alfa‑sinucleina multimerica sia in condizioni normali sia quando l’aggregazione era indotta. Altre proteine legate all’RNA hanno mostrato spostamenti di prossimità con l’aggregazione dell’alfa‑sinucleina. Questi riscontri sollevano la possibilità che piccoli assemblaggi di alfa‑sinucleina possano intrappolare proteine che gestiscono l’RNA nel posto sbagliato all’interno delle cellule, collegando potenzialmente la biologia delle malattie da corpi di Lewy con quella della SLA e della FTD, sebbene interazioni fisiche dirette debbano ancora essere verificate.
Cosa significa per la comprensione della malattia
Per i non specialisti, il messaggio principale è che questo lavoro fornisce una "lista di contatti" in fase iniziale delle proteine che viaggiano con l’alfa‑sinucleina mentre passa da un ruolo fisiologico a un ammasso dannoso. Lo studio suggerisce che la perdita di certe relazioni protettive—come quelle con specifiche chinasi o enzimi del controllo qualità—potrebbe essere importante tanto quanto l’acquisizione di nuovi partner tossici. Pur essendo gli esperimenti condotti in un modello cellulare semplificato e non dimostrando ancora nessi di causa‑effetto, essi evidenziano candidati concreti e vie da testare in futuro in neuroni e tessuto cerebrale. A lungo termine, mappare questi quartieri proteici in evoluzione potrebbe guidare strategie per ripristinare interazioni protettive, sostenere la segnalazione legata all’insulina o evitare la cattura di proteine leganti l’RNA, rallentando potenzialmente il passaggio da sottili cambiamenti molecolari a forme conclamate di malattie da corpi di Lewy.
Citazione: Fernandes, A.R., Owen, A.P., Faroqi, A.H. et al. A split biotin ligase approach reveals proteins associated with oligomeric alpha-synuclein during aggregation. Sci Rep 16, 7270 (2026). https://doi.org/10.1038/s41598-026-37551-6
Parole chiave: alfa-sinucleina, malattia da corpi di Lewy, aggregazione proteica, protezionomia di prossimità, malattia di Parkinson