Clear Sky Science · it
Approfondimenti sulle differenze strutturali tra omo- e eterodimeri arricchiti da un cocktail di anticorpi monoclonali contro SARS-CoV-2
Perché miscelare anticorpi può riservare sorprese
Durante la pandemia di COVID-19, farmaci a base di anticorpi come il cocktail REGEN-COV sono stati impiegati per bloccare il virus responsabile della malattia, SARS-CoV-2. Questi medicinali sono progettati con cura, ma una volta miscelati in una vial possono formare accoppiamenti rari detti eterodimeri—due anticorpi diversi uniti in coppia. Questo studio pone una domanda pratica con grandi implicazioni per sicurezza ed efficacia: quando si formano queste coppie insolite, si comportano in modo diverso rispetto alle coppie più familiari di anticorpi identici, e ciò potrebbe modificare l’efficacia del farmaco?
Coppie insolite in un potente farmaco anti-COVID-19
REGEN-COV combina due anticorpi monoclonali, casirivimab e imdevimab, ciascuno progettato per legarsi alla proteina spike di SARS-CoV-2 in modo diverso. Quando entrambi sono formulati insieme, una piccolissima frazione di anticorpi si associa in coppie. Alcune coppie sono omodimeri (due copie dello stesso anticorpo); altre sono eterodimeri (un casirivimab più un imdevimab). Gli eterodimeri sono considerati una impurità perché non fanno parte del progetto originario del farmaco, e il loro comportamento nell’organismo è rimasto in gran parte sconosciuto. Gli autori hanno prima utilizzato un processo di purificazione in più fasi per isolare diverse specie distinte di omodimeri e l’eterodimero dallo stesso lotto di REGEN-COV, ottenendo così una rara opportunità di confrontare tutte queste formazioni fianco a fianco.
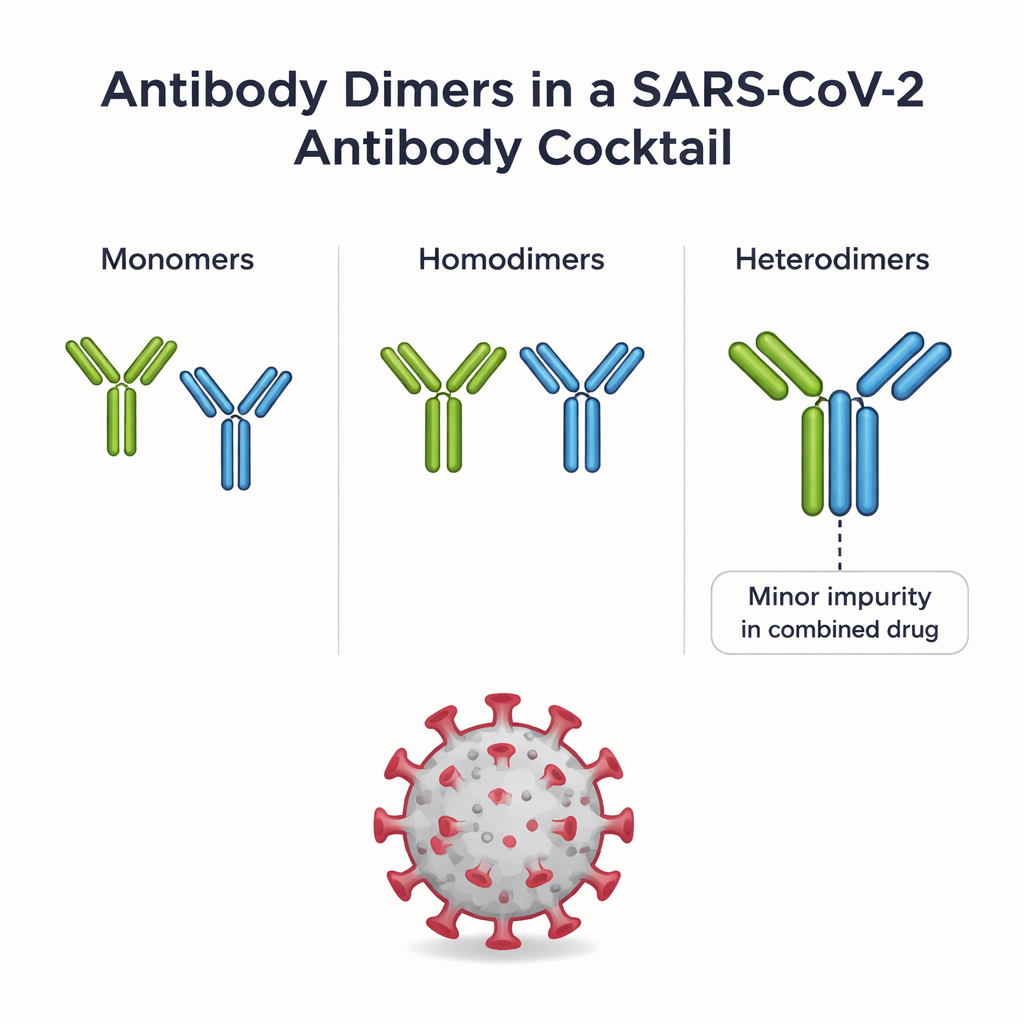
Indagare forma, adesività e legami chimici
Per capire cosa rende unico ciascun tipo di dimero, il gruppo ha combinato diversi strumenti analitici di alto livello. Esperimenti di cromatografia hanno rivelato come i dimeri differiscano in termini di “adesività” superficiale (idrofobicità), mentre l’elettroforesi capillare e una forma specializzata di spettrometria di massa hanno mostrato se i due anticorpi in un dimero siano tenuti insieme da attrazioni deboli o da legami covalenti più forti. La microscopia elettronica e l’ultracentrifugazione analitica hanno poi fornito informazioni sulla forma complessiva—se un dimero è allungato e flessibile oppure compatto e strettamente impacchettato. Insieme, questi metodi hanno mostrato che casirivimab e imdevimab formano diversi omodimeri distinti con forme e modelli di legame differenti, e che l’eterodimero è particolarmente compatto e arricchito in legami covalenti che coinvolgono parti diverse dei bracci e del gambo dell’anticorpo.
Come la struttura si collega al blocco del virus e alla citotossicità cellulare
I ricercatori hanno quindi chiesto come queste differenze strutturali influenzino ciò che conta davvero: fermare il virus e coinvolgere il sistema immunitario. Hanno testato ogni dimero in un saggio di neutralizzazione con pseudovirus, che misura quanto bene gli anticorpi bloccano l’ingresso di una particella simile a un virus, e in un saggio di citotossicità cellulare dipendente da anticorpi (ADCC), che valuta con quale efficacia gli anticorpi reclutano le cellule immunitarie per distruggere bersagli infettati. Sorprendentemente, la maggior parte delle forme dimeriche si è dimostrata almeno efficace quanto, e talvolta migliore di, i corrispondenti monomeri nel neutralizzare il virus. In particolare, gli omodimeri di imdevimab hanno mostrato una neutralizzazione “iperpotente”, probabilmente perché la loro geometria consente di collegare più proteine spike sulla superficie virale. Alcuni omodimeri di casirivimab hanno prodotto segnali ADCC particolarmente forti, apparentemente perché la loro orientazione lascia le regioni terminali (le porzioni Fc) ben esposte ai recettori delle cellule immunitarie.
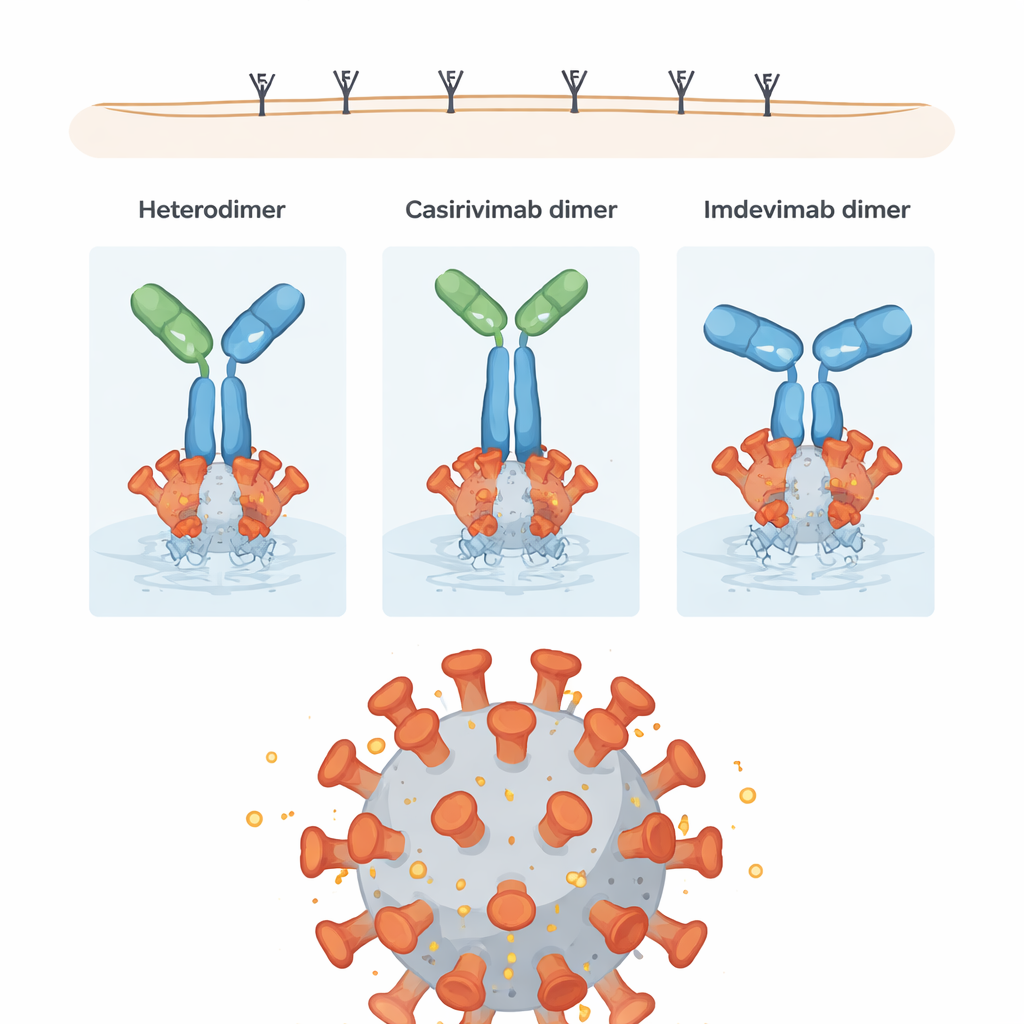
Un’impurità compatta con prestazioni miste
L’eterodimero, pur essendo ricco di connessioni compatte e robuste tra i suoi due anticorpi differenti, ha mostrato prestazioni in qualche misura ridotte: circa il 70% dell’attività neutralizzante e ADCC della miscela co-formulata prevista. L’ampio reticolo di crosslinking tra i suoi bracci e il gambo sembra limitare la libertà di rotazione e riorientamento della molecola quando è legata alla spike virale, il che a sua volta può limitare sia il blocco del virus sia la segnalazione alle cellule immunitarie. Tuttavia, molti dei suoi legami sono di un tipo che può rompersi lentamente in condizioni fisiologiche, rendendo l’eterodimero relativamente instabile nel tempo e incline a ricadere in anticorpi individuali.
Cosa significa per i farmaci a base di anticorpi
Per pazienti e sviluppatori di farmaci, il messaggio principale è rassicurante ma sfumato. Questa analisi approfondita dei dimeri di REGEN-COV suggerisce che la maggior parte delle forme dimeriche, inclusa l’insolita impurità dell’eterodimero, mantiene un’attività antivirale sostanziale, e non emerge un segnale chiaro di rischio di sicurezza aggiuntivo dovuto ad aggregati di ordine superiore in questo sistema. Allo stesso tempo, il lavoro mostra che dettagli minuti—dove gli anticorpi si toccano, quanto strettamente sono crosslinkati e quanto sono compatti o allungati—possono modificare in modo significativo la potenza. Gli autori sostengono che un profilo strutturale e funzionale simile dei dimeri in altri farmaci a base di anticorpi potrebbe diventare un potente approccio non clinico per comprendere e gestire le impurità, e potrebbe persino ispirare nuovi anticorpi multimero progettati appositamente che sfruttino la geometria per meglio riconoscere e neutralizzare i virus.
Citazione: Nguyen, J.B., Liu, S., Yan, Y. et al. Insights into the structural differences between homo- and heterodimers enriched from a cocktail of monoclonal antibodies against SARS-CoV-2. Sci Rep 16, 7024 (2026). https://doi.org/10.1038/s41598-026-37545-4
Parole chiave: dimeri di anticorpi, REGEN-COV, spike di SARS-CoV-2, cocktail di anticorpi monoclonali, aggregati proteici