Clear Sky Science · it
Immobilizzazione covalente della perossidasi di Lepidium draba su nanoparticelle magnetiche rivestite di chitosano e sua applicazione nel biosensing del glucosio
Perché i piccoli magneti contano per lo zucchero nel sangue
Mantenere sotto controllo la glicemia è fondamentale per gestire il diabete e prevenire danni a lungo termine a cuore, reni, occhi e nervi. I test del glucosio attuali funzionano bene, ma gli enzimi che li alimentano possono essere fragili, di breve durata e difficili da riutilizzare, il che aumenta i costi e i rifiuti. Questo studio esplora un modo ingegnoso per rendere un enzima vegetale più robusto e durevole fissandolo su microscopiche sfere magnetiche, aprendo la strada a test del glucosio più rapidi, più affidabili e potenzialmente più economici.
Un aiuto vegetale ispirato alla rafano
Molti test medicali si basano su enzimi—proteine che accelerano le reazioni chimiche. Un cavallo di battaglia nei laboratori diagnostici è la perossidasi di rafano, usata per trasformare cambiamenti chimici invisibili in nitidi spostamenti di colore visibili a occhio nudo. I ricercatori hanno lavorato con un parente vicino di questo enzima, chiamato perossidasi di Lepidium draba, prodotto in batteri in modo da poterlo ottenere in grandi quantità. Da sola, questa forma libera dell’enzima è potente ma delicata: perde attività con il calore, durante lo stoccaggio e con gli usi ripetuti, il che ne limita l’impiego nei sensori industriali e nei kit clinici.
Trasformare gli enzimi in strumenti magnetici
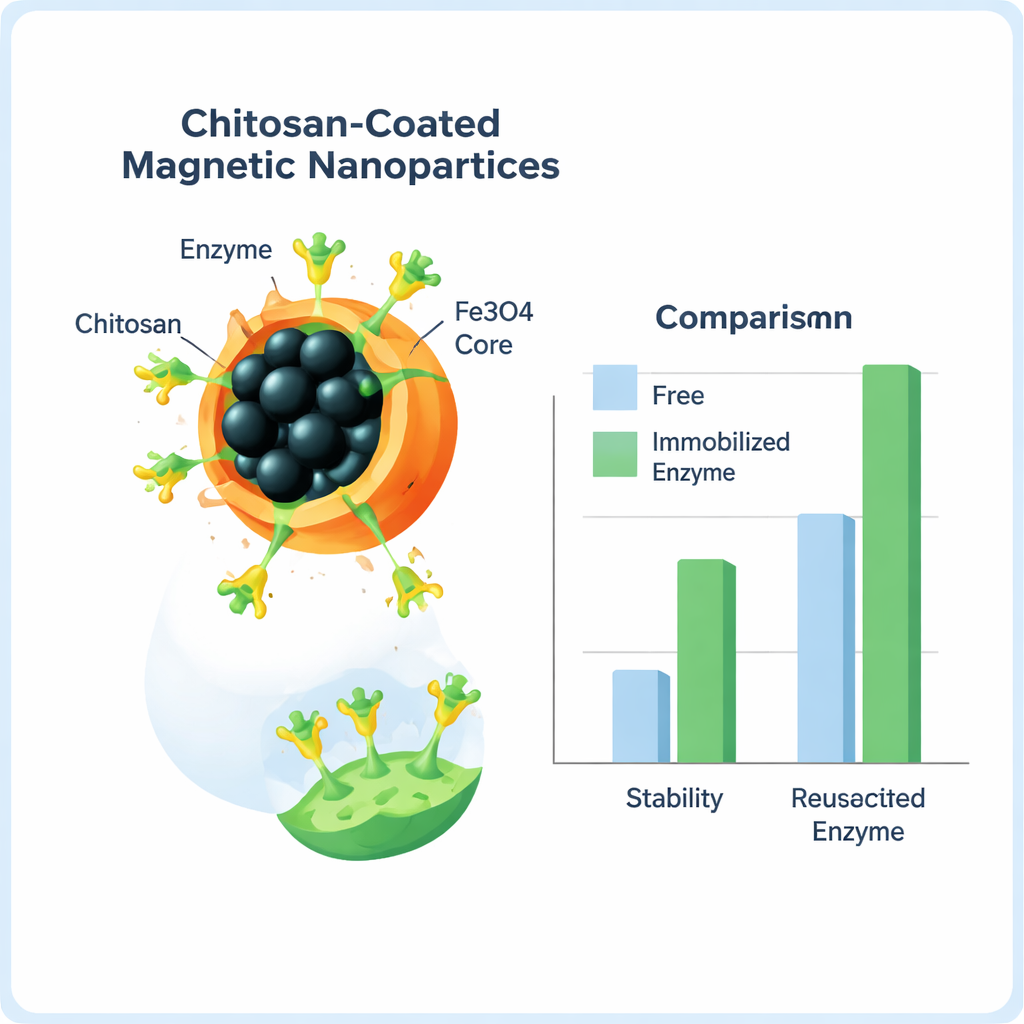
Per proteggere e riutilizzare l’enzima, il gruppo lo ha legato a nanoparticelle di ossido di ferro—minuscoli granuli di materiale magnetico—rivestite con un polimero naturale chiamato chitosano, ricavato dai gusci dei crostacei. Il chitosano fornisce uno strato morbido e biocompatibile pieno di “maniglie” chimiche in grado di agganciare gli enzimi. Usando una piccola molecola cross‑linker, il glutaraldeide, hanno creato forti legami covalenti tra l’enzima e le particelle rivestite. Gli scienziati hanno quindi ottimizzato la quantità di cross‑linker, la durata della reazione e la quantità di materiale di supporto, scegliendo condizioni che offrivano il migliore equilibrio tra quantità di enzima fissato e mantenimento dell’attività.
Verificare struttura, robustezza e durata
Dopo l’immobilizzazione, il team ha confermato che l’enzima era effettivamente ancorato alle particelle usando diversi strumenti strutturali che leggono le vibrazioni dei legami, i pattern cristallini e la morfologia superficiale. Più importante per l’uso pratico, l’enzima immobilizzato ha mostrato prestazioni superiori rispetto alla sua forma libera. Mostrava un’affinità migliore per il suo substrato colorimetrico e lo convertiva in prodotto colorato con efficienza molto maggiore—fino a 11 volte in alcuni test. L’enzima legato tollerava anche una gamma più ampia di acidità, manteneva livelli di attività maggiori attraverso temperature utili e resisteva al riscaldamento a 50 °C per molto più tempo. La sua emivita a quella temperatura più che raddoppiò e, dopo due mesi in frigorifero, conservava circa il doppio dell’attività rispetto all’enzima libero. Poiché le particelle sono magnetiche, potevano essere estratte dalla soluzione con un magnete e riutilizzate; anche dopo 11 cicli di reazione, rimaneva circa il 40% dell’attività iniziale.
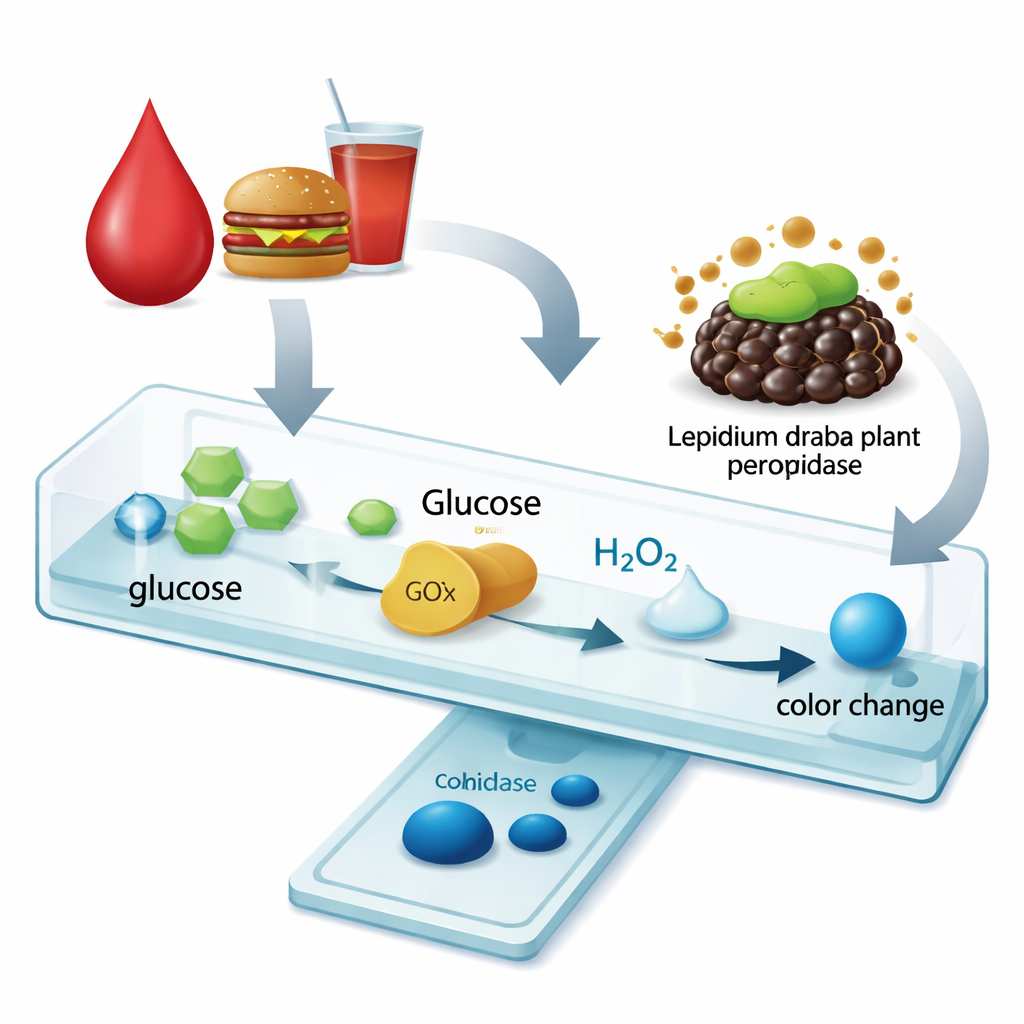
Un cambio di colore più netto per i test del glucosio
Per verificare se questo enzima più resistente migliorasse davvero un test pratico, i ricercatori hanno costruito un semplice saggio colorimetrico per il glucosio. Prima, un enzima standard, la glucosio ossidasi, converte il glucosio in perossido di idrogeno. Poi la perossidasi di Lepidium draba, libera o immobilizzata sulle sfere magnetiche di chitosano, usa quel perossido per trasformare un colorante incolore in un blu intenso. Con la forma immobilizzata, l’intervallo utile di misura del glucosio si è ampliato drasticamente—from coprire solo 0,1–1 millimole per litro con l’enzima libero a 0,1–10 millimoli per litro quando immobilizzato. Allo stesso tempo, il tempo di reazione necessario per il saggio si è ridotto a circa un terzo, mentre il livello minimo di glucosio rilevabile è rimasto molto basso e clinicamente rilevante.
Cosa significa per la salute di tutti i giorni
Ancoraeando un enzima vegetale su nanoparticelle magnetiche rivestite di chitosano, gli autori hanno creato un componente sensibile, riutilizzabile e robusto per sensori colorimetrici del glucosio. Per un non esperto, ciò significa che in futuro strisce reattive, kit di laboratorio o persino confezioni intelligenti per alimenti potrebbero diventare più stabili, più accurate su un intervallo di zuccheri più ampio e potenzialmente più economiche perché l’enzima attivo può essere recuperato e riutilizzato. Pur essendo necessari ulteriori sviluppi per aumentare la capacità di carico degli enzimi sulle particelle e per estendere l’approccio ad altri marker ematici come colesterolo o urea, questo studio dimostra come nanomateriali e polimeri naturali possano combinarsi per trasformare strumenti biochimici familiari in sistemi diagnostici più robusti, puliti e versatili.
Citazione: Sepahi-Baghan, M., Asoodeh, A. & Riahi-Madvar, A. Covalent immobilization of Lepidium draba peroxidase on chitosan-coated magnetic nanoparticles and its application in glucose biosensing. Sci Rep 16, 7035 (2026). https://doi.org/10.1038/s41598-026-37542-7
Parole chiave: biosensore per glucosio, immobilizzazione degli enzimi, nanoparticelle magnetiche, rilevazione colorimetrica, perossidasi