Clear Sky Science · it
Interazione del campo elettromagnetico pulsato a bassa frequenza (PEMF) con i mitocondri
Campi delicati e le centrali energetiche della cellula
La terapia con campo elettromagnetico pulsato (PEMF) è già utilizzata in ambito clinico per favorire la guarigione delle fratture, alleviare il dolore articolare e accelerare il recupero post‑operatorio. Tuttavia non comprendiamo ancora pienamente come questi campi delicati a bassa frequenza agiscano all’interno del nostro corpo. Questo studio pone una domanda semplice ma importante: i segnali PEMF influenzano direttamente i mitocondri, le piccole centrali energetiche delle cellule che producono la maggior parte dell’energia, e se sì, in che modo?
Perché i mitocondri sono importanti per la salute quotidiana
I mitocondri trasformano cibo e ossigeno nella molecola ATP, la «moneta energetica» universale delle cellule. Quando i mitocondri funzionano male, i tessuti guariscono più lentamente, i muscoli si affaticano prima e le malattie legate al metabolismo possono peggiorare. Poiché ricerche precedenti suggerivano che i trattamenti PEMF migliorano il metabolismo energetico e favoriscono la riparazione tissutale, gli autori si sono concentrati sul verificare se un dispositivo PEMF specifico potesse modulare l’attività mitocondriale. Hanno usato un segnale magnetico ben definito: brevi impulsi di millisecondi di un’onda seno a 30 kHz con bassa energia in ingresso, applicati a cellule muscolari in coltura, a tessuti di ratto e a mitocondri purificati.
Uno sguardo più ravvicinato all’interno delle cellule vive
In cellule muscolari umane coltivate in laboratorio, il gruppo ha misurato tre indicatori chiave dopo l’esposizione al PEMF: il potenziale elettrico attraverso la membrana interna mitocondriale (una sorta di piccola batteria), i livelli di specie reattive dell’ossigeno (che ad alti livelli possono essere dannose) e l’ossido nitrico, un gas che può bloccare temporaneamente la respirazione mitocondriale. Circa 90 minuti dopo il trattamento, il potenziale di membrana mitocondriale risultava lievemente ridotto, mentre i livelli di ossido nitrico erano diminuiti; le specie reattive dell’ossigeno non aumentavano. Un piccolo calo del potenziale di membrana può indicare sia danno che una più intensa produzione di ATP. Poiché le cellule non mostravano segni di stress, gli autori hanno ipotizzato che i mitocondri stessero semplicemente lavorando un po’ più intensamente, consumando il voltaggio immagazzinato attraverso la loro membrana interna.
Testare come «respirano» i mitocondri
Per verificare più direttamente questa ipotesi, i ricercatori hanno perforato delicatamente la membrana esterna cellulare in modo da poter fornire con precisione diversi combustibili ai mitocondri e misurarne l’uso di ossigeno. Hanno osservato in modo coerente una tendenza verso una respirazione più alta legata alla produzione di ATP dopo il PEMF, soprattutto quando era presente il glutammato, un combustibile mitocondriale comune. L’analisi statistica su numerosi campioni ha suggerito che la combinazione di esposizione a PEMF e la scelta del combustibile influenzava significativamente la velocità con cui i mitocondri consumavano ossigeno. Importante: non c’erano segnali che il PEMF danneggiasse le cellule o i loro mitocondri. Al contrario, i campi sembravano stimolare selettivamente la modalità di respirazione «accoppiata», in cui l’uso dell’ossigeno è strettamente legato alla sintesi di ATP, senza aumentare la combustione inefficiente e disaccoppiata del combustibile.
Infiammazione, ossido nitrico e una sorpresa dalla luce blu
Dato che l’ossido nitrico può accumularsi durante l’infiammazione e bloccare un passaggio chiave della respirazione mitocondriale, il gruppo ha chiesto se il PEMF potesse aiutare i mitocondri a recuperare da tale inibizione. Hanno aggiunto un donatore chimico di ossido nitrico a omogeneizzati di muscolo e fegato e a mitocondri epatici isolati, rallentando fortemente la respirazione. In queste condizioni, il PEMF non ha ripristinato la funzione mitocondriale, nemmeno quando i mitocondri erano altamente concentrati. Per verificare se il blocco fosse almeno parzialmente reversibile, hanno illuminato con luce blu i mitocondri inibiti dall’ossido nitrico, utilizzando un metodo noto per liberare l’ossido nitrico dal suo sito di legame. La luce blu ha parzialmente recuperato la respirazione, confermando che il sistema poteva riprendersi, ma il PEMF non ha fornito alcun beneficio aggiuntivo. Questo dimostra che gli effetti positivi del PEMF non derivano dalla rimozione dell’ossido nitrico in condizioni simili all’infiammazione.
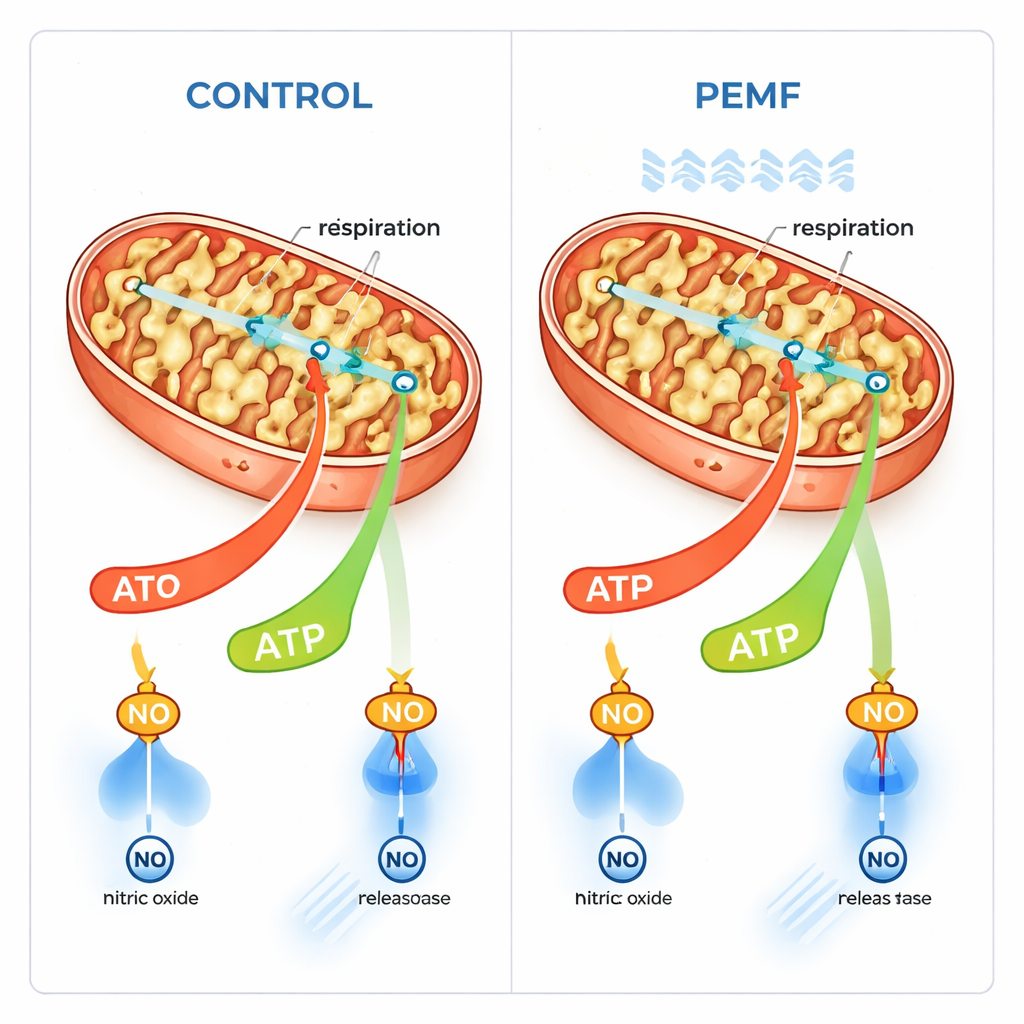
Cancelli di membrana e flusso di energia
Tracciando un’analogia tra cellule e circuiti elettrici, gli autori suggeriscono che il PEMF possa agire principalmente sulle membrane biologiche. I mitocondri sono avvolti da una membrana esterna che contiene una proteina gateway chiave chiamata VDAC, la quale permette il passaggio di molecole legate all’energia. Diversamente dall’altissimo voltaggio della membrana interna, la membrana esterna presenta un potenziale più piccolo e più facilmente influenzabile. Gli autori propongono che il PEMF alteri sottilmente questo potenziale della membrana esterna, modificando la frequenza di apertura dei «cancelli» VDAC e facilitando così il flusso di combustibile e di ATP esaurito attraverso la membrana. Questo aumenterebbe naturalmente la modalità di respirazione accoppiata, produttiva di ATP, senza cambiare la capacità massima della macchina di trasporto degli elettroni stessa.
Cosa significa per le terapie future
Complessivamente, lo studio non trova evidenze che questo tipo di PEMF sia dannoso per i mitocondri. Al contrario, il PEMF migliora delicatamente la parte della respirazione mitocondriale che produce ATP, lasciando invariate la capacità respiratoria massima e lo stress ossidativo. Tuttavia, non recupera mitocondri bloccati da alti livelli di ossido nitrico, suggerendo che i suoi benefici nei tessuti infiammati devono derivare da altre vie. Per pazienti e clinici, questi risultati supportano l’idea che campi elettromagnetici accuratamente tarati possano spingere le centrali cellulari verso uno stato più efficiente di produzione energetica, offrendo una spiegazione meccanicistica plausibile per alcuni degli effetti di guarigione osservati nella riparazione ossea, nella cura delle ferite e nel recupero post‑chirurgico.
Citazione: Zavadskis, S., Gasser, A.S., Karas, M. et al. Interaction of pulsed low frequency electromagnetic field (PEMF) with mitochondria. Sci Rep 16, 6681 (2026). https://doi.org/10.1038/s41598-026-37527-6
Parole chiave: terapia con campo elettromagnetico pulsato, mitocondri, energia cellulare, ossido nitrico, produzione di ATP