Clear Sky Science · it
Validazione di un nuovo biomarcatore genomico della scalabilità delle cellule staminali mesenchimali e implicazioni dello stato genotipico sui fenotipi di senescenza cellulare
Perché coltivare le cellule staminali diventa più difficile col tempo
Le cellule staminali del midollo osseo adulto sono un pilastro di molte terapie sperimentali, dalla riparazione delle ossa danneggiate alla modulazione dell’infiammazione. Ma c’è un problema: per trattare un paziente i laboratori devono espandere queste cellule all’esterno del corpo e, più a lungo vengono coltivate, più rallentano e si comportano come cellule “invecchiate”. Questo studio esplora perché le cellule staminali di alcune persone invecchiano più lentamente in coltura e se un piccolo pezzo mancante di DNA può aiutare gli scienziati a selezionare le cellule più robuste per trattamenti futuri.
Un gene mancante che cambia le regole
I ricercatori si sono concentrati su un gene chiamato GSTT1, che aiuta le cellule a disintossicarsi dalle molecole dannose prodotte dal metabolismo normale e dallo stress. Sorprendentemente, una frazione non trascurabile di persone è completamente priva di questo gene: sono “GSTT1 null”. Lavori precedenti avevano suggerito che le cellule staminali del midollo osseo di questi individui potessero crescere più velocemente e mantenere più a lungo i loro cappucci cromosomici protettivi, i telomeri. In questo progetto il team ha esaminato cellule staminali provenienti da sei donatori sani, le ha raggruppate in GSTT1-positive e GSTT1-null e ha quindi seguito il comportamento delle cellule durante numerosi cicli di espansione e dopo esposizione a radiazioni X, un forte induttore della senescenza cellulare.
Cellule a crescita rapida che resistono ai segnali di invecchiamento
Quando gli scienziati hanno monitorato il numero di cellule su diversi giorni, le cellule staminali GSTT1-null si sono moltiplicate più rapidamente nelle prime passate rispetto alle cellule che portavano il gene. Durante un’espansione molto prolungata i tassi di crescita tra i gruppi sono diventati più simili, ma il vantaggio iniziale era evidente. Per sondare direttamente l’invecchiamento, il team ha usato una colorazione classica che rende blu le cellule senescenti o “invecchiate”. Dopo molte divisioni e di nuovo dopo irradiazione, le colture GSTT1-null contenevano costantemente meno cellule blu senescenti rispetto alle colture GSTT1-positive. È importante sottolineare che questa differenza non derivava da un accorciamento dei telomeri più lento né da una maggiore attività dell’enzima che mantiene i telomeri (hTERT); entrambe le misure risultavano simili indipendentemente dallo stato GSTT1, suggerendo che fosse in gioco un altro meccanismo.
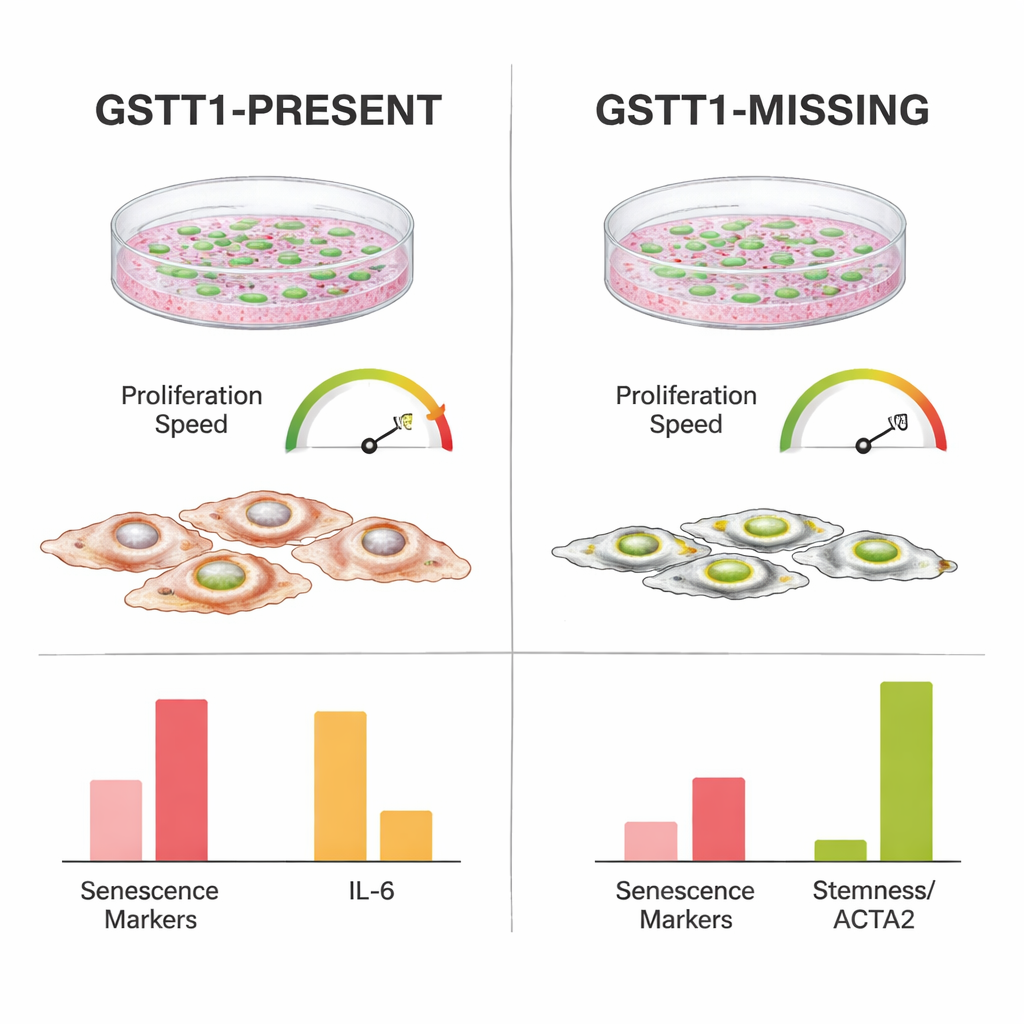
Meno stress e infiammazione in coltura
Per capire cosa rendeva più resilienti le cellule GSTT1-null, i ricercatori hanno misurato l’attività di geni legati all’arresto del ciclo cellulare, al danno del DNA e al cosiddetto fenotipo secretorio associato alla senescenza — un cocktail di segnali infiammatori e di stress rilasciati dalle cellule invecchiate. Le cellule con GSTT1 presente mostravano livelli più elevati di segnali chiave di “stop” come p21 e p14, soprattutto nelle passate avanzate e dopo irradiazione. Aumentavano inoltre l’espressione di IL-6, una potente molecola infiammatoria, e di altri geni legati allo stress in misura maggiore rispetto alle cellule GSTT1-null. Al contrario, le cellule staminali GSTT1-null mantenevano livelli inferiori di questi marcatori di invecchiamento e infiammazione, pur conservando livelli più alti di ACTA2 e TWIST1, geni associati all’integrità strutturale e a comportamenti più “stem-like”. È notevole che entrambi i genotipi conservassero una simile capacità di specializzarsi in cellule ossee e adipose, il che indica che l’effetto protettivo non derivava semplicemente da una perdita della normale funzione staminale.
Cosa potrebbe significare per le future terapie cellulari
Nel complesso i risultati suggeriscono che le cellule staminali del midollo osseo prive di GSTT1 sono in parte protette dall’usura tipica dell’espansione in laboratorio e dell’irradiazione. Crescono più rapidamente nelle fasi iniziali, accumulano meno cellule chiaramente invecchiate e mantengono un profilo meno infiammatorio, nonostante i loro cromosomi si accorcino a ritmi simili. Per aziende e cliniche che producono grandi quantità di cellule staminali, lo stato GSTT1-null potrebbe fungere da marcatore genetico pratico per identificare donatori le cui cellule tollerano meglio l’espansione, potenzialmente producendo terapie più consistenti e potenti. Naturalmente, lo studio ha utilizzato un piccolo gruppo di donatori e condizioni di coltura non cliniche, quindi sono necessari studi più ampi e controllati. Tuttavia, il lavoro mette in luce come una singola differenza ereditaria possa inclinare l’equilibrio tra comportamento giovanile e invecchiamento nelle cellule staminali coltivate per la medicina rigenerativa.
Citazione: Ardana, I.K.K.G., Maldonado, V.V., Barnes, C.L. et al. Validation of a novel genomic biomarker of mesenchymal stem cell scalability and implications of genotype status on cellular senescence phenotypes. Sci Rep 16, 6219 (2026). https://doi.org/10.1038/s41598-026-37517-8
Parole chiave: cellule staminali mesenchimali, senescenza cellulare, biomarcatori, produzione di terapie cellulari, polimorfismo GSTT1