Clear Sky Science · it
Intrappolamento del sensore di tensione NaV1.5 da parte del Mg-protoporfirina con selettività eccezionale compromette la migrazione delle cellule tumorali
Un pigmento vegetale indica una nuova strategia contro il cancro
I nostri cuori e i nostri tumori potrebbero condividere una vulnerabilità inaspettata: un particolare tipo di porta elettrica nella membrana cellulare chiamata NaV1.5. Questo studio mostra che un parente naturale dei mattoni della clorofilla nelle piante, la magnesio‑protoporfirina IX (MgPpIX), può chiudere questa porta con straordinaria precisione. Facendo ciò rallenta nettamente il movimento di alcune cellule tumorali, suggerendo che una molecola ispirata alla chimica della fotosintesi potrebbe aiutare a contenere le metastasi senza disturbare pesantemente cervello e muscoli.
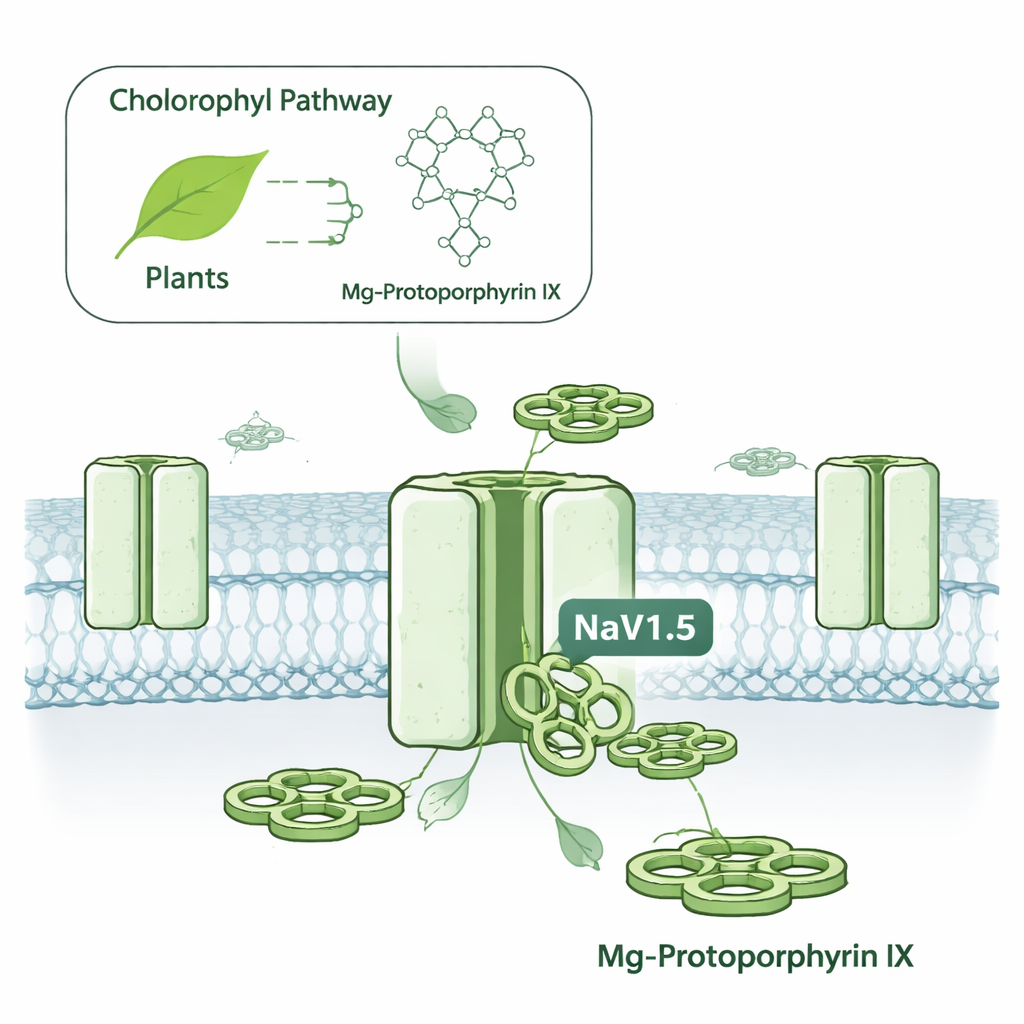
Un interruttore elettrico nascosto nelle cellule tumorali
Le cellule usano i canali del sodio voltaggio‑dipendenti come piccole porte che si aprono e si chiudono per lasciar passare particelle cariche, generando segnali elettrici. NaV1.5 è più nota per il suo ruolo nei battiti cardiaci, dove aiuta a scatenare ogni contrazione. Ma lo stesso canale si trova anche in diversi tumori, compresi quelli al seno e al colon, dove la sua attività è stata collegata a un aumento della mobilità e dell’invasività cellulare. Mirare a NaV1.5 è stato difficile perché la maggior parte dei farmaci per i canali del sodio colpisce anche canali affini nel sistema nervoso e nel muscolo scheletrico, con rischi di effetti collaterali come convulsioni, intorpidimento o debolezza muscolare. Gli autori hanno cercato di scoprire se piccole molecole potessero distinguere NaV1.5 dai suoi parenti con una selettività molto più elevata.
Un bloccante ispirato alle piante con precisione record
Il gruppo ha esaminato una famiglia di molecole ad anello chiamate protoporfirine metallate, che somigliano al nucleo dell’eme nel sangue e della clorofilla nelle piante ma contengono atomi metallici centrali diversi. Quando hanno applicato varie versioni a canali NaV1.5 umani espressi in cellule coltivate, è emerso un composto in particolare: MgPpIX. Ha ridotto la corrente elettrica attraverso NaV1.5 di circa il 99% a concentrazioni nanomolari, circa 100 volte più potente rispetto a un omologo a base di ferro (emina). Altre versioni metalliche, come quelle con nichel o rame, risultavano essenzialmente inattive. Notevolmente, MgPpIX ha lasciato intatti diversi altri tipi di canali del sodio umani (usati dal cervello, dai nervi periferici e dal muscolo scheletrico) alle stesse dosi, rendendo la sua selettività tra le più nette mai riportate per questa famiglia di canali.
Come la molecola inceppa una piccola leva di tensione
Per comprendere questa precisione insolita, i ricercatori hanno combinato modifiche genetiche con simulazioni al computer. I canali del sodio hanno quattro parti ripetute, ciascuna contenente un “sensore di tensione” che cambia posizione quando il potenziale di membrana varia. Scambiando singoli aminoacidi tra NaV1.5 e i suoi parenti insensibili, il team ha ricondotto l’azione di MgPpIX al sensore di tensione del secondo dominio, in particolare a due residui esposti all’esterno della cellula. Simulazioni di dinamica molecolare in un ambiente di membrana realistico hanno suggerito che MgPpIX si adagia contro questo sensore quando è nella posizione di riposo, la posizione “discendente”. Il centro metallico positivamente carico di MgPpIX è attratto da una catena laterale negativamente carica sul canale, mentre l’anello piatto interagisce con i lipidi circostanti. Questo legame sembra bloccare il sensore di tensione in posizione, impedendogli di passare allo stato attivo “ascendente” e mantenendo così il canale chiuso. Interessante notare che forti depolarizzazioni — come quelle durante un battito cardiaco — possono temporaneamente scardinare la molecola, un comportamento che gli autori descrivono come “dipendenza d’uso inversa”.
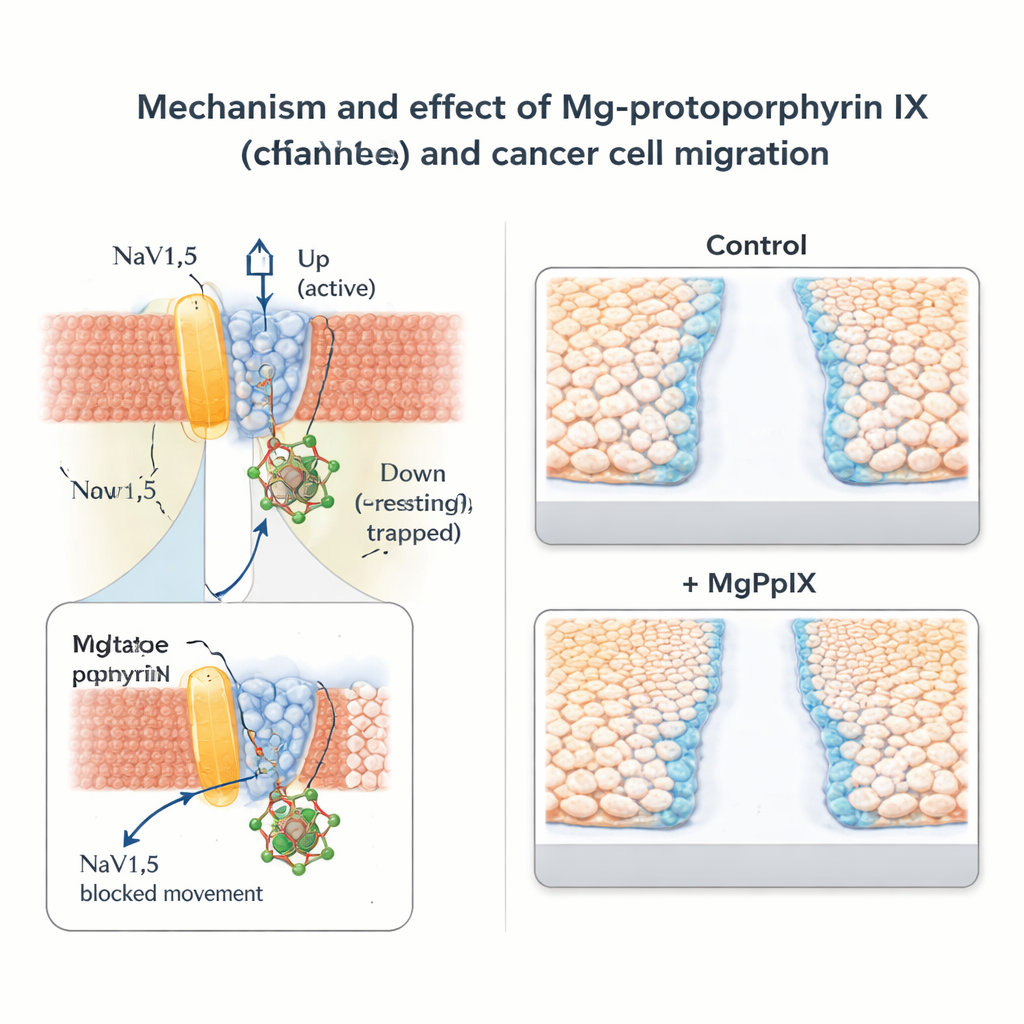
Rallentare la migrazione delle cellule tumorali senza bloccare ampiamente i nervi
Il gruppo ha poi esplorato cosa significa questo freno molecolare per il comportamento tumorale. In linee cellulari di carcinoma mammario (MDA‑MB‑231) e del colon (SW‑480) che esprimono naturalmente NaV1.5, MgPpIX ha ridotto drasticamente le correnti di sodio e rallentato la migrazione cellulare nei classici saggi di “scratch” e transwell. Quanto più un dato protoporfirina metallica bloccava NaV1.5, tanto più ostacolava il movimento cellulare, rafforzando il legame tra attività del canale e motilità. Al contrario, linee tumorali prive di NaV1.5 non mostravano risposta a MgPpIX né elettricamente né nei test di migrazione, a sostegno dell’idea che l’effetto sia altamente specifico e non semplicemente tossico. Rispetto alla classica tossina dei canali del sodio tetrodotossina, MgPpIX ha ottenuto una soppressione della migrazione più marcata a concentrazioni molto più basse.
Promesse e cautele per futuri farmaci anti‑metastasi
Per il non specialista, il messaggio centrale è che i ricercatori hanno trovato una molecola di origine vegetale che agisce come una pinza di precisione su una porta elettrica di tipo cardiaco dirottata da alcuni tumori. Intrappolando la piccola leva di tensione della porta nella posizione di riposo, MgPpIX può ridurre fortemente la mobilità delle cellule tumorali in laboratorio facendo risparmiare altri canali del sodio cruciali per la sensibilità e il movimento. Poiché l’attività elettrica rapida del cuore può parzialmente alleviare questo blocco, potrebbe esserci anche una finestra di sicurezza in cui le cellule tumorali sono inibite più delle cellule cardiache. Pur non essendo MgPpIX stessa immediatamente pronta come farmaco, il suo sito di legame e il suo meccanismo unico forniscono un potente progetto per sviluppare futuri farmaci mirati a fermare la diffusione del cancro colpendo NaV1.5 con una selettività senza precedenti.
Citazione: Jamili, M., Ahmed, M., Bernert, A. et al. Exceptionally selective voltage-sensor trapping of NaV1.5 channels by Mg-protoporphyrin impairs cancer cell migration. Sci Rep 16, 4085 (2026). https://doi.org/10.1038/s41598-026-37492-0
Parole chiave: canali del sodio, Nav1.5, migrazione delle cellule tumorali, molecole derivate dalla clorofilla, farmaci mirati sui canali ionici