Clear Sky Science · it
MiniPromoter Ple384 (TH) e Ple388 (PITX3) per il targeting dei neuroni dopaminergici del mesencefalo in topi e scimmie
Perché questa ricerca è importante per la salute del cervello
Le cellule cerebrali che producono dopamina ci aiutano a muoverci, apprendere dalle ricompense e mantenere la motivazione. Sono anche le cellule che muoiono nella malattia di Parkinson. Scienziati e medici vorrebbero consegnare geni utili o strumenti molecolari proprio a questi neuroni vulnerabili, sia negli animali di laboratorio sia, un giorno, negli esseri umani. Ma indirizzare la terapia genica in modo che si attivi soltanto nelle cellule giuste, e non ovunque nel cervello, è stato un importante ostacolo. Questo studio descrive due nuovi, compatti “interruttori” di DNA che possono attivare in modo affidabile geni quasi esclusivamente nei neuroni dopaminergici del mesencefalo di topi e scimmie, aprendo la strada a trattamenti più precisi e potenzialmente più sicuri.
Piccoli interruttori genetici con un grande compito
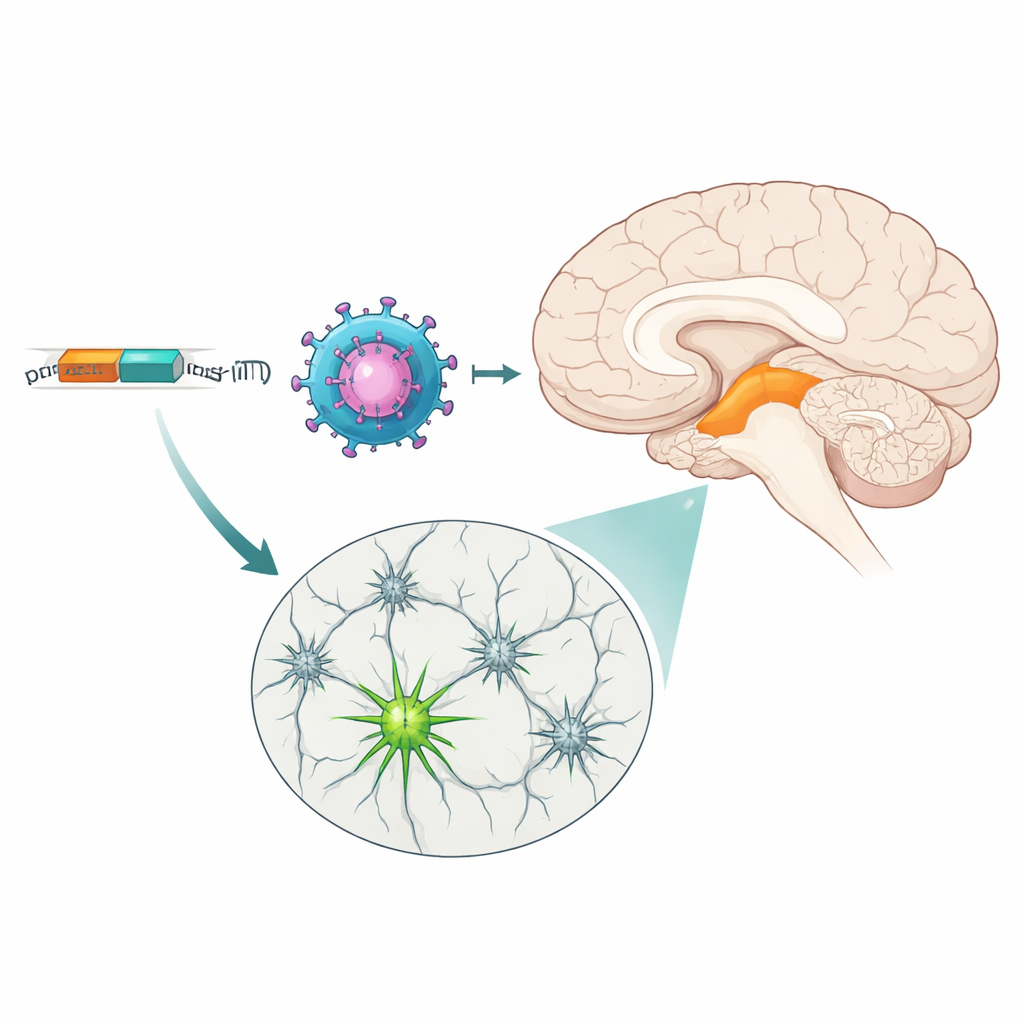
Per portare un gene terapeutico nelle cellule cerebrali, i ricercatori spesso usano virus adeno-associati (AAV), vettori innocui che possono trasportare solo una quantità limitata di DNA. All’interno di ciascun virus, una breve sequenza promotrice agisce come un interruttore on–off, decidendo dove quel gene sarà attivo. Molti promotori naturali sono troppo grandi o troppo generici, attivando i geni in troppi tipi cellulari. Il team ha usato la bioinformatica per progettare otto “MiniPromoters” molto compatti a partire dal DNA umano—brevi combinazioni di elementi di controllo presi da geni noti per marcare i neuroni produttori di dopamina. L’obiettivo era ottenere una serie di interruttori che entrassero negli AAV ma che guidassero comunque un’espressione forte e focalizzata per tipo cellulare.
Trovare i bersagli giusti nel cervello del topo
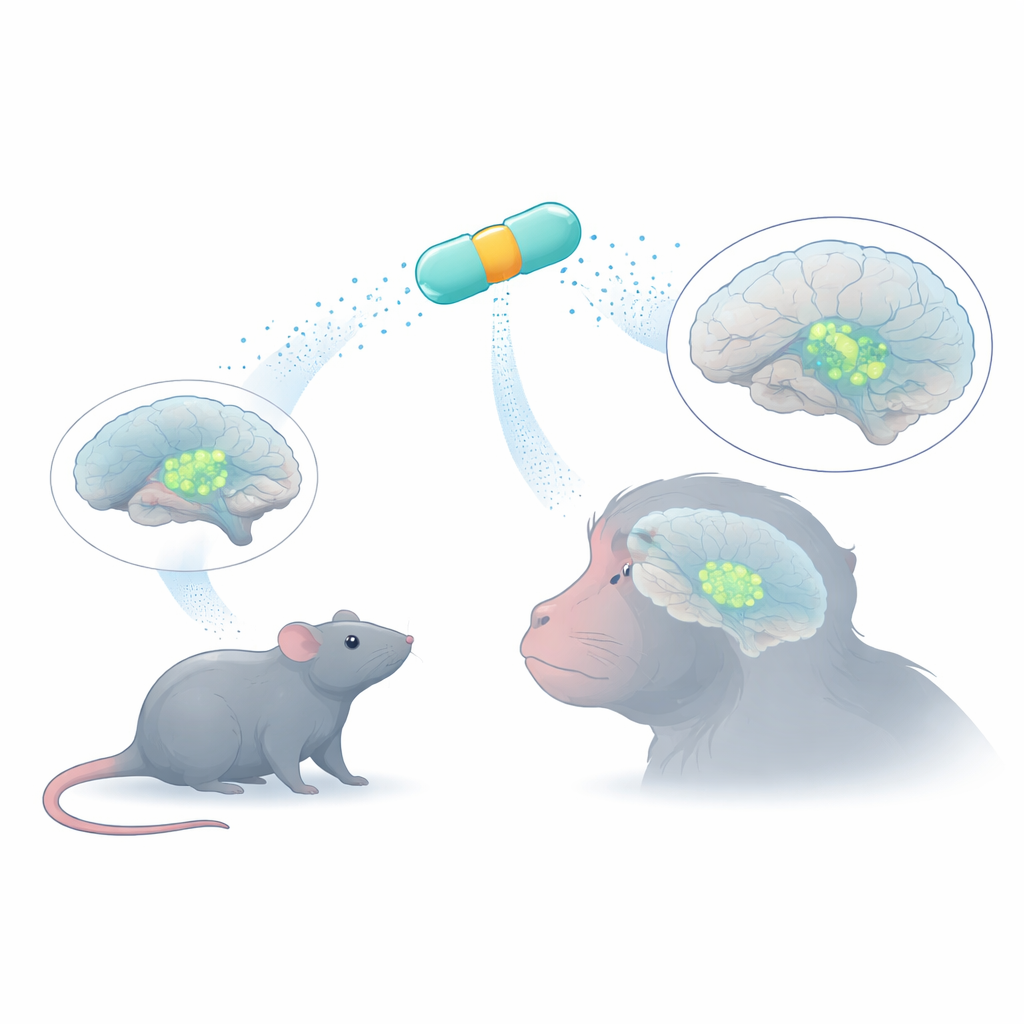
Gli otto MiniPromoters candidati sono stati prima testati nei topi. Ciascun promotore è stato inserito in un AAV contenente una proteina fluorescente verde, permettendo agli scienziati di vedere dove lo switch era attivo. Hanno somministrato i virus o nel flusso sanguigno o direttamente negli spazi pieni di liquido del cervello. La maggior parte dei MiniPromoters non si è dimostrata selettiva: alcuni si accendevano in molte cellule non dopaminergiche, altri funzionavano appena. Due si sono distinte. Una, chiamata Ple384, è stata costruita da regioni di controllo del gene della tirosina idrossilasi, l’enzima chiave usato da tutti i neuroni che producono catecolamine. L’altra, Ple388, derivava da PITX3, un gene critico per un sottogruppo di neuroni dopaminergici del mesencefalo. Sia Ple384 sia Ple388 hanno prodotto segnali luminosi, strettamente confinati nella substantia nigra pars compacta e nell’area tegmentale ventrale—i centri mesencefalici dei neuroni dopaminergici—con oltre il 90% delle cellule etichettate che portavano anche la molecola caratteristica della dopamina.
Da topi a scimmie senza perforare in profondità il cervello
Qualsiasi terapia genica destinata a una malattia umana deve infine funzionare nei primati, i cui cervelli sono più grandi e complessi. Iniettare direttamente la substantia nigra è tecnicamente impegnativo e può danneggiare questa struttura piccola e profonda. Invece, i ricercatori hanno testato se gli stessi MiniPromoters potessero essere somministrati nel liquido cerebrospinale di macachi rhesus tramite una singola iniezione in un ventricolo laterale. Usando una variante di capsid AAV nota per diffondersi ampiamente dagli spazi liquidi, hanno scoperto che sia Ple384 sia Ple388 guidavano un’espressione robusta nei neuroni dopaminergici del mesencefalo della substantia nigra e dell’area tegmentale ventrale, risparmiando in gran parte altre regioni ricche di dopamina come l’ipotalamo e il locus coeruleus. La maggior parte delle cellule etichettate nella regione bersaglio era costituita da neuroni dopaminergici, confermando che gli interruttori mantenevano la loro selettività tra le specie.
Due strumenti con punti di forza diversi
Sebbene entrambi i MiniPromoters colpissero i loro bersagli, lo fecero con pattern diversi. Ple384, basato sul più ampio gene della tirosina idrossilasi, ha illuminato complessivamente più neuroni e ha coperto sia gli strati ventrali che dorsali della substantia nigra oltre a una porzione più ampia dell’area tegmentale ventrale. Ple388, rispecchiando il gene PITX3 più ristretto, etichettava principalmente un sottogruppo di neuroni del livello ventrale e produceva una fluorescenza più debole. L’espressione fuori bersaglio è stata osservata principalmente vicino ai siti di iniezione e in alcuni organi periferici dopo somministrazione nel flusso sanguigno, ma controlli accurati hanno mostrato che i vettori virali erano in grado di raggiungere molte regioni cerebrali; erano i MiniPromoters stessi a limitare l’espressione soprattutto ai neuroni dopaminergici del mesencefalo. Questa forza regolabile—uno più potente e ampio, l’altro più selettivo e moderato—significa che i ricercatori possono scegliere lo switch che meglio si adatta alle loro esigenze, dalla modulazione lieve all’intervento su larga scala.
Cosa significa per le terapie future
Per un non specialista, il messaggio chiave è che gli autori hanno creato due compatti interruttori genetici che agiscono come interruttori programmabili e precisi per i neuroni della dopamina sia nei topi sia nelle scimmie. Ple384 offre un accesso forte e diffuso a queste cellule, mentre Ple388 si concentra su un sottogruppo più ristretto e particolarmente vulnerabile. Poiché gli interruttori sono abbastanza piccoli da entrare agevolmente nei vettori virali comunemente usati, lasciano spazio per i geni terapeutici e possono aiutare a ridurre gli effetti collaterali evitando regioni cerebrali indesiderate. Con l’avanzare della terapia genica per il morbo di Parkinson e condizioni correlate, elementi di controllo mirati come questi saranno ingredienti essenziali per trattamenti potenti ma precisi.
Citazione: Galvan, A., Choi, D., Korecki, A.J. et al. MiniPromoters Ple384 (TH) and Ple388 (PITX3) for targeting midbrain dopaminergic neurons in mice and monkeys. Sci Rep 16, 9277 (2026). https://doi.org/10.1038/s41598-026-37466-2
Parole chiave: neuroni della dopamina, terapia genica, morbo di Parkinson, vettori AAV, promotori specifici per tipo cellulare