Clear Sky Science · it
Effetti terapeutici dell’IGF-2 sulla NMOSD inibendo l’apoptosi degli astrociti tramite la modulazione della via di segnalazione IGF-1R/PI3K/AKT
Proteggere il cervello in una malattia autoimmune poco conosciuta
Il disturbo dello spettro della neuromielite ottica, o NMOSD, è una malattia autoimmune rara ma devastante che attacca i nervi ottici e il midollo spinale, lasciando spesso i pazienti con cecità, paralisi o gravi problemi cognitivi. I farmaci attuali mirano soprattutto a calmare il sistema immunitario, sono costosi e non proteggono direttamente le cellule cerebrali dal danno. Questo studio esplora se una molecola naturale legata alla crescita presente nel sangue, chiamata IGF‑2, possa aiutare a proteggere le cellule cerebrali dai danni nella NMOSD e offrire un nuovo approccio terapeutico.
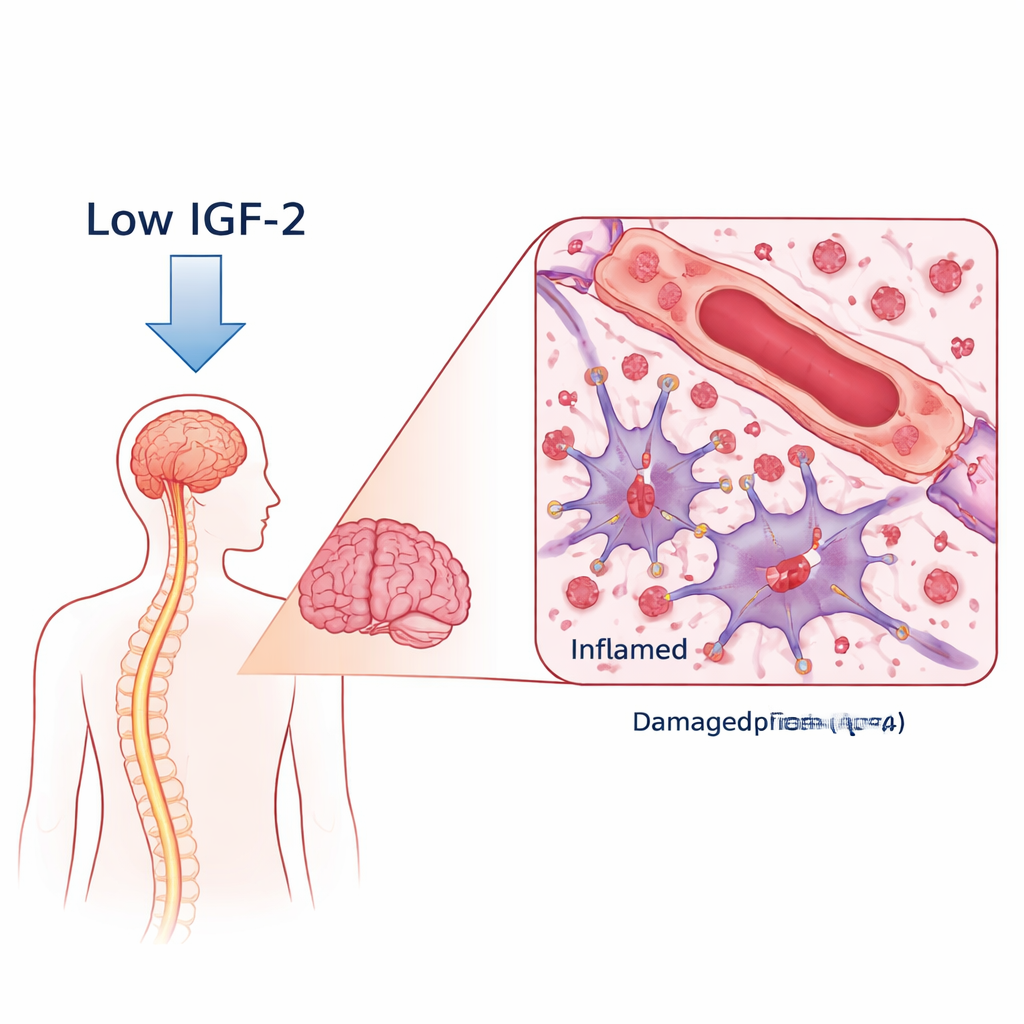
Un anticorpo dannoso e un protettore assente
Nella NMOSD, l’organismo produce anticorpi contro una proteina canale per l’acqua chiamata AQP4, presente sulle cellule di supporto a forma stellata del cervello chiamate astrociti. Quando questi anticorpi si legano, scatenano attacchi immunitari che danneggiano gli astrociti, rimuovono la mielina (il rivestimento isolante dei nervi) e possono danneggiare i neuroni. I ricercatori hanno confrontato il sangue di donne con NMOSD positive per anticorpi anti‑AQP4 e quello di volontarie sane. Attraverso un’analisi proteica estesa, hanno rilevato che i livelli di IGF‑2 erano nettamente più bassi nei pazienti con NMOSD, mentre due proteine leganti l’IGF che possono sequestrare IGF‑2 risultavano più alte. È importante che i pazienti con i livelli più bassi di IGF‑2 tendevano ad avere disabilità più gravi e punteggi peggiori nei test di memoria e delle funzioni cognitive, collegando questa molecola alla gravità della malattia e alla salute cognitiva.
Il trattamento standard favorisce il recupero di IGF-2
Molti pazienti con NMOSD ricevono rituximab, un farmaco che elimina le cellule B produttrici di anticorpi. Il team ha misurato le proteine nel sangue prima e dopo il trattamento con rituximab. Dopo la terapia, i livelli di IGF‑2 sono aumentati e le proteine leganti sono diminuite, avvicinandosi al profilo osservato nelle persone sane. Ciò suggerisce che moderare il sistema immunitario possa permettere all’organismo di ripristinare alcuni dei suoi fattori protettivi. Sebbene rituximab non sia progettato per agire direttamente su IGF‑2, lo spostamento di questa molecola suggerisce che potrebbe far parte della risposta di recupero dell’organismo e che il monitoraggio di IGF‑2 potrebbe aiutare a seguire l’evoluzione clinica dei pazienti nel tempo.
Testare l’IGF-2 in una versione murina della malattia
Per verificare se IGF‑2 possa fare più che segnalare la gravità della malattia, gli scienziati si sono rivolti a un modello murino. Hanno iniettato anticorpi umani anti‑AQP4 e complemento umano nel cervello dei topi, riproducendo caratteristiche chiave della NMOSD: perdita di AQP4 sugli astrociti, infiammazione, danno alla mielina e debolezza degli arti. Un altro gruppo di topi ha ricevuto prima un virus innocuo che induceva le cellule cerebrali a produrre IGF‑2 in eccesso. Questi topi con IGF‑2 aumentato hanno perso meno peso, manifestato problemi motori più lievi e mostrato minore perdita di mielina e infiammazione nei tessuti cerebrali e spinali. Anche il trattamento standard con rituximab ha dato benefici, ma la sovraespressione di IGF‑2 sembra aver protetto il tessuto cerebrale in modo più diretto, suggerendo un ruolo neuroprotettivo oltre a un’azione esclusivamente immunosoppressiva.
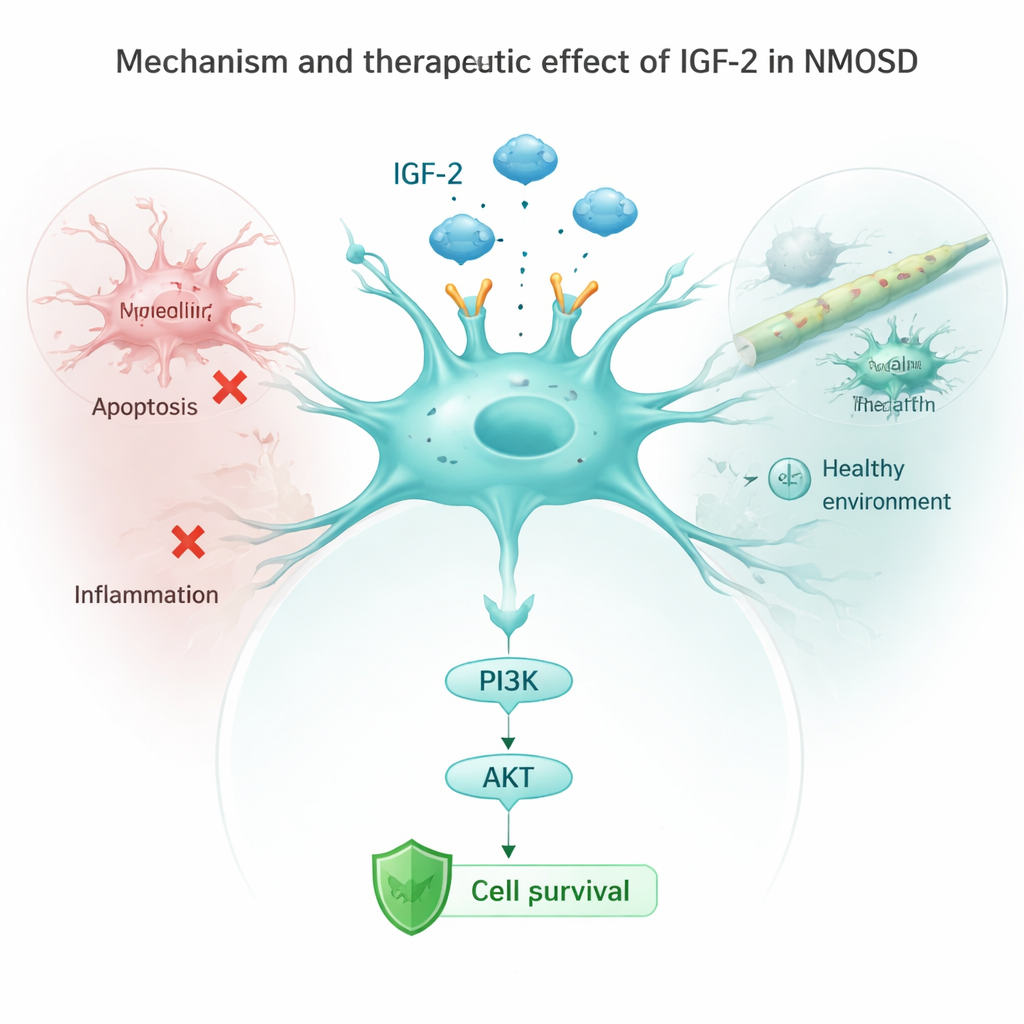
Come l’IGF-2 mitiga la morte cellulare e l’infiammazione
Il team ha poi esaminato astrociti in coltura esposti agli anticorpi della NMOSD. Normalmente questi anticorpi riducevano i livelli di un recettore chiave chiamato IGF‑1R e attenuavano una via di sicurezza a valle nota come PI3K/AKT, attivando al contempo proteine “autodistruttive” e segnali infiammatori. Quando i ricercatori hanno indotto gli astrociti a produrre più IGF‑2, questa via protettiva si è riattivata, i marcatori di morte cellulare sono calati e le cellule hanno rilasciato meno molecole infiammatorie come IL‑1β, IL‑6 e TNF‑α. Il blocco del recettore IGF‑1R ha in parte annullato questi benefici, mostrando che l’IGF‑2 agisce principalmente attivando la catena IGF‑1R/PI3K/AKT all’interno degli astrociti. Nei topi viventi, l’aumento di IGF‑2 ha anche ridotto l’attivazione delle microglia, le sentinelle immunitarie del cervello, e ha abbassato i segnali infiammatori nel circolo sanguigno.
Cosa potrebbe significare per i pazienti
Nel complesso, questi risultati suggeriscono che bassi livelli di IGF‑2 sono sia un segnale d’allarme sia un’opportunità mancata nella NMOSD. I pazienti con meno IGF‑2 tendono a essere più disabili e a presentare funzioni cognitive peggiori, mentre il ripristino o l’aumento di IGF‑2 nei modelli sperimentali aiuta gli astrociti a sopravvivere, riduce l’infiammazione cerebrale e attenua il danno nervoso. Sebbene questo lavoro sia preliminare e basato su un numero limitato di pazienti e su studi animali, indica l’IGF‑2 come un bersaglio promettente per terapie future che non solo attenuerebbero l’attacco immunitario ma proteggerebbero direttamente le cellule cerebrali vulnerabili.
Citazione: Zhang, Y., Xu, N., Yu, K. et al. Therapeutic effects of IGF-2 on NMOSD by inhibiting astrocyte apoptosis through modulation of the IGF-1R/PI3K/AKT signaling pathway. Sci Rep 16, 6312 (2026). https://doi.org/10.1038/s41598-026-37456-4
Parole chiave: neuromielite ottica, astrociti, IGF-2, neuroinfiammazione, neuroprotezione