Clear Sky Science · it
La valutazione metabolomica rivela l’esaurimento di aminoacidi e metaboliti energetici nel muscolo scheletrico dopo danno renale acuto ischemico nei topi
Perché i reni danneggiati possono prosciugare la tua forza
Le persone con insufficienza renale improvvisa notano spesso qualcosa che sembra non avere a che fare con urine o esami del sangue: i muscoli si sentono deboli e il recupero è lento. Questo studio pone una domanda semplice ma importante: quando i reni subiscono un danno acuto, cosa succede effettivamente all’interno dei carburanti e dei mattoni di costruzione dei nostri muscoli? Utilizzando un’indagine chimica dettagliata sui muscoli di topo, i ricercatori mostrano che il danno renale acuto scatena un depauperamento a livello corporeo di nutrienti chiave e molecole energetiche, lasciando il muscolo scheletrico in uno stato impoverito e povero di energia.
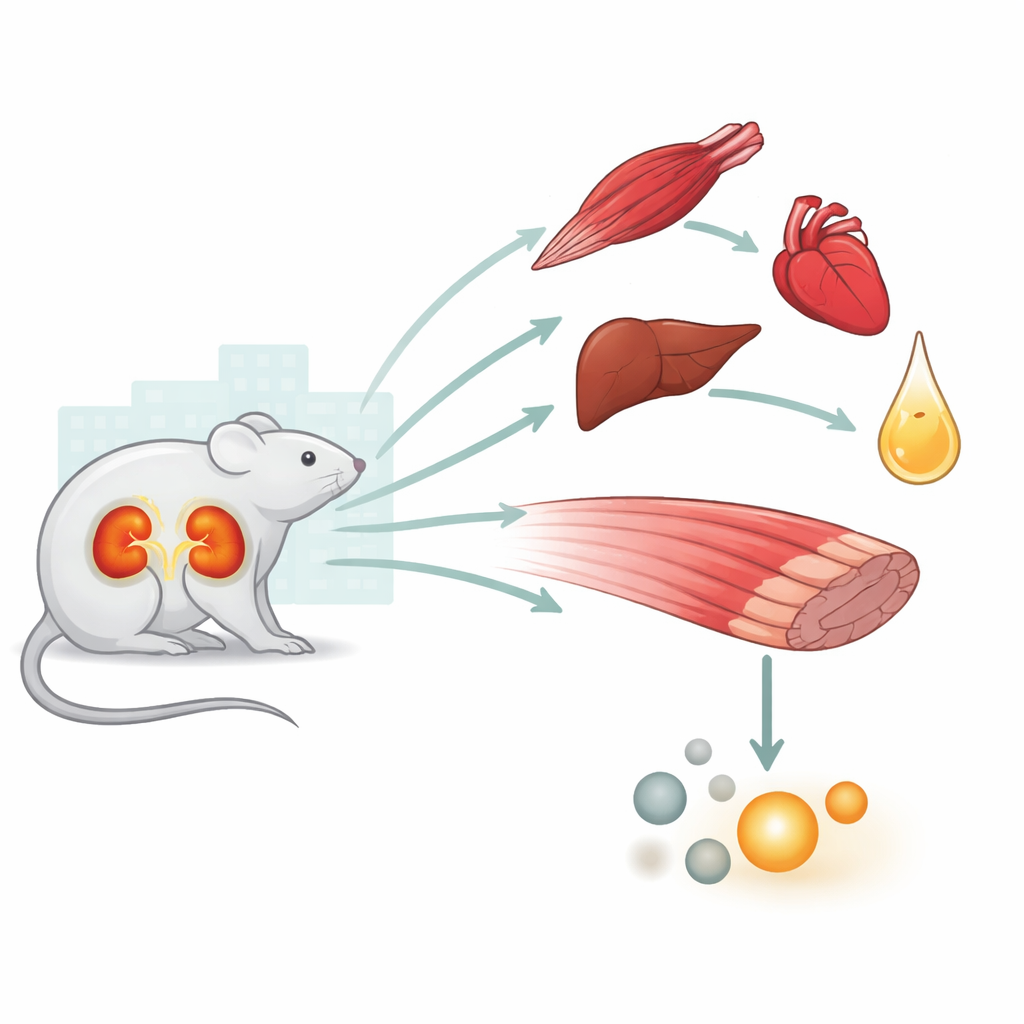
Una crisi che coinvolge tutto il corpo, non solo i reni
Il danno renale acuto (AKI) è comune nei pazienti ospedalizzati e critici ed è fortemente associato a un maggior rischio di morte. I medici hanno da tempo osservato che l’AKI si comporta come uno stato di stress che coinvolge tutto l’organismo, colpendo cuore, polmoni, fegato, cervello e muscoli. Lavori precedenti di questo gruppo avevano mostrato che dopo una temporanea perdita di flusso sanguigno ai reni nei topi, cuore, fegato, polmoni e gli stessi reni presentavano segni chimici di bassa energia e stress ossidativo. Partendo da questi risultati, lo studio attuale si concentra sul muscolo scheletrico, un importante serbatoio di carboidrati e aminoacidi che l’organismo può utilizzare durante uno stress severo.
Come è stato condotto lo studio nei topi
I ricercatori hanno indotto AKI ischemico in topi maschi giovani adulti bloccando brevemente l’apporto di sangue a entrambi i reni, quindi consentendo il ripristino del flusso. Hanno confrontato questi animali con topi sottoposti a intervento fittizio (sham) e con controlli non operati. A 24 e 72 ore hanno raccolto un muscolo chiave della gamba (il gastrocnemio) e hanno usato un approccio metabolomico non mirato — una scansione chimica ultra‑sensibile — per misurare 175 piccole molecole, inclusi aminoacidi, antiossidanti e composti legati all’energia. Sono stati impiegati metodi statistici e di riconoscimento dei pattern per determinare quali molecole cambiassero maggiormente e come la chimica muscolare differisse tra i gruppi.
Carburante muscolare e antiossidanti in calo
I cambiamenti più sorprendenti si sono manifestati 24 ore dopo il danno renale. Circa due quinti di tutti i metaboliti rilevati risultavano alterati, e il quadro complessivo era chiaro: molti composti chiave nel muscolo erano depleti rispetto all’intervento fittizio. Aminoacidi essenziali e non essenziali come alanina, valina, lisina, metionina e tirosina sono diminuiti, così come diverse molecole del ciclo dell’urea (arginina, citrullina, ornitina, argininosuccinato) che aiutano a gestire i rifiuti azotati e a supportare la produzione di creatina. Il principale antiossidante cellulare, il glutatione, e i suoi precursori (inclusa la metionina e un dipeptide cisteina‑glicina) sono risultati ridotti, indicativo di uno stress ossidativo aumentato. Anche le molecole legate all’energia, tra cui la creatina e intermedi delle vie energetiche centrali, tendevano a diminuire, suggerendo che il muscolo stia sacrificando le proprie riserve per sostenere il resto dell’organismo.
Collegare il muscolo agli altri organi
Per inquadrare il quadro più ampio, il team ha confrontato i dati muscolari con profili metabolomici raccolti in precedenza da rene, fegato, cuore e plasma sanguigno allo stesso punto temporale di 24 ore. In tutti questi siti si sono ripetuti alcuni temi: esaurimento diffuso del glutatione e dei suoi precursori, riduzione dell’alanina e alterazioni coerenti della chimica legata all’arginina e al ciclo dell’urea. Allo stesso tempo, alcuni prodotti di degradazione, come l’allantoina (un marcatore di stress ossidativo), sono aumentati in più organi e nel circolo sanguigno. Creatina e la sua forma ad alta energia, la fosfocreatina, risultavano relativamente aumentate in fegato, rene e sangue, mentre arginina e aminoacidi cadevano in muscolo e plasma, suggerendo che il muscolo scheletrico potrebbe esportare substrati affinché altri organi — e in particolare i reni lesionati — possano continuare a produrre energia sotto sforzo.
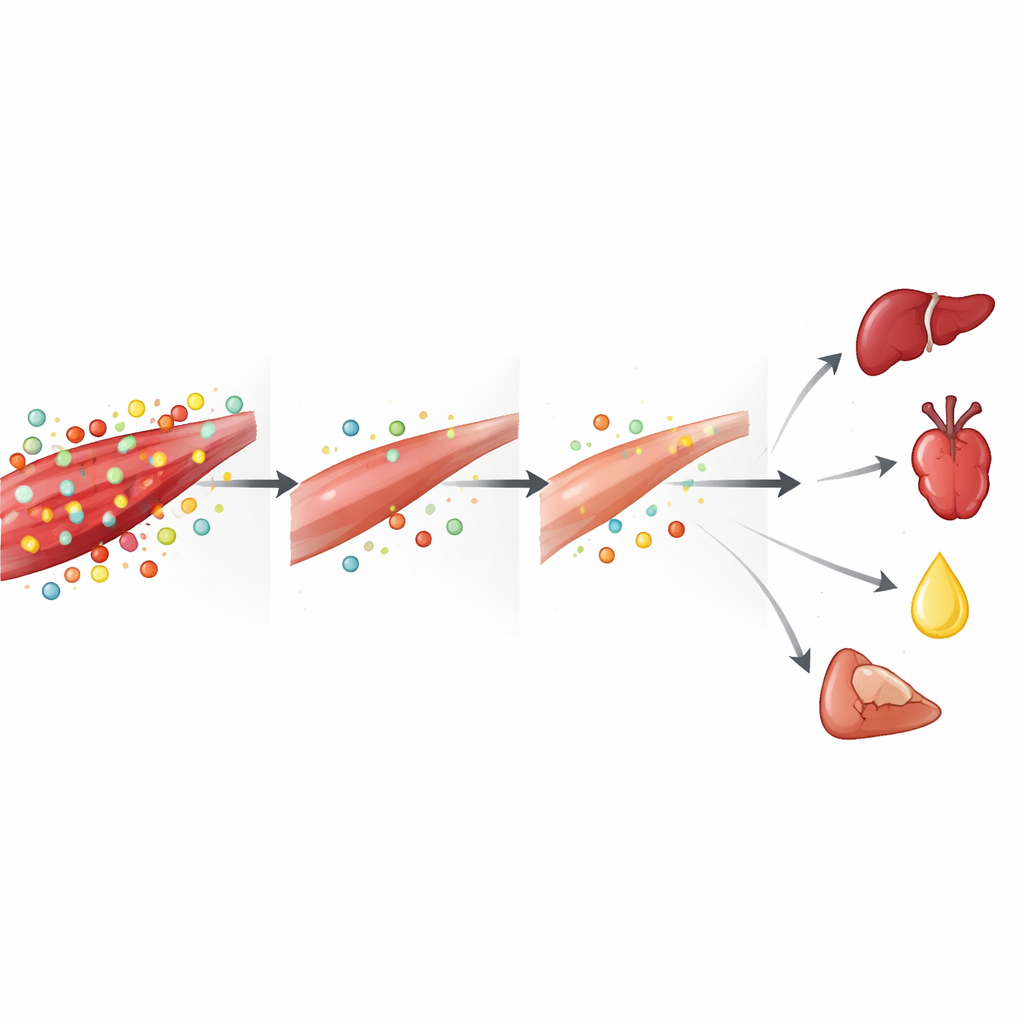
Cosa significa per i pazienti e per terapie future
Riletto in termini quotidiani, lo studio descrive l’AKI come un evento metabolico di «prelievo» per l’organismo: il muscolo scheletrico degrada le sue riserve di proteine e antiossidanti per aiutare a nutrire e proteggere organi vitali, lasciando i muscoli stessi a corto di carburante e difese. Questo aiuta a spiegare perché le persone con danno renale grave sono soggette a perdita muscolare, debolezza e scarsa ripresa funzionale. Solleva inoltre la possibilità che un supporto nutrizionale mirato — in particolare aminoacidi e composti che rinforzano i sistemi glutatione e creatina‑fosfocreatina — possa un giorno contribuire a proteggere sia i reni sia i muscoli durante malattie acute. Pur essendo risultati derivati da topi e basati su istantanee chimiche più che su tracciamenti diretti dei flussi, forniscono una mappa dettagliata di come la chimica muscolare sia disturbata dal danno renale e indicano nuove strategie per preservare la forza e migliorare gli esiti quando i reni vengono a mancare all’improvviso.
Citazione: Li, A.S., Baker, P.R., Park, S. et al. Metabolomic assessment reveals depletion of amino acids and energy metabolites in skeletal muscle after ischemic acute kidney injury in mice. Sci Rep 16, 8823 (2026). https://doi.org/10.1038/s41598-026-37424-y
Parole chiave: danno renale acuto, metabolismo del muscolo scheletrico, esaurimento di aminoacidi, stress ossidativo, metabolomica