Clear Sky Science · it
Analisi della funzione cardiaca sistolica in topi privi di PERM1 utilizzando grandi coorti di animali
Perché i piccoli cuori dei topi contano per la salute umana
L’insufficienza cardiaca è spesso descritta come una pompa stanca, ma ciò che rende effettivamente debole un cuore è sorprendentemente complesso. In questo studio, gli scienziati hanno usato un gruppo insolitamente ampio di topi per porre una domanda mirata: disattivare un singolo gene chiamato PERM1, noto per aiutare le cellule cardiache nella produzione di energia, modifica anche la forza con cui il cuore si contrae? Scansionando con cura i cuori di oltre 170 topi, mostrano che questo gene rimodella sottilmente il cuore e ne riduce la forza di pompaggio, mentre gli animali rimangono in gran parte apparentemente sani. I loro risultati aiutano a risolvere un dibattito nel campo e offrono una guida per progettare esperimenti cardiaci migliori in futuro.
Un gene che collega l’uso del carburante alla forza di contrazione
PERM1 è stato identificato per la prima volta come un interruttore che aumenta la produzione di energia nelle cellule muscolari, incluso il cuore. Lavori precedenti avevano mostrato che i livelli di PERM1 diminuiscono nei cuori in insufficienza sia nei topi sia negli esseri umani, sollevando la possibilità che bassi livelli di PERM1 possano contribuire a battiti cardiaci più deboli. Ma studi su topi privi di PERM1 — animali ingegnerizzati per non avere il gene — avevano prodotto risposte contrastanti sul fatto che i loro cuori pompassero davvero meno efficacemente. Poiché PERM1 è considerato un possibile bersaglio per nuove terapie dell’insufficienza cardiaca, gli autori hanno deciso di testarene l’impatto sulla funzione cardiaca con un numero sufficiente di animali e una statistica rigorosa per ottenere una risposta chiara sì/no.
Uno sguardo su larga scala a cuori piccoli
Il team ha raccolto dati ecocardiografici — la stessa tecnica a ultrasuoni usata nelle cliniche cardiologiche — da ogni topo privo di PERM1 e dal suo fratello sano impiegati nel loro laboratorio in un periodo di 18 mesi. Questa raccolta retrospettiva ha prodotto 84 animali normali (wild-type) e 88 knockout, una dimensione del campione molto più ampia del tipico negli studi cardiaci murini. Dalle immagini ecografiche hanno misurato indicatori standard di funzionamento del ventricolo sinistro, la principale camera di pompaggio. Il numero chiave è stato la frazione di eiezione, la percentuale di sangue espulsa a ogni battito, insieme a misure correlate come quanto si riduce il diametro del ventricolo durante la contrazione, lo spessore delle pareti e la quantità totale di sangue pompata al minuto.
Contrazione più debole, camera più ampia, portata simile
I risultati mostrano uno schema coerente. In media, la frazione di eiezione è scesa da circa il 65% nei topi normali al 54% nei knockout PERM1, una differenza sufficientemente ampia da avere rilevanza clinica negli esseri umani e supportata da statistiche molto robuste. Altre misure di contrazione, come il frazionale di accorciamento e l’ispessimento delle pareti, sono calate anch’esse. Allo stesso tempo, i ventricoli sinistri dei knockout erano visibilmente più grandi, soprattutto alla fine della contrazione, indicando che nella camera rimaneva più sangue. Nonostante questa contrazione più debole, la quantità totale di sangue pompata al minuto è diminuita solo leggermente — di circa il 6% — perché le camere ingrandite potevano contenere più sangue inizialmente. In altre parole, il cuore ha compensato parzialmente la cattiva contrazione dilatando la sua camera principale.
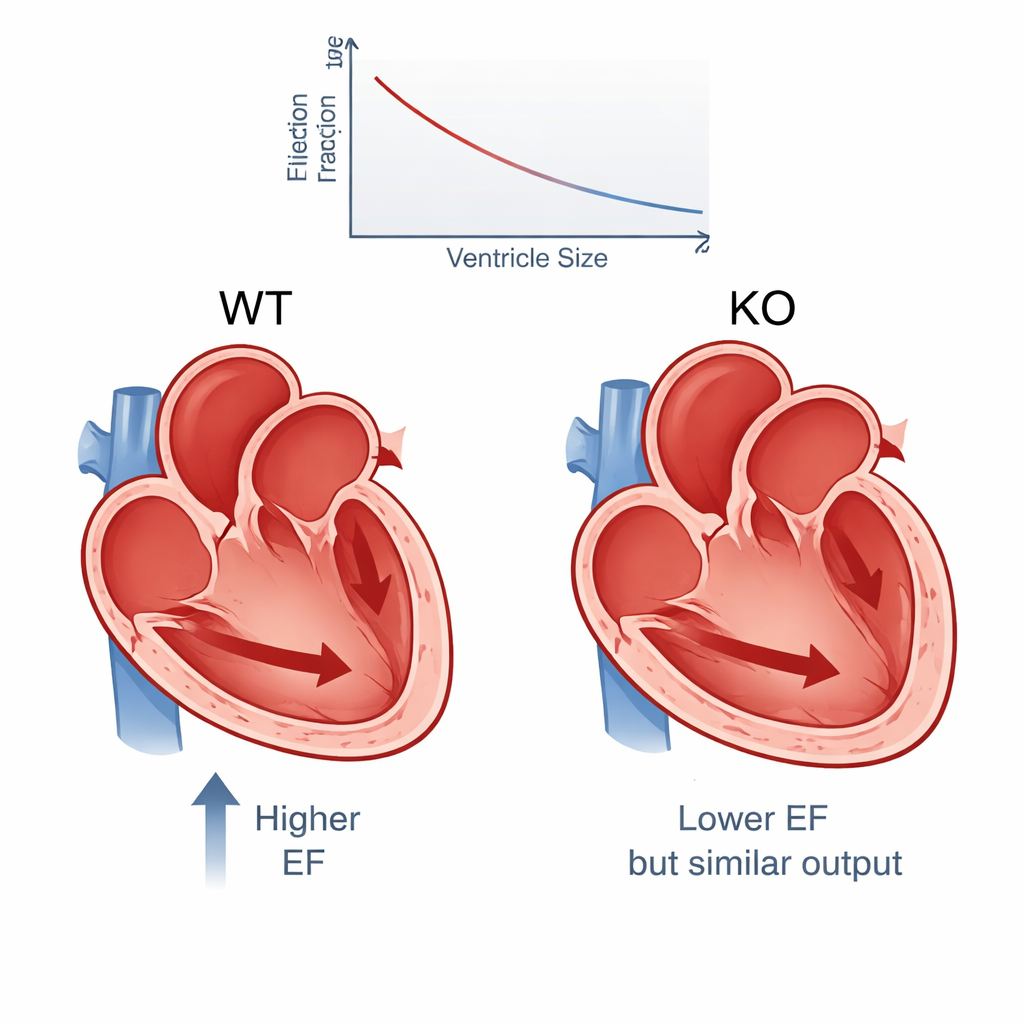
Una diversità nascosta in cuori “identici”
Poiché lo studio includeva così tanti animali, i ricercatori hanno potuto guardare oltre le medie e studiare come variano i singoli cuori. Anche tra topi sani geneticamente identici hanno osservato una sorprendente ampiezza nella distribuzione della frazione di eiezione. L’eliminazione di PERM1 ha spostato verso il basso l’intera distribuzione — più cuori con forza di pompaggio inferiore — ma non ha reso la dispersione stessa più ampia. Circa il 7% dei topi knockout aveva una frazione di eiezione inferiore al 40%, un livello che negli esseri umani corrisponderebbe a insufficienza cardiaca con ridotta frazione di eiezione, eppure questi topi mantenevano ancora una portata sanguigna quasi normale. Le analisi statistiche hanno mostrato che sesso, età e peso corporeo spiegavano solo una piccola parte della variabilità; la maggior parte delle differenze probabilmente deriva da fattori biologici più difficili da misurare, come influenze ambientali sottili o cambiamenti epigenetici.
Cosa significa per la ricerca cardiaca futura
Per aiutare altri scienziati a progettare esperimenti migliori, gli autori hanno utilizzato il loro ampio set di dati per calcolare quante cavie sono tipicamente necessarie per rilevare cambiamenti significativi in ciascun parametro cardiaco. Hanno scoperto che le dimensioni dei gruppi modeste spesso usate nel campo possono facilmente non individuare effetti reali ma moderati, specialmente per misure sottili come il volume di gittata sistolica o la portata cardiaca. Complessivamente, lo studio fornisce solide prove che la perdita di PERM1 provoca una rimodellamento specifico del cuore — camere più grandi, contrazione più debole — piuttosto che un vero e proprio collasso funzionale, e che questo rimodellamento è in parte bilanciato da cambiamenti strutturali che aiutano a preservare il flusso ematico. Per i non specialisti, il messaggio è che un singolo gene che regola l’energia può spingere il cuore verso una nuova modalità di funzionamento, che dall’esterno sembra sana ma comporta cambiamenti più silenziosi nella struttura della pompa e nella sua fatica di lavoro.
Citazione: Zaitsev, A.V., Sreedevi, K., Goode, B. et al. Analysis of systolic cardiac function in PERM1-knockout mice using large cohorts of animals. Sci Rep 16, 7705 (2026). https://doi.org/10.1038/s41598-026-37420-2
Parole chiave: insufficienza cardiaca, contrattilità cardiaca, energetica mitocondriale, modelli murini, ecocardiografia