Clear Sky Science · it
Identificazione e caratterizzazione di biomarcatori correlati ai fibroblasti e sottopopolazioni pro-infiammatorie nella parodontite mediante analisi trascrittomica integrata e a singola cellula
Perché le tue gengive contano oltre il sorriso
Gengive sanguinanti e denti mobili possono sembrare problemi minori, ma la malattia gengivale cronica—nota come parodontite—può danneggiare l’osso mascellare, causare la perdita dei denti ed è associata a condizioni come malattie cardiache e diabete. Questo studio esamina da vicino un gruppo di cellule delle gengive solitamente trascurato, i fibroblasti, per capire come contribuiscono ad accendere o modulare l’infiammazione. Combinando grandi dataset genetici con l’analisi a singola cellula, i ricercatori scoprono nuovi segnali di allarme e tipi cellulari che potrebbero migliorare la diagnosi e il trattamento delle malattie gengivali.
Attori nascosti nelle gengive doloranti
I fibroblasti sono le cellule operative che costruiscono e mantengono il tessuto connettivo che tiene i denti in posizione. Per anni sono stati visti principalmente come una “impalcatura” strutturale. Questa ricerca mostra che sono molto di più: i fibroblasti possono funzionare come piccoli centri di controllo dell’infiammazione. Quando i batteri alterano l’equilibrio microbico normale della bocca, i fibroblasti rispondono rilasciando messaggeri chimici che attraggono cellule immunitarie e possono sia favorire la riparazione dei tessuti sia intensificare il danno. Gli autori si sono concentrati sull’individuare segnali genici correlati ai fibroblasti che differiscono tra gengive sane e parodontite, e nel riconoscere sottogruppi di fibroblasti che diventano particolarmente pro-infiammatori nel tessuto malato.
Analisi della flora gengivale cellula per cellula
Per farlo, il team ha esplorato diversi grandi set di dati di espressione genica provenienti da pazienti con gengive sane e con parodontite, insieme a un dataset moderno di sequenziamento a singola cellula che profila migliaia di singole cellule. Hanno prima mappato i principali tipi cellulari nel tessuto gengivale—come cellule immunitarie, cellule vascolari e fibroblasti—e hanno confermato che il numero e l’attività dei fibroblasti erano maggiori nelle gengive malate. Hanno poi cercato geni che fossero sia alterati nella parodontite sia specificamente associati ai fibroblasti. Usando un metodo statistico che restringe le caratteristiche più informative, hanno individuato sei geni chiave correlati ai fibroblasti il cui schema combinato di attività distingueva in modo affidabile la parodontite dalla salute attraverso diversi gruppi di pazienti.
Pattern di rischio e “personalità” immunitarie della malattia gengivale
Con questi sei geni, i ricercatori hanno costruito un modello diagnostico che si è comportato bene nel separare i campioni malati da quelli sani, e lo hanno tradotto in una semplice tabella di punteggio—chiamata nomogramma—che, in linea di principio, potrebbe stimare il rischio individuale. Quando hanno raggruppato i pazienti in base all’intensità di espressione di questi geni dei fibroblasti, sono emerse tre forme distinte di parodontite. Una forma mostrava un paesaggio immunitario altamente infiammatorio, ricco di cellule T aggressive e macrofagi in “modalità d’attacco”. Una seconda forma era dominata da cellule che attenuano le risposte immunitarie, suggerendo un ambiente più soppressivo. Una terza forma si collocava in mezzo, con una miscela più equilibrata o a riposo di cellule immunitarie. Questi schemi suggeriscono che non tutta la malattia gengivale è uguale—e che i fibroblasti contribuiscono a plasmare queste diverse “personalità” dell’infiammazione.
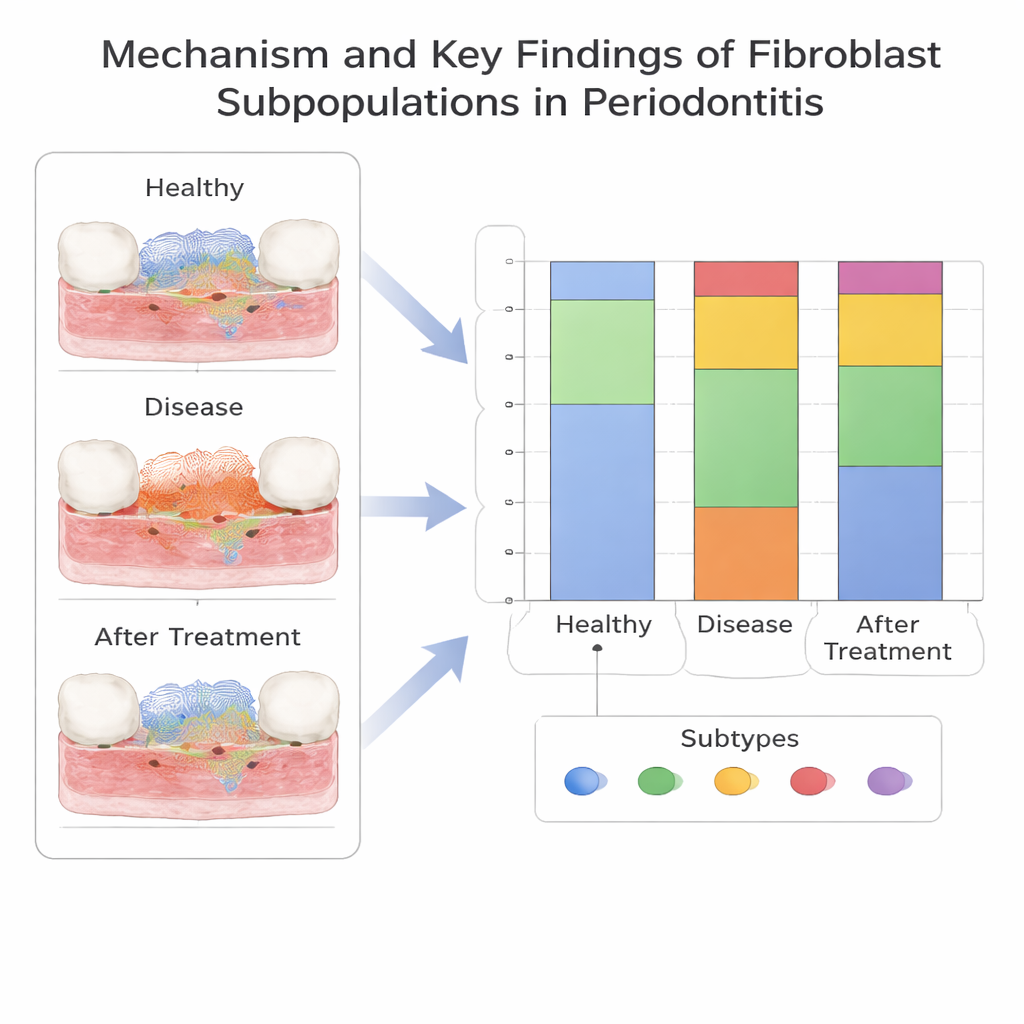
Un nuovo sottotipo di fibroblasto pro-infiammatorio
Approfondendo a livello di singola cellula, il team ha diviso i fibroblasti in cinque sottotipi basati sulla loro attività genica. Un sottotipo, caratterizzato da un gene chiamato CXCL13, si è distinto perché era molto più comune nella parodontite rispetto alle gengive sane. Questo gruppo di fibroblasti CXCL13-positivi appariva precocemente lungo un percorso di sviluppo ed era associato a segnali che attraggono cellule immunitarie e rimodellano la matrice tissutale—caratteristiche coerenti con un forte ruolo pro-infiammatorio. Al contrario, un altro sottotipo di fibroblasti era arricchito nei tessuti sani e potrebbe contribuire a mantenere stabile l’ambiente gengivale. Gli autori hanno confermato nei campioni di pazienti che alcuni geni correlati ai fibroblasti, in particolare SELL, e gli stessi fibroblasti CXCL13-positivi, erano effettivamente più elevati nelle gengive malate, rafforzando i riscontri computazionali.
Cosa significa per la cura delle gengive in futuro
In termini semplici, lo studio rivela che alcuni fibroblasti nelle gengive si comportano come acceleratori dell’infiammazione, mentre altri possono agire più come freni o squadre di riparazione. Identificando marcatori genici precisi e un distinto sottogruppo di fibroblasti pro-infiammatori, il lavoro apre la strada a test più accurati che segnalino la parodontite prima e con maggiore affidabilità. Suggerisce inoltre che i trattamenti futuri potrebbero mirare a queste vie specifiche guidate dai fibroblasti—attenuando i sottogruppi dannosi come i fibroblasti CXCL13-positivi o potenziando quelli protettivi—per controllare meglio l’infiammazione gengivale e possibilmente ridurne l’impatto sulla salute sistemica.
Citazione: Huang, M., Lin, Y., Wu, Z. et al. Identification and characterization of fibroblast-related biomarkers and pro-inflammatory subpopulations in periodontitis by integrated transcriptomic and single-cell analysis. Sci Rep 16, 6223 (2026). https://doi.org/10.1038/s41598-026-37385-2
Parole chiave: parodontite, fibroblasti, infiammazione gengivale, sequenziamento RNA a singola cellula, biomarcatori