Clear Sky Science · it
Apoptosi efficiente tramite rotture a doppio filamento del DNA in cellule epiteliali umane indotta da un effetto non termico di onde terahertz a banda larga ad alto campo
Una nuova luce sull’eliminazione delle cellule tumorali
I trattamenti anticancro spesso procedono su una linea sottile: devono distruggere le cellule tumorali senza danneggiare gravemente i tessuti sani o il sistema immunitario. Questo studio esplora uno strumento insolito per questo compito—impulsi terahertz (THz) intensi, una forma di luce invisibile tra le microonde e l’infrarosso. I ricercatori mostrano che impulsi THz a banda larga e ad alto campo, opportunamente tarati, possono indurre le cellule tumorali a compiere un “suicidio” controllato, senza cuocere il tessuto o provocare la morte cellulare disordinata che conduce all’infiammazione.
Perché la morte cellulare ‘gentile’ conta
Molte terapie antitumorali spingono le cellule verso la morte, ma spesso lo fanno con danni collaterali. Farmaci e agenti biologici possono perdere efficacia man mano che i tumori sviluppano resistenza e possono indebolire il sistema immunitario. Metodi fisici come raggi X, radioattività o ablazione termica possono danneggiare il tessuto sano circostante, causando frequentemente necrosi—una forma violenta di morte cellulare che scatena infiammazione e dolore. Un metodo che invece induca apoptosi, un processo ordinato di autodistruzione in cui la cellula si smonta silenziosamente, potrebbe offrire un modo molto meno traumatico per ridurre i tumori, specialmente quelli superficiali o vicini alla pelle.
Onde terahertz e cellule del tumore al seno
Il team si è concentrato su cellule umane di carcinoma mammario (MCF‑7), un tipo di cellula epiteliale spesso usato negli studi in vitro. Hanno esposto queste cellule a impulsi THz pulsati, a banda larga e di intensità molto elevata, per periodi fino a quattro ore mantenendole a temperatura corporea normale. I campi elettrici hanno raggiunto diverse decine di milioni di volt per centimetro, valori molto superiori a quelli dei dispositivi di uso quotidiano. In queste condizioni, la frazione di cellule che entravano in apoptosi aumentava costantemente con il tempo di esposizione. Con l’intensità THz massima testata, quasi il 99% delle cellule tumorali ha attivato l’apoptosi, mentre meno dell’1% è morto per necrosi. Questa massiccia e pulita ondata di morte cellulare programmata suggerisce che gli impulsi THz agiscano in modo diverso dal semplice riscaldamento delle cellule.
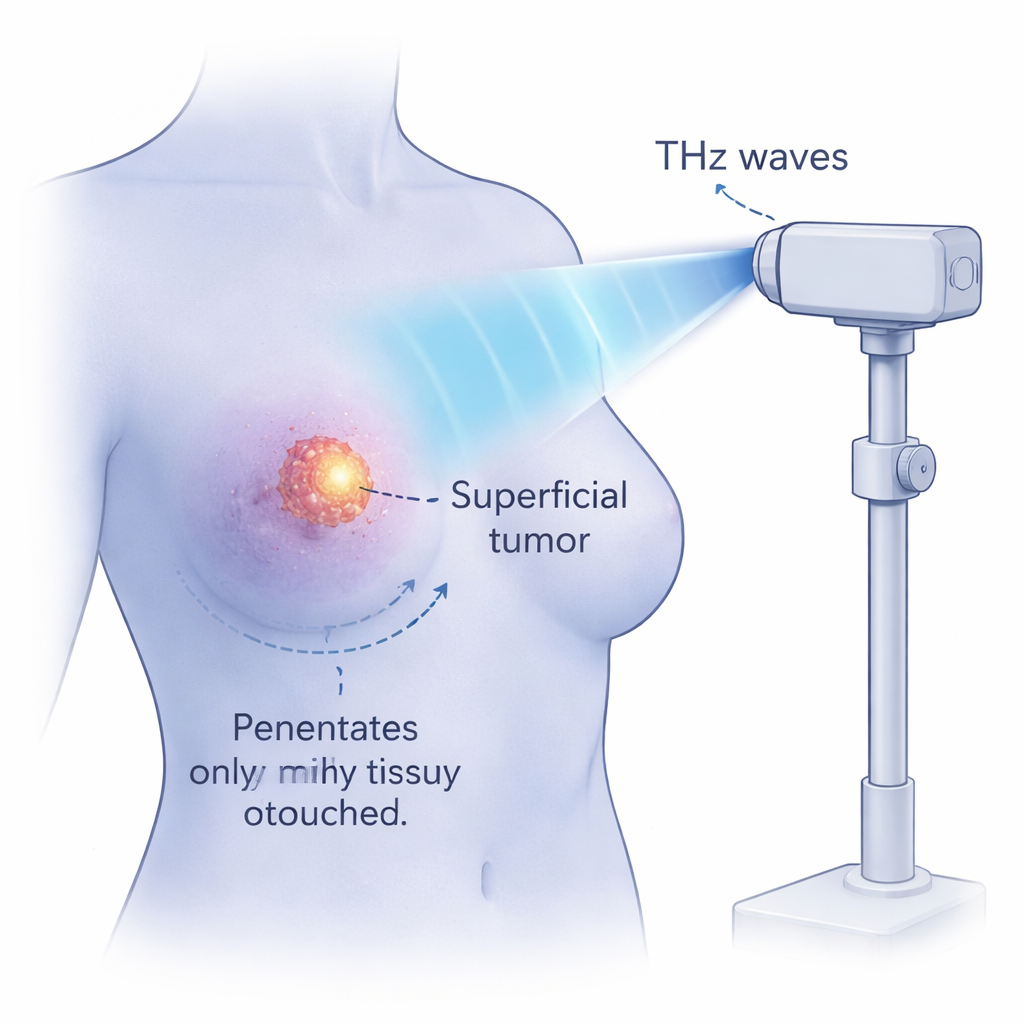
Effetti non termici e limiti di sicurezza della temperatura
Poiché l’acqua assorbe fortemente la radiazione THz, la preoccupazione ovvia è il riscaldamento accidentale. Gli scienziati hanno utilizzato l’imaging termico per monitorare le variazioni di temperatura durante l’irradiazione. Anche dopo quattro ore a intensità moderate, le cellule tumorali si sono riscaldate di circa 3 °C e la necrosi è rimasta sotto il 4%. Esperimenti di controllo in cui le cellule sono state semplicemente riscaldate per quattro ore hanno mostrato che temperature inferiori a 41 °C producono quasi nessuna morte, mentre un aumento netto della necrosi si osserva oltre i 43 °C. Anche con le impostazioni THz più intense, i ricercatori hanno mantenuto le temperature cellulari a o sotto la soglia di 43 °C e hanno comunque osservato quasi totale apoptosi con necrosi minima. Abbassando la frequenza di ripetizione degli impulsi hanno dimostrato che la temperatura può essere mantenuta sotto controllo pur conservando forti effetti antitumorali, sottolineando che è in gioco un meccanismo non termico.
Scuotere il DNA e attivare i geni della morte
Per identificare quel meccanismo, il gruppo ha osservato l’interno delle cellule. Al microscopio elettronico, le cellule trattate con THz mostravano segni classici di apoptosi precoce: materiale genetico condensato, nuclei alterati e membrane esterne intatte. Usando un marcatore fluorescente chiamato γ‑H2AX, hanno rilevato estese rotture a doppio filamento del DNA—danni molto più frequenti nelle cellule irradiate rispetto ai controlli non trattati o leggermente riscaldati. Il pattern del danno seguiva il profilo di intensità del fascio THz, diventando più marcato verso il centro. Analisi di geni e proteine hanno mostrato che un insieme di molecole rispondenti a stress e danno, come GADD45B e c‑Jun, erano fortemente attivate, mentre protagonisti noti delle vie tradizionali di morte cellulare, tra cui p53 e molte caspasi, non variavano significativamente. Gli autori propongono che campi THz intensi possano indurre violente “risonanze” vibratorie nel DNA, sollecitando fisicamente e rompendo il doppio elica e quindi attivando un percorso apoptotico distinto, indipendente da p53 e caspasi.
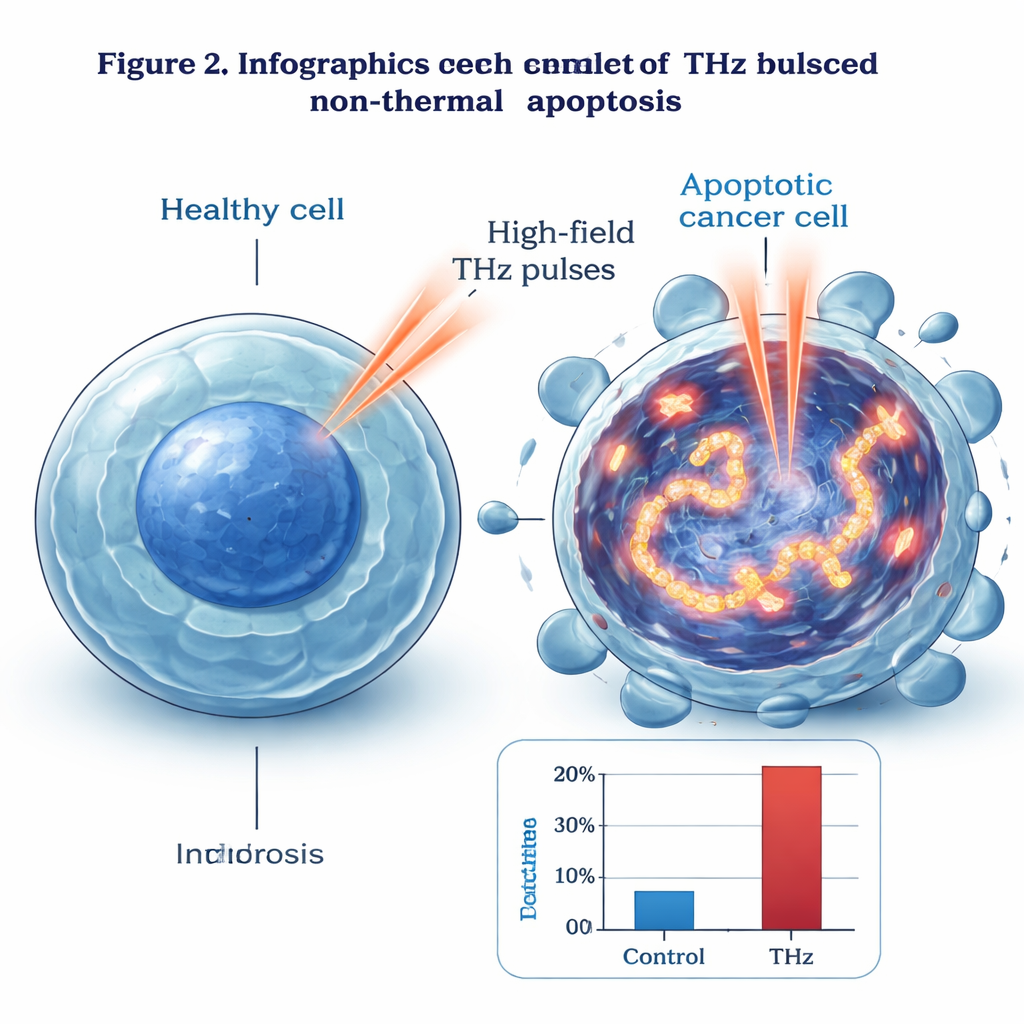
Dal piatto di laboratorio alle terapie future
Sebbene questi esperimenti siano stati condotti in colture cellulari, suggeriscono un nuovo approccio fisico alla terapia del cancro. Le onde THz ad alto campo sembrano in grado di penetrare per diversi millimetri in tessuto umido—sufficiente a raggiungere tumori superficiali—pur attenuandosi rapidamente, risparmiando potenzialmente gli organi più profondi. Poiché l’effetto è principalmente non termico, in linea di principio potrebbe eliminare le cellule tumorali strato per strato senza bruciare il tessuto circostante o provocare intensa infiammazione. Rimane molto lavoro: il meccanismo di “risonanza” del DNA proposto deve essere confermato, la sicurezza per le cellule normali richiede valutazioni approfondite e sono necessari studi su animali e clinici. Tuttavia, questa ricerca apre la strada all’idea che impulsi di luce ingegnerizzati con cura, sintonizzati sui moti naturali delle biomolecole, possano un giorno offrire un modo preciso e relativamente delicato per ablare alcuni tipi di cancro.
Citazione: Zhou, H., Wei, X., Peng, XY. et al. Efficient apoptosis via double-strand breaks of DNA in human epithelial cells induced by non-thermal effect of high-field broadband terahertz waves. Sci Rep 16, 6163 (2026). https://doi.org/10.1038/s41598-026-37373-6
Parole chiave: terapia antitumorale con terahertz, apoptosi non termica, rotture a doppio filamento del DNA, cellule del tumore al seno, ablazione fisica del tumore