Clear Sky Science · it
Modelli generalizzati di vasi sanguigni per oncologia basata su nanoparticelle magnetiche: proprietà geometriche e microfluidiche
Guidare minuscoli magneti attraverso il corpo
Immaginate di poter attirare i farmaci antitumorali direttamente all'interno di un tumore usando un magnete, risparmiando al resto del corpo gli effetti collaterali più aggressivi. Questo studio esplora come particelle magnetiche di piccola dimensione si muovono all'interno di reti che simulano i vasi sanguigni e pone una domanda apparentemente semplice: in condizioni di flusso realistiche, i magneti riescono davvero a indirizzare queste particelle dove i medici desiderano?
Perché la geometria dei vasi e il flusso contano
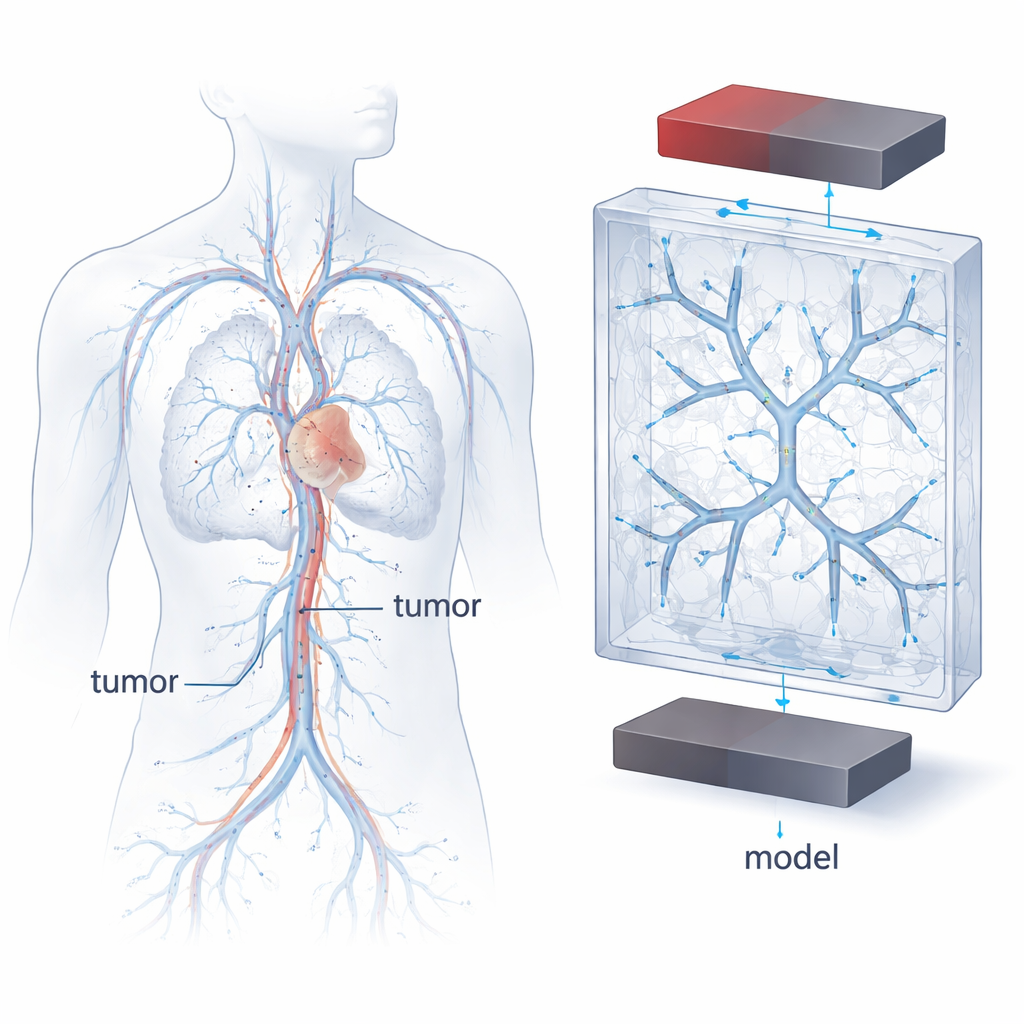
Le terapie magnetiche contro il cancro si basano su nanoparticelle di ossido di ferro superparamagnetico — SPION — che possono essere attratte da un campo magnetico mentre trasportano farmaci nel flusso sanguigno. Ma i vasi non sono tubi rettilinei semplici: si diramano, si restringono, curvano e si dividono, e la velocità del sangue accelera o rallenta in risposta. Questi cambiamenti di forma e di velocità influenzano il modo in cui le particelle si muovono, dove si concentrano e se rimangono a contatto con le pareti abbastanza a lungo da aderire. I vasi dei pazienti reali variano enormemente, il che rende difficile confrontare esperimenti o prevedere il comportamento di una nuova terapia. Gli autori hanno quindi deciso di costruire una “vascolarizzazione modello” altamente controllata e ripetibile che catturasse comunque le caratteristiche essenziali dei vasi che alimentano i tumori.
Costruire reti vascolari tumorali idealizzate
Per progettare questi vasi modello, il team si è basato su regole classiche che descrivono come si ramificano le arterie reali. Una di queste regole, la legge di Murray, collega i diametri dei vasi genitore e dei vasi figli in una rete efficiente dal punto di vista energetico. Utilizzando misurazioni cliniche tratte da tumori mammari e queste leggi di scala, i ricercatori hanno generato matematicamente alberi ramificati che imitano il restringersi dei vasi che alimentano il tumore verso il letto capillare. Hanno poi impiegato la stampa 3D ad alta risoluzione per incorporare reti di canali cavi con due, tre o quattro livelli di diramazione all'interno di blocchi di plastica trasparente. I canali seguivano un modello di ramificazione simmetrico ed estendevano in tre dimensioni, offrendo un paesaggio semplificato ma ispirato alla fisiologia in cui studiare il moto delle particelle.
Osservare le particelle magnetiche in azione
Attraverso queste reti stampate, il team ha pompato acqua come sostituto del sangue, quindi ha iniettato a monte un fluido contenente SPION e applicato un campo magnetico statico attorno al modello. Riprese ad alta velocità hanno fornito un resoconto in stile filmato di come le nubi scure di particelle attraversavano i diversi rami, mentre l'analisi al computer ha convertito le variazioni di luminosità in segnali temporali che riflettono la presenza locale di particelle. Variando la portata di flusso di fondo, la concentrazione di particelle, la complessità delle diramazioni e la presenza o assenza del magnete, i ricercatori hanno potuto distinguere come ciascun fattore modellasse la distribuzione delle particelle, il tempo di permanenza e la deposizione finale sulle pareti dei canali.
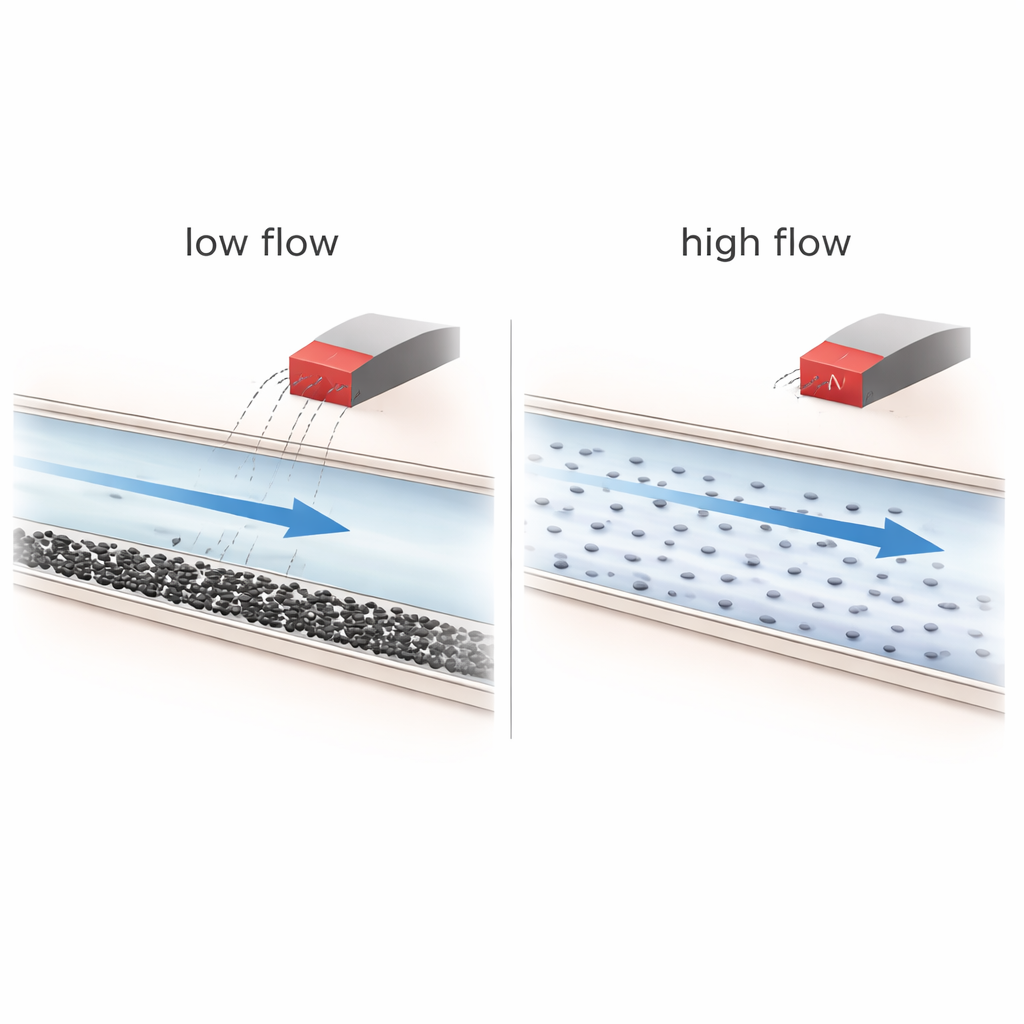
Quando i magneti aiutano — e quando non lo fanno
Gli esperimenti rivelano che sono le condizioni di flusso a dominare la situazione. A velocità di flusso più elevate, il fluido risulta ben miscelato e le nanoparticelle viaggiano rapidamente; in queste condizioni il campo magnetico ha quasi nessuna influenza e le particelle seguono semplicemente le linee di flusso attraverso la rete. A basse velocità di flusso, invece, la gravità e gli effetti di concentrazione fanno sì che le particelle tendano a depositarsi verso il fondo dei canali, formando strati stratificati e talvolta aggregati lassi. In questa situazione già irregolare, il magnete può spingere un numero maggiore di particelle verso certi rami e prolungarne leggermente la permanenza, in particolare in reti più complesse e altamente ramificate. Tuttavia i calcoli mostrano che la forza magnetica su una singola particella di 40 nanometri è molti ordini di grandezza più debole della resistenza viscosa del liquido in movimento, rendendo fisicamente irrealistico il «pilotaggio» di singole particelle nelle condizioni testate.
Cosa significa questo per le terapie oncologiche future
Per un non specialista, il punto principale è che i magneti da soli non possono estrarre in modo affidabile nanoparticelle libere da un flusso sanguigno rapido. Piuttosto, effetti magnetici evidenti emergono solo quando le particelle si sono già rallentate, depositate o aggregate — situazioni che aumentano effettivamente la loro risposta magnetica. I modelli vascolari generalizzati e stampati in 3D presentati qui forniscono un modo standardizzato per esplorare tali effetti attraverso diverse geometrie di rete e regimi di flusso. Per il futuro del targeting magnetico dei farmaci, questo lavoro suggerisce che le strategie di successo dovranno probabilmente sfruttare comportamenti collettivi — come aggregazione controllata o sistemi vettore — piuttosto che fare affidamento sullo steering di nanoparticelle isolate attraverso vasi grandi e rapidamente perfusi.
Citazione: Fleischhauer, D., Schlicht, S. & Drummer, D. Generalized blood vessel models for magnetic nanoparticle-based oncology: geometric and microfluidic properties. Sci Rep 16, 3701 (2026). https://doi.org/10.1038/s41598-026-37348-7
Parole chiave: targeting magnetico dei farmaci, nanoparticelle, vascolarizzazione tumorale, modelli microfluidici, somministrazione di farmaci