Clear Sky Science · it
Mirare l’asse Akt–EphA2 e l’adesione cellula–cellula aumenta la sensibilità all’anoikis nelle cellule tumorali
Perché le cellule tumorali libere in sospensione sono importanti
Quando le cellule tumorali si staccano da un tumore e viaggiano attraverso il flusso sanguigno, dovrebbero normalmente morire perché perdono l’ancoraggio al tessuto circostante. Questo programma di sicurezza intrinseco, chiamato morte cellulare indotta dal distacco, aiuta a impedire che tessuti crescano dove non dovrebbero. Le cellule tumorali metastatiche, tuttavia, spesso imparano a ignorare questo segnale e rimangono vive mentre fluttuano, facilitando la formazione di nuovi focolai tumorali. Questo studio pone una domanda apparentemente semplice: se ripristiniamo un importante “senso del tatto” meccanico in cellule di carcinoma mammario aggressive, possiamo costringere queste cellule vaganti a morire e, se no, quali stratagemmi di riserva usano per sopravvivere?
Ririscaldare un senso del tatto perduto
Le cellule testano continuamente quanto è rigido l’ambiente circostante, tirando sulle strutture che le ancorano. Nei tessuti sani, perdere il contatto o atterrare su una superficie molto morbida tende a innescare l’autodistruzione. La proteina Tropomyosin 2.1 (Tpm2.1) è una parte importante di questa macchina di tensione interna ed è spesso assente o ridotta nelle cellule tumorali. I ricercatori hanno usato una linea cellulare di carcinoma mammario metastatico ampiamente studiata e l’hanno ingegnerizzata per produrne più Tpm2.1, ripristinando gran parte di questa capacità di percezione della rigidità. Quando queste cellule modificate sono state costrette a crescere in piastre antiaderenti speciali che impediscono l’attacco, hanno effettivamente mostrato più morte cellulare, una crescita più lenta e una ridotta motilità rispetto alle cellule tumorali non modificate. Eppure, anche dopo diversi giorni in sospensione, circa il 70% delle cellule che esprimevano Tpm2.1 era ancora vivo, suggerendo che il risveglio del loro senso del tatto da solo non risolve completamente il problema.
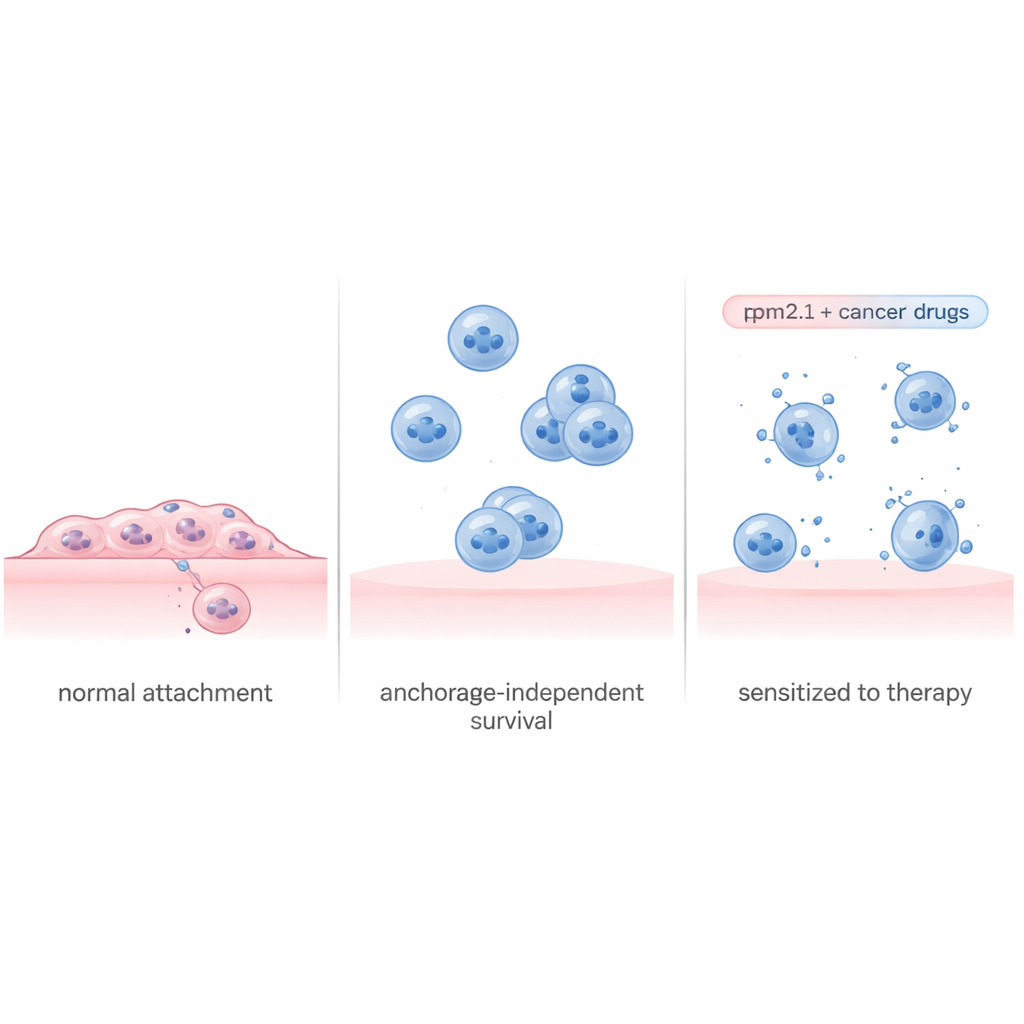
Leggere il manuale di sopravvivenza delle cellule tumorali
Per capire perché alcune cellule morivano mentre altre sopravvivevano, il team ha separato le cellule fluttuanti che esprimevano Tpm2.1 in due gruppi: quelle che mostravano segni precoci di morte cellulare e quelle che apparivano sane. Hanno quindi misurato quali geni erano attivati o spenti in ciascun gruppo nell’arco di quattro giorni. Le cellule morenti mostravano una vasta inattivazione di programmi coinvolti nella divisione cellulare, nella riparazione del DNA e nell’adesione, insieme a segnali di stress che somigliavano a una strada a senso unico verso l’autodistruzione. Al contrario, le cellule sopravvissute hanno attivato un piano coordinato di sopravvivenza. Nelle fasi iniziali dopo il distacco hanno acceso vie infiammatorie e correlate al sistema immunitario e successivamente hanno aumentato circuiti principali di crescita e sopravvivenza, inclusa una via ben nota incentrata sulla proteina Akt. Allo stesso tempo, hanno fortemente potenziato geni che favoriscono l’adesione cellula–cellula, permettendo loro di formare aggregati protettivi anche senza ancorarsi alla matrice circostante.
Forza nel numero: come i cluster cellulari resistono alla morte
Poiché i dati genici indicavano un aumento dell’adesione cellula–cellula, i ricercatori hanno verificato se il semplice assembramento potesse aiutare le cellule a sopravvivere in sospensione. Quando le cellule che esprimevano Tpm2.1 sono state coltivate ad alta densità, dove il clustering era facilitato, molte meno cellule sono morte rispetto a quando sono state mantenute a bassa densità. Una molecola di adesione, ICAM1, è risultata particolarmente elevata nelle cellule sopravvissute ed è già nota per favorire la formazione di cluster di cellule tumorali circolanti e il loro insediamento in tessuti distanti. Bloccare ICAM1 con un inibitore a piccola molecola ha aumentato la morte delle cellule che esprimevano Tpm2.1 in sospensione, mentre ha avuto scarso effetto sulle colture tradizionalmente aderenti. Questi risultati supportano l’idea che, una volta che la loro meccanica interna è parzialmente ripristinata, le cellule tumorali possano comunque sfuggire alla morte aggrappandosi letteralmente l’una all’altra anziché all’ambiente.
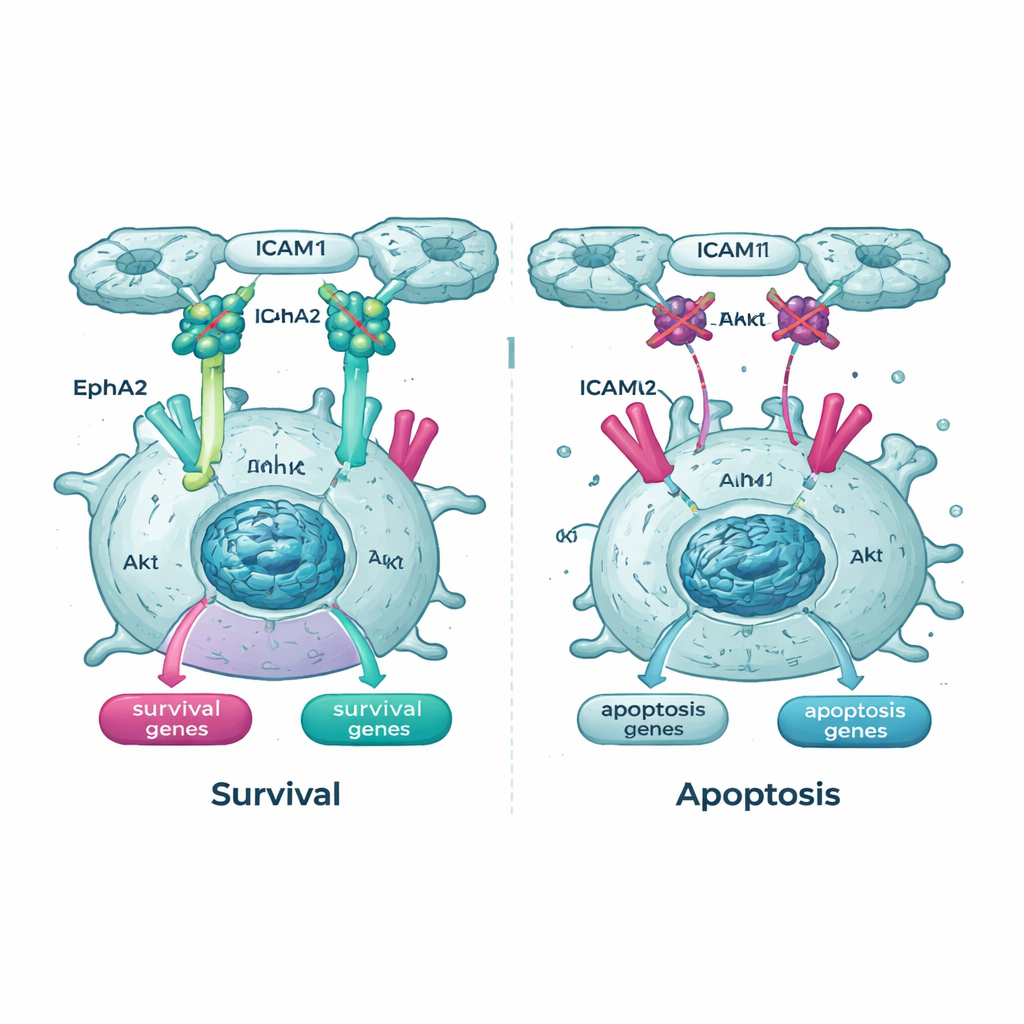
Recidere linee vitali chiave all’interno della cellula
Le analisi genetiche hanno anche messo in evidenza la via Akt e uno dei suoi partner, un recettore chiamato EphA2, come linee vitali importanti per le cellule tumorali in sospensione. Nelle cellule che esprimevano Tpm2.1, la forma attiva e fosforilata di Akt era più bassa in sospensione rispetto alle cellule di controllo, e anche i livelli e l’attività di EphA2 risultavano ridotti. Quando il team ha trattato le cellule con farmaci che bloccano Akt o EphA2, sia le cellule tumorali standard sia quelle che esprimevano Tpm2.1 sono diventate molto più propense a morire in sospensione. È importante notare che le cellule con il senso di rigidità restaurato erano particolarmente sensibili a questi farmaci nel tempo, il che implica che una volta che i loro controlli meccanici di sicurezza sono parzialmente riattivati, dipendono in misura maggiore dai segnali di sopravvivenza rimanenti.
Trasformare uno stato «pronto» in una debolezza letale
Per un non specialista, il messaggio chiave è che riparare un interruttore di sicurezza guasto nelle cellule tumorali—la loro capacità di sentire e rispondere alla perdita di contatto—è necessario ma non sufficiente per indurle all’autodistruzione. Le cellule che sopravvivono lo fanno raggruppandosi e ricollegando i loro circuiti interni attraverso vie alternative di crescita e sopravvivenza. Questo lavoro mostra che il ripristino della sensibilità alla rigidità con Tpm2.1 mette le cellule di carcinoma mammario metastatico in uno stato «pronto», in cui sono più vicine alla morte ma non ancora compromesse. Bloccare successivamente la via Akt–EphA2 e disturbare l’adesione cellula–cellula tramite ICAM1 consente ai ricercatori di spingere queste cellule «pronte» oltre il limite e aumentare notevolmente la morte indotta dal distacco. In termini pratici, lo studio delinea una strategia per future terapie combinate volte a eliminare le cellule tumorali libere in sospensione prima che possano impiantare nuove metastasi.
Citazione: Vivante, A.G., Dwivedi, N., Sheetz, M.P. et al. Targeting the Akt–EphA2 axis and cell–cell adhesion enhances anoikis sensitivity in cancer cells. Sci Rep 16, 6197 (2026). https://doi.org/10.1038/s41598-026-37327-y
Parole chiave: metastasi del tumore al seno, adesione cellulare, anoikis, segnalizzazione Akt, sensibilità alla rigidità