Clear Sky Science · it
TRMT6 attenua la suscettibilità e la progressione della colite indotta da DSS in modo multifattoriale tramite la regolazione della traduzione
Perché questo studio sull’intestino è importante
La malattia infiammatoria intestinale (MII) – che comprende il morbo di Crohn e la colite ulcerosa – colpisce milioni di persone nel mondo e può provocare dolore cronico, sanguinamento, perdita di peso e affaticamento. Al centro di queste condizioni c’è un rivestimento intestinale fragile, spesso un singolo strato di cellule, che deve continuamente ripararsi pur trattenendo trilioni di microbi. Questo studio rivela un «custode» molecolare finora sottovalutato, una proteina chiamata TRMT6, che aiuta le cellule intestinali a crescere, guarire e gestire il loro metabolismo. Comprendere come funziona TRMT6 potrebbe aprire nuove strade a terapie più mirate e meno invasive per la MII.
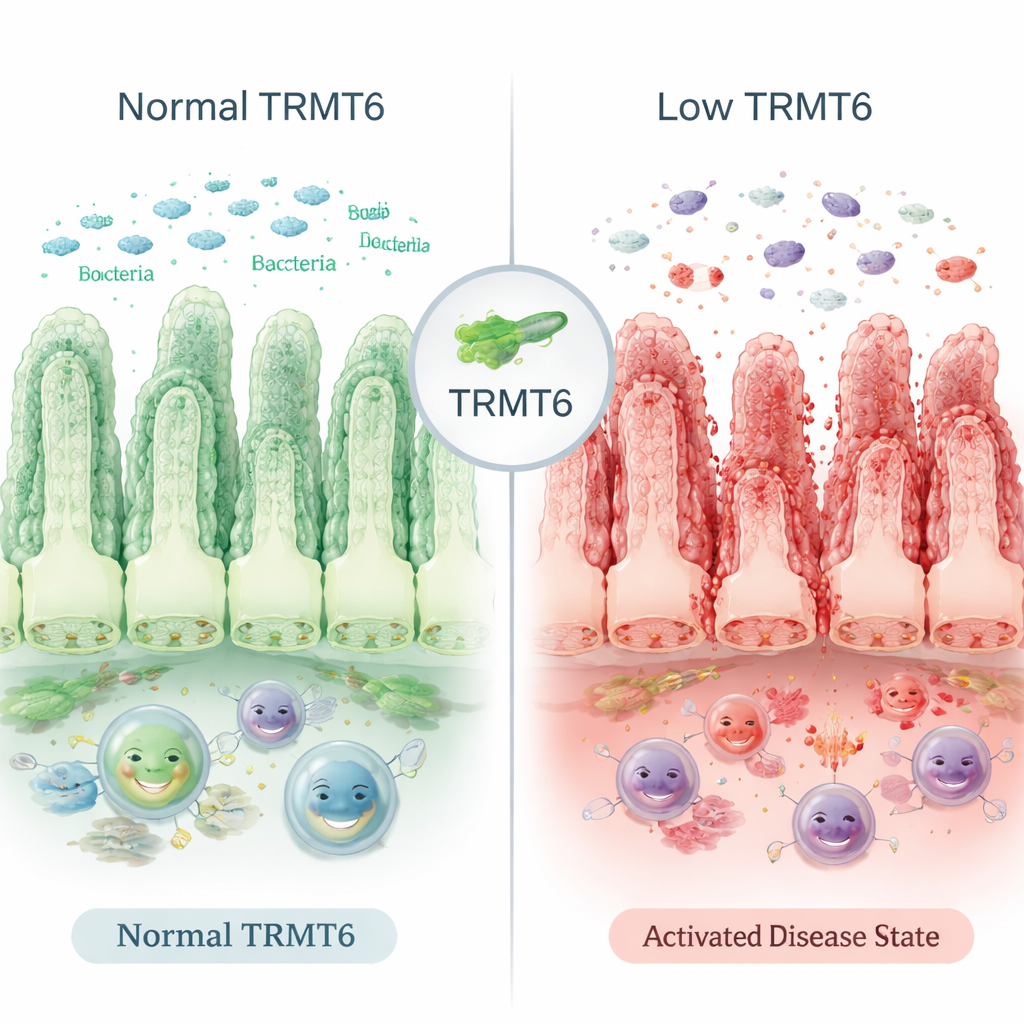
Un guardiano microscopico della parete intestinale
La superficie interna dell’intestino è rivestita da un singolo strato di cellule che si rinnova ogni pochi giorni. Questo tappeto vivente funge da barriera, separando i batteri intestinali dai tessuti interni del corpo. I ricercatori hanno osservato che TRMT6, un enzima presente in queste cellule intestinali, è ridotto nei campioni di tessuto prelevati da persone con MII attiva e nei topi con colite indotta chimicamente. TRMT6 non altera la sequenza del DNA; invece modifica in modo sottile l’RNA – le copie operative dell’informazione genetica che guidano la produzione proteica – in modi che influenzano l’efficienza con cui le proteine vengono sintetizzate. Quando i livelli di TRMT6 diminuiscono, questo processo di produzione proteica si indebolisce e il rivestimento intestinale diventa più vulnerabile ai danni.
Cosa succede quando TRMT6 viene spento
Per valutare l’importanza di TRMT6, il gruppo ha creato topi in cui TRMT6 è stato eliminato specificamente nelle cellule dell’intestino tenue. In condizioni normali, questi animali apparivano sani e gli intestini sembravano in gran parte normali all’esame microscopico. Tuttavia, quando i topi sono stati esposti a una sostanza chimica (DSS) che irrita l’intestino e viene largamente usata come modello di colite, il quadro è cambiato drasticamente. Rispetto ai loro consanguinei normali, i topi privi di TRMT6 hanno mostrato una maggiore perdita di peso, coloni più corti e più gonfi, e lesioni più profonde nell’intestino tenue. Un secondo modello genetico che rimuoveva TRMT6 solo dalle cellule staminali intestinali – le cellule che rimpiazzano continuamente il rivestimento – ha prodotto una malattia altrettanto grave, confermando che l’enzima è particolarmente critico in questo compartimento rigenerativo.
Riparazione rallentata, metabolismo alterato e microbi scomposti
Un’analisi più ravvicinata del tessuto intestinale ha rivelato perché l’assenza di TRMT6 è così dannosa durante la colite. Nell’intestino danneggiato si osservavano più cellule in via di morte programmata e meno cellule in divisione attiva, come mostrato dalle colorazioni istologiche standard. Un regolatore chiave della crescita, la proteina MYC, risultava marcatamente ridotta a livello proteico, anche se il suo messaggero RNA era diminuito solo modestamente. Questo disallineamento suggerisce che TRMT6 aiuta le cellule intestinali a tradurre efficientemente l’RNA di MYC in proteina, permettendo una rapida riparazione del rivestimento. Per approfondire, i ricercatori hanno combinato misure su larga scala di RNA, proteine, piccole molecole (metaboliti) e DNA batterico. Queste analisi «multi‑omiche» hanno mostrato che la perdita di TRMT6 altera proteine coinvolte nel trattamento dei grassi e nell’assorbimento dei nutrienti, modifica i livelli di numerosi lipidi e acidi organici nell’intestino e nel sangue, e sposta l’equilibrio della comunità microbica intestinale, riducendo gruppi benefici a favore di specie più associate all’infiammazione.
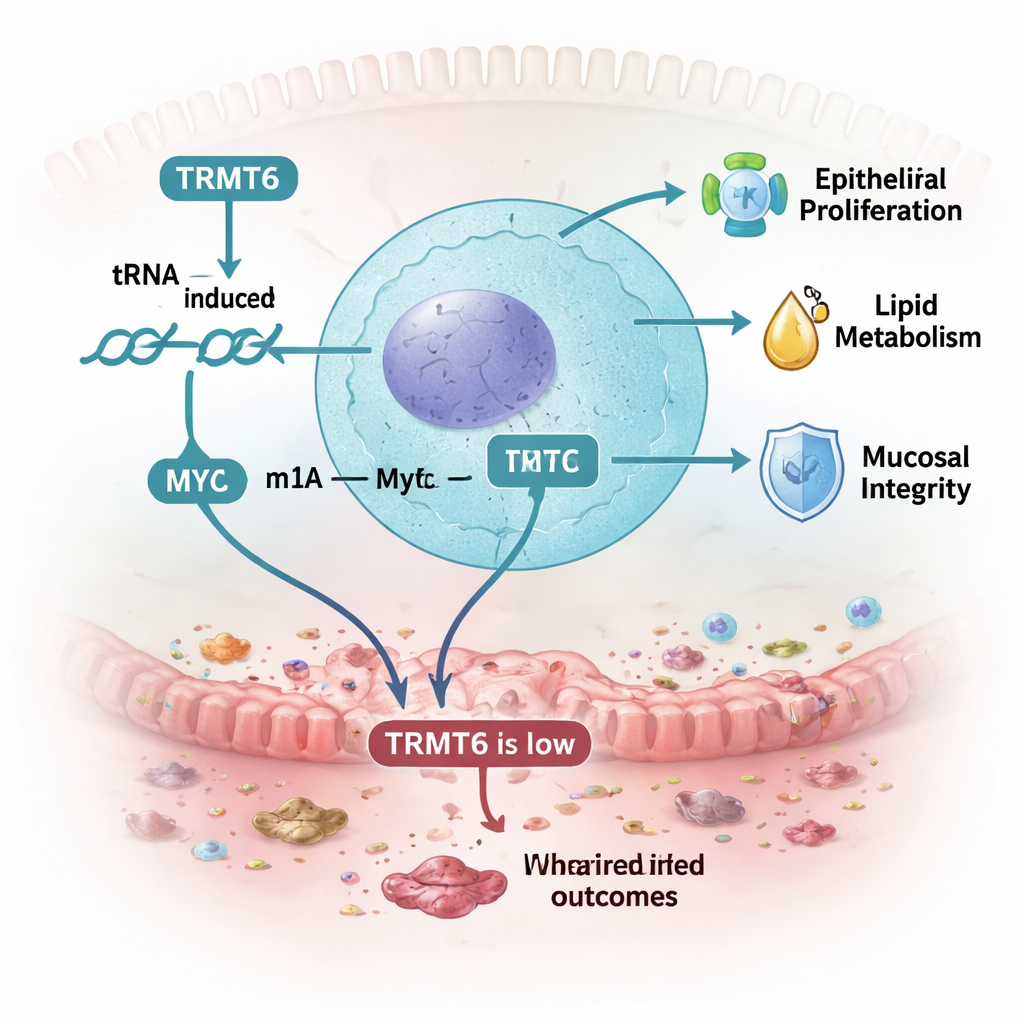
Un snodo molecolare che collega barriera, metabolismo e infiammazione
Nel complesso, i risultati ritraggono TRMT6 come un hub centrale che aiuta il rivestimento intestinale a far fronte allo stress. Regolando finemente una specifica modificazione chimica sul transfer RNA, TRMT6 sostiene la produzione di MYC e di altre proteine che guidano il rinnovamento cellulare, regolano il metabolismo lipidico e mantengono una tenuta efficace tra il corpo e i microbi residenti. Quando TRMT6 è assente o ridotto, la parete intestinale si ripara più lentamente, assorbe i nutrienti meno efficacemente e favorisce condizioni che avvantaggiano una comunità microbica più dannosa. Sotto la pressione aggiuntiva di un trigger infiammatorio, queste debolezze si traducono in una colite più grave nei topi, riecheggiando la riduzione di TRMT6 osservata nei tessuti umani con MII.
Cosa potrebbe significare per i trattamenti futuri
Per chi non è specialista, il messaggio chiave è che la MII non è soltanto un problema del sistema immunitario; deriva anche da disfunzioni nella gestione quotidiana delle cellule intestinali. TRMT6 emerge come uno degli strumenti cellulari che mantengono l’equilibrio tra produzione proteica, metabolismo e riparazione della barriera. Sebbene questa ricerca sia ancora in fase precoce e preclinica, suggerisce che potenziare delicatamente l’attività di TRMT6, o mimare i suoi effetti sull’RNA e sulla sintesi proteica, potrebbe un giorno contribuire a rafforzare il rivestimento intestinale e a calmare l’infiammazione nelle persone con MII. Serviranno studi più ampi in diversi modelli di malattia e su campioni di pazienti, ma questo lavoro indica un nuovo e più preciso punto di intervento per affrontare l’infiammazione intestinale cronica.
Citazione: Zhang, X., Du, Y., Ye, Y. et al. TRMT6 mitigates susceptibility and progression of DSS-induced colitis multifacetedly via translational regulation. Sci Rep 16, 6809 (2026). https://doi.org/10.1038/s41598-026-37299-z
Parole chiave: malattia infiammatoria intestinale, barriera intestinale, modifica dell'RNA, microbioma intestinale, metabolismo intestinale