Clear Sky Science · it
Impatto della microbiota definita Oligo-MM12 sulla colonizzazione intestinale e la disseminazione di Listeria monocytogenes
Perché i microrganismi nel tuo intestino contano
Molti conoscono Listeria monocytogenes come un pericoloso microrganismo trasmesso dagli alimenti, associato a cibi pronti contaminati e a malattie gravi in individui vulnerabili. Meno evidente è invece che la capacità di questo batterio di impiantarsi nell’organismo dipende non solo dal nostro sistema immunitario, ma anche dalla vivace comunità di microrganismi che già vive nell’intestino. Questo studio utilizza modelli murini appositamente progettati e un piccolo “colon artificiale” per porsi una domanda semplice ma importante: come influisce la complessità del microbioma intestinale sulla capacità di Listeria di colonizzare l’intestino e diffondersi nell’organismo?
La storia di due quartieri microbici
Per affrontare la domanda, i ricercatori hanno confrontato due tipi di topi. Un gruppo, chiamato topi SPF, ospitava un ricco mix naturale di batteri intestinali simile a quello presente in molti animali da laboratorio. L’altro gruppo, i topi Oligo-MM12, supportava una comunità molto più semplice composta da sole 12 ceppi batterici ben caratterizzati. Poiché ogni membro di questa comunità è noto e stabile attraverso le generazioni, i topi Oligo-MM12 sono uno strumento potente per analizzare quali microbi aiutano a bloccare gli invasori e quali potrebbero lasciare lacune nelle nostre difese. Contrastando questi modelli, il team ha potuto testare come un ecosistema intestinale denso e diversificato differisca da uno snello e minimalista nel gestire una sfida infettiva.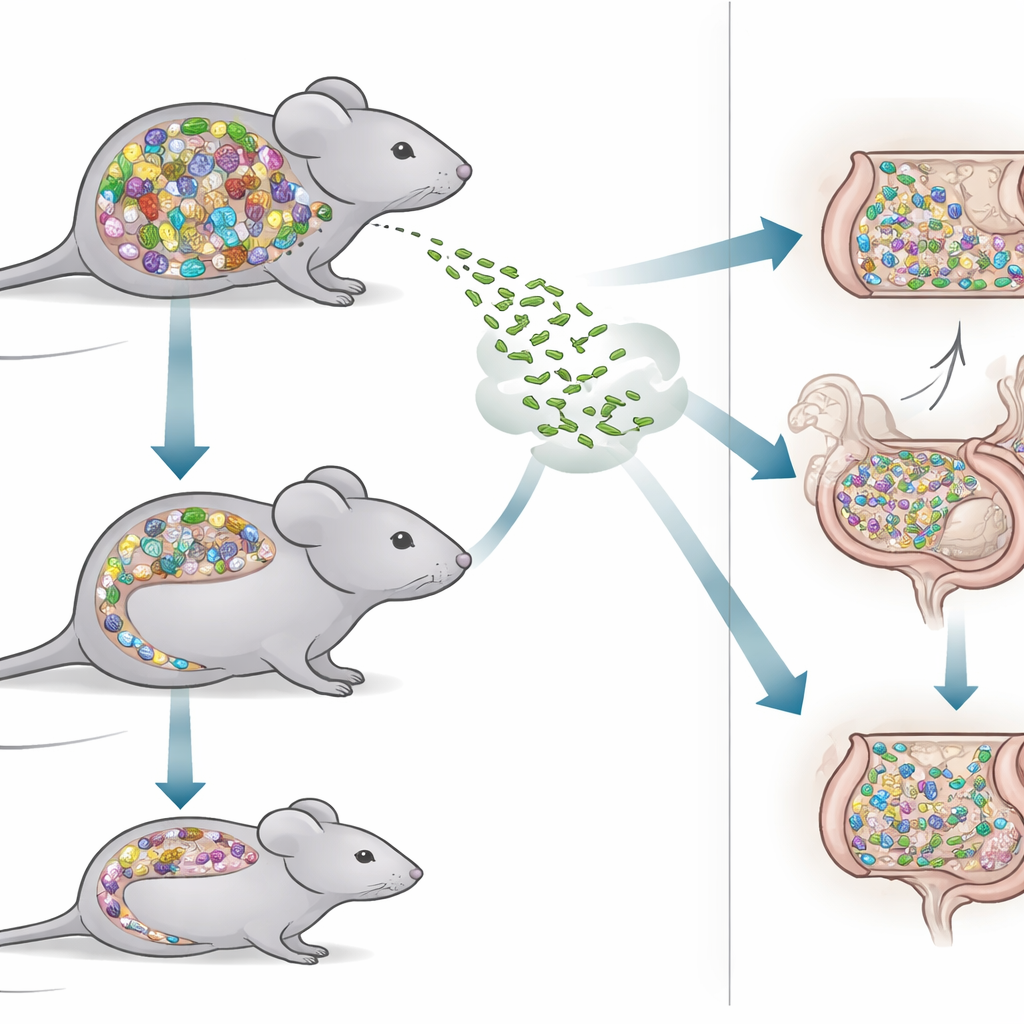
Seguire Listeria attraverso l’intestino e oltre
Gli scienziati hanno infettato entrambi i tipi di topo con la stessa dose orale di Listeria e hanno monitorato quante cellule batteriche comparivano nelle feci e negli organi interni per tre giorni. Interessante, la più semplice comunità Oligo-MM12 sembrava inizialmente più efficace a tenere Listeria sotto controllo: nel primo giorno dopo l’infezione questi topi espellevano meno cellule di Listeria nelle feci rispetto ai topi SPF. Tuttavia, questo vantaggio iniziale è svanito. Al terzo giorno, i topi Oligo-MM12 mostravano una maggiore eliminazione di Listeria, mentre i topi SPF avevano progressivamente ridotto i livelli. Nonostante queste differenze chiare nell’intestino, i numeri di Listeria negli organi interni come fegato, milza e linfonodi erano simili tra i due modelli murini, suggerendo che una volta che Listeria raggiunge i tessuti profondi la complessità del microbioma giochi un ruolo minore.
Simulare il colon in una scatola controllata
Per separare gli effetti dei tessuti ospite e dell’immunità dal comportamento dei microbi stessi, il team ha eseguito anche un esperimento ex vivo utilizzando un dispositivo chiamato bioreattore micro-Matrix. Hanno preparato sospensioni fecali da ciascun tipo di topo, le hanno aggiunte a un mezzo ricco di nutrienti in pozzetti sigillati e privi di ossigeno, e hanno introdotto Listeria in alcune di queste colture in miniatura lasciando altre come controlli. In cinque giorni hanno misurato il numero di Listeria e sequenziato il DNA batterico per seguire l’evoluzione delle comunità. In questo colon artificiale, Listeria è cresciuta a livelli simili indipendentemente dal confronto con la complessa microbiota SPF o con la più semplice comunità Oligo-MM12, e la sua presenza ha causato solo spostamenti modesti nella composizione complessiva delle comunità. Questo contrasto con gli animali vivi mette in evidenza quanto fortemente sistema immunitario, rivestimento intestinale e flussi di bile e muco plasmino l’infezione nell’intestino reale.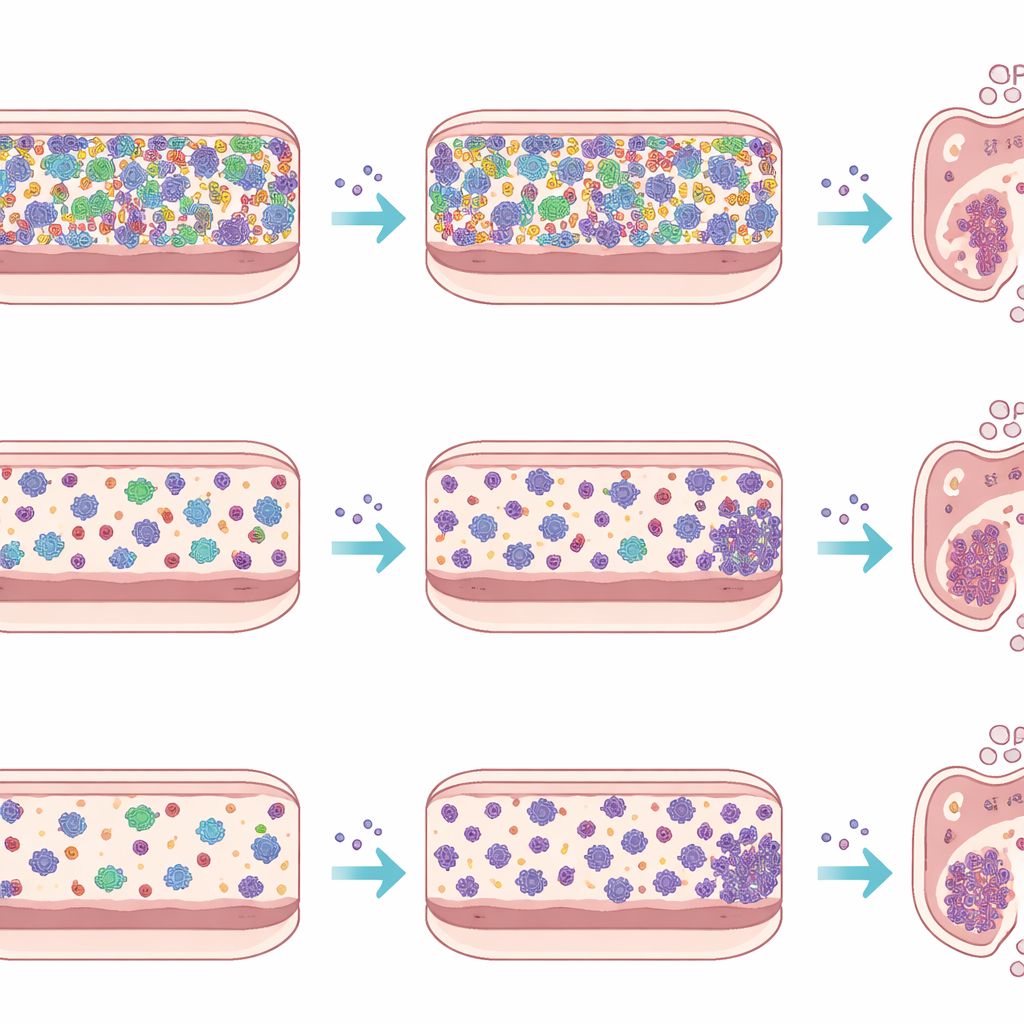
Vincitori, perdenti e spettatori microbici chiave
Analizzando quali gruppi batterici aumentavano o diminuivano durante l’infezione, lo studio individua candidati che possono influenzare il successo di Listeria. Nei topi Oligo-MM12, i livelli di Akkermansia, un batterio associato al muco spesso collegato alla salute intestinale, sono calati il secondo giorno per poi riprendersi fortemente al terzo giorno. Nei topi SPF, diversi generi noti per produrre metaboliti benefici o sostenere l’integrità della barriera, come Blautia e Bacteroides, sono diminuiti durante l’infezione, mentre alcuni batteri simili a Prevotella hanno mostrato aumenti e cali complessi che possono riflettere un bersaglio diretto dei composti antimicrobici prodotti da Listeria stessa. Ex vivo, questi schemi sono stati in gran parte attenuati, rafforzando l’idea che molti dei cambiamenti osservati derivino da interazioni a tre vie tra patogeno, microbi residenti e ambiente ospite piuttosto che da semplice competizione microbica.
Cosa significa per la protezione delle persone
Per i non specialisti, il messaggio centrale è che non tutti i microbiomi dall’aspetto sano proteggono dalle infezioni allo stesso modo, e che “più diversità” non è sempre meglio in ogni momento. La comunità semplificata Oligo-MM12 ha fornito una forte resistenza precoce a Listeria nell’intestino, ma nel tempo il microbioma più intricato degli SPF ha fatto un lavoro migliore nello eliminare l’invasore. Il lavoro mostra che modelli di microbiota a bassa complessità attentamente progettati, combinati con sistemi ex vivo controllabili, possono rivelare quali gruppi batterici e quali fattori ambientali sono cruciali per bloccare patogeni alimentari pericolosi. In ultima analisi, tali intuizioni potrebbero guidare probiotici mirati o terapie basate sul microbioma che rafforzino i giusti alleati microbici al momento opportuno per prevenire infezioni da Listeria gravi nei pazienti a rischio.
Citazione: Cazzaniga, M., Bra, K.K., Herzog, M.K.M. et al. Impact of the defined Oligo-MM12 microbiota on intestinal colonisation and dissemination of Listeria monocytogenes. Sci Rep 16, 8434 (2026). https://doi.org/10.1038/s41598-026-37294-4
Parole chiave: Infezione da Listeria, microbioma intestinale, resistenza alla colonizzazione, modello murino, probiotici