Clear Sky Science · it
Analisi integrata dei regolatori globali e dei geni di efflusso associati alla inversione della resistenza antimicrobica in Klebsiella pneumoniae multiresistente
Perché questi germi ospedalieri sono così difficili da uccidere
Negli ospedali di tutto il mondo, alcuni ceppi del batterio Klebsiella pneumoniae sono diventati notoriamente difficili da curare. Resistono a molti antibiotici che una volta funzionavano in modo affidabile, trasformando infezioni di routine in emergenze potenzialmente letali. Questo studio indaga il motore microbico per comprendere un trucco importante che questi batteri utilizzano: pompe microscopiche che espellono gli antibiotici dalla cellula e gli interruttori genetici che sembrano aumentare o diminuire l’attività di queste pompe.
Superbatteri e le loro vie di fuga molecolari
La Klebsiella pneumoniae multiresistente è ormai riscontrata in molti ospedali, incluso il centro medico iracheno dove è stata condotta questa ricerca. Questi batteri possono sopravvivere a diversi grandi gruppi di antibiotici contemporaneamente, come i fluorochinoloni, gli aminoglicosidi e le cefalosporine di terza generazione. Un modo in cui lo fanno è installare potenti “pompe di efflusso” nella loro membrana cellulare. Tra le più importanti c’è un sistema chiamato AcrAB‑TolC, che attraversa le membrane batteriche e funziona come una piccola pompa di sentina, afferrando le molecole di antibiotico all’interno della cellula e respingendole all’esterno prima che i farmaci possano causare danni seri. Quando queste pompe sono molto attive, la concentrazione di antibiotico all’interno del batterio non raggiunge mai livelli letali.
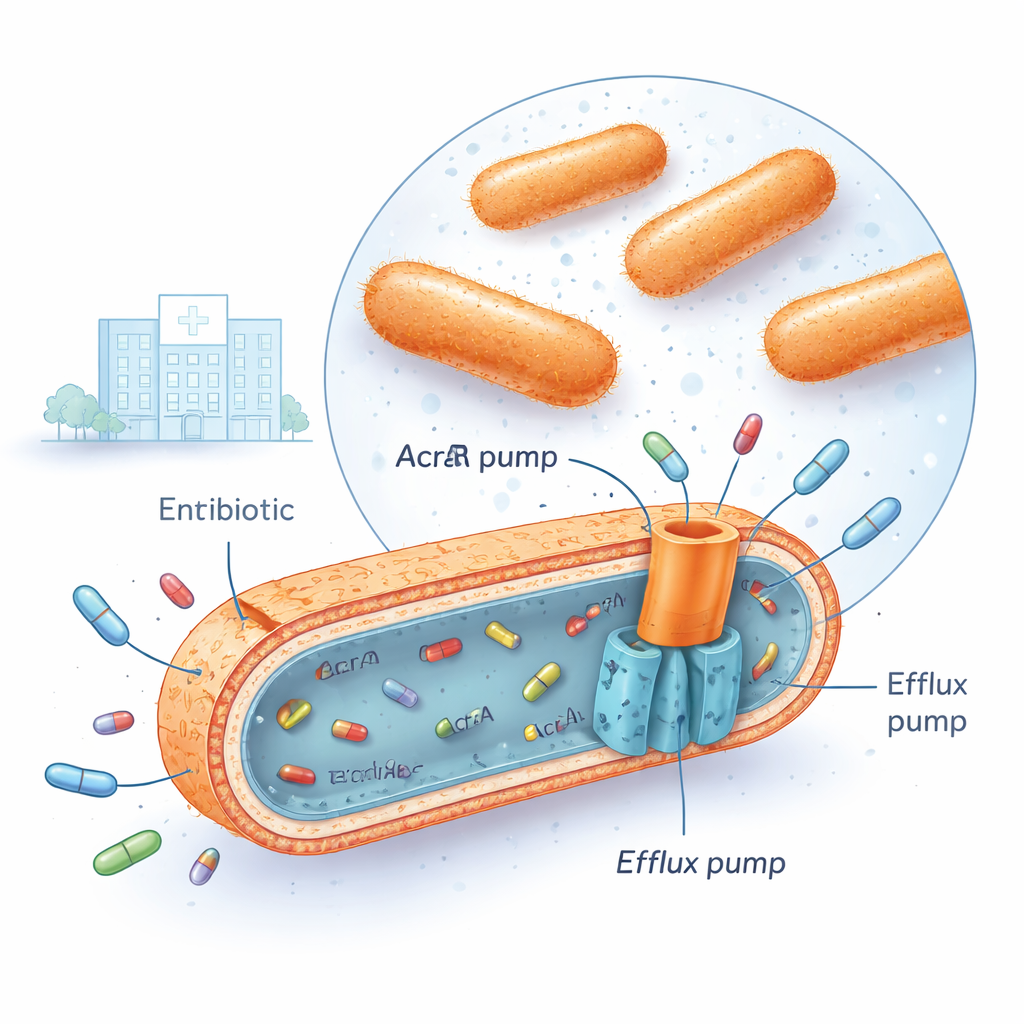
Interruttori genici che accompagnano la sovraattivazione delle pompe
I ricercatori hanno raccolto 30 isolati clinici multiresistenti di Klebsiella pneumoniae e li hanno confrontati con 10 isolati sensibili agli antibiotici e un ceppo di riferimento standard. Utilizzando una tecnica chiamata PCR quantitativa in tempo reale, hanno misurato quanto alcuni geni fossero espressi. Si sono concentrati su tre “regolatori globali”—i geni denominati marA, soxS e rob—insieme alle tre componenti della pompa AcrAB‑TolC stessa (acrA, acrB e tolC). Nei ceppi resistenti, due regolatori, marA e soxS, risultavano tipicamente sovraespressi di circa quattro‑cinque volte rispetto ai batteri sensibili, mentre acrB, un componente centrale della pompa, era aumentato quasi di otto volte. L’analisi statistica ha mostrato che quando i livelli di marA e soxS erano alti, anche i livelli di acrB tendevano a essere elevati, e quei ceppi sopportavano dosi molto più alte di antibiotici fluorochinolonici come la ciprofloxacina. Un terzo regolatore, rob, variava poco e non si allineava con l’attività della pompa, suggerendo che svolga un ruolo minore nelle condizioni testate.
Spegnere le pompe per indebolire la resistenza
Il fatto che i geni della pompa e dei regolatori siano attivi insieme è indicativo ma non sufficiente a dimostrare che siano la causa diretta della resistenza. Per verificare se le pompe fossero funzionalmente importanti, il gruppo ha utilizzato uno strumento chimico chiamato PAβN. Questo composto non è impiegato come farmaco nei pazienti, ma in laboratorio può ostruire pompe simili ad AcrAB‑TolC e impedirne l’espulsione degli antibiotici. Gli scienziati hanno scelto dieci isolati resistenti che mostravano livelli particolarmente alti del gene acrB e hanno misurato quanta ciprofloxacina fosse necessaria per arrestarne la crescita, con e senza PAβN. In otto di questi dieci ceppi, il blocco della pompa ha ridotto la dose di ciprofloxacina richiesta di almeno quattro volte, e talvolta fino a sedici volte. Questa riduzione dimostra che, in molti di questi superbatteri, pompe di efflusso attive sono effettivamente una ragione principale per la loro tolleranza a dosi elevate di antibiotico.
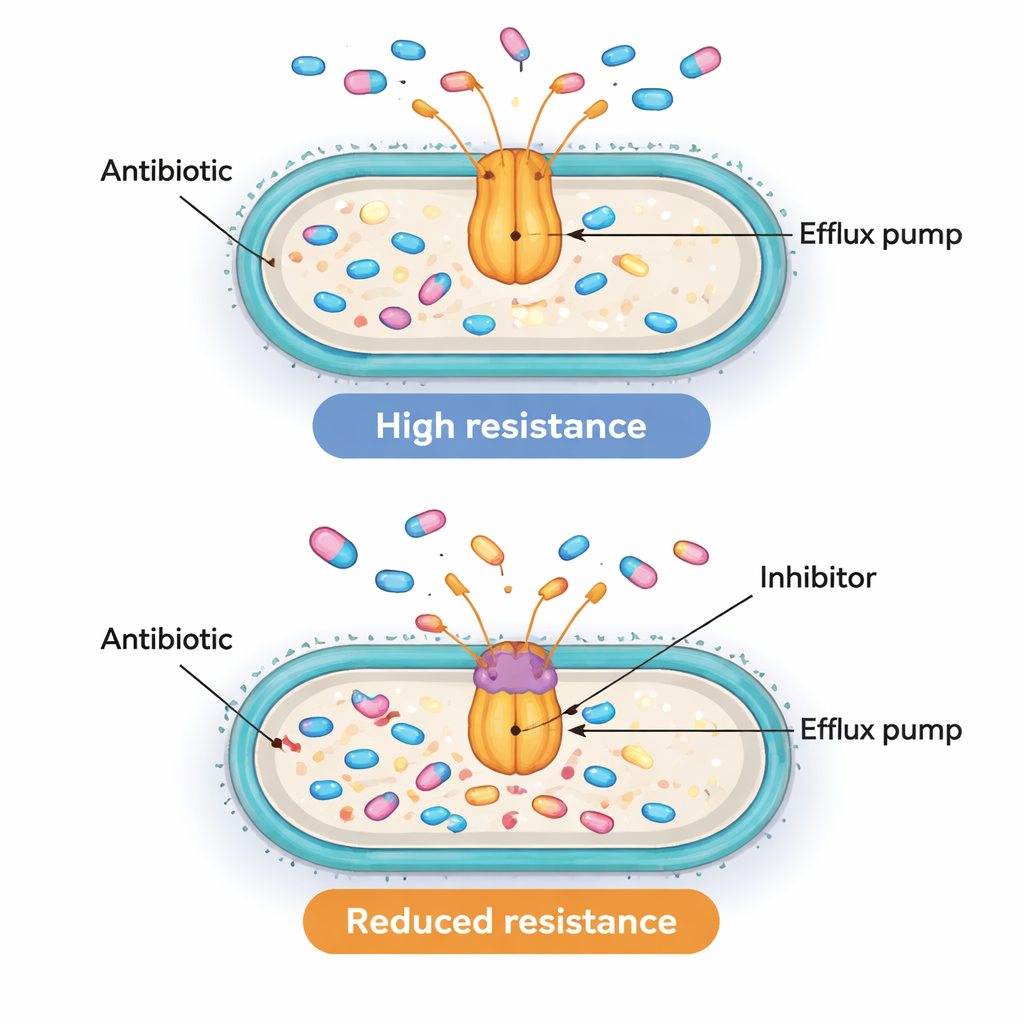
Un puzzle complesso della resistenza con bersagli promettenti
Non tutti i ceppi si comportavano allo stesso modo. Alcuni batteri con forte espressione dei geni della pompa hanno riacquistato sensibilità solo parzialmente quando le pompe sono state bloccate, implicando che altre vie di resistenza—come modifiche al bersaglio dell’antibiotico all’interno della cellula, produzione di enzimi che inattivano il farmaco o pompe alternative—contribuiscano anch’esse. La gentamicina, un antibiotico aminoglicosidico, per esempio, è rimasta in gran parte non influenzata dai modelli osservati nei geni marA/soxS e AcrAB‑TolC, sottolineando che la resistenza multidroga è generalmente costruita su diverse difese sovrapposte piuttosto che su un singolo meccanismo.
Cosa significa per i trattamenti futuri
Per chi non è specialista, il messaggio chiave è che alcuni batteri ospedalieri possono sopravvivere agli antibiotici non solo bloccando o degradando i farmaci, ma espellendoli attivamente. Questo studio collega una maggiore attività di due “interruttori” genici, MarA e SoxS, a pompe di efflusso più attive e a una resistenza più marcata a una classe di antibiotici ampiamente usata. Quando le pompe vengono sperimentalmente ostruite, molti di questi batteri diventano almeno parzialmente sensibili di nuovo. Pur non avendo ancora dimostrato esattamente come questi regolatori controllino le pompe, il lavoro evidenzia sia i regolatori sia le pompe come bersagli interessanti. A lungo termine, associare antibiotici convenzionali a inibitori sicuri delle pompe—or a farmaci che riducano l’attività di questi regolatori globali—potrebbe aiutare a ripristinare l’efficacia delle terapie esistenti contro infezioni multiresistenti altrimenti difficili da trattare.
Citazione: Obaid, A.J., Alkawaz, A.J. & Naser, M.S. Integrated analysis of global regulators and efflux genes associated with antimicrobial resistance reversal in multidrug resistant Klebsiella pneumoniae. Sci Rep 16, 7435 (2026). https://doi.org/10.1038/s41598-026-37272-w
Parole chiave: resistenza agli antibiotici, pompe di efflusso, Klebsiella pneumoniae, fluorochinoloni, inversione della resistenza