Clear Sky Science · it
La riduzione dell’enzima deubiquitinante USP10 si correla con l’apoptosi neuronale nella mielopatia associata a HTLV-1
Perché questo è importante per le persone che vivono con malattie virali del sistema nervoso
Alcuni virus non provocano solo infezioni di breve durata; possono danneggiare silenziosamente il sistema nervoso per molti anni. Il virus della leucemia a cellule T umano di tipo 1 (HTLV-1) è uno di questi e può portare a un disturbo cronico del midollo spinale chiamato mielopatia associata a HTLV-1 (HAM). Le persone con HAM perdono gradualmente forza e controllo delle gambe, insieme a problemi urinari e sensoriali. Questo studio pone una domanda semplice ma cruciale: perché i neuroni del midollo spinale muoiono in questa condizione, e potrebbe una singola molecola protettiva aiutare a spiegare chi sta meglio o peggio?
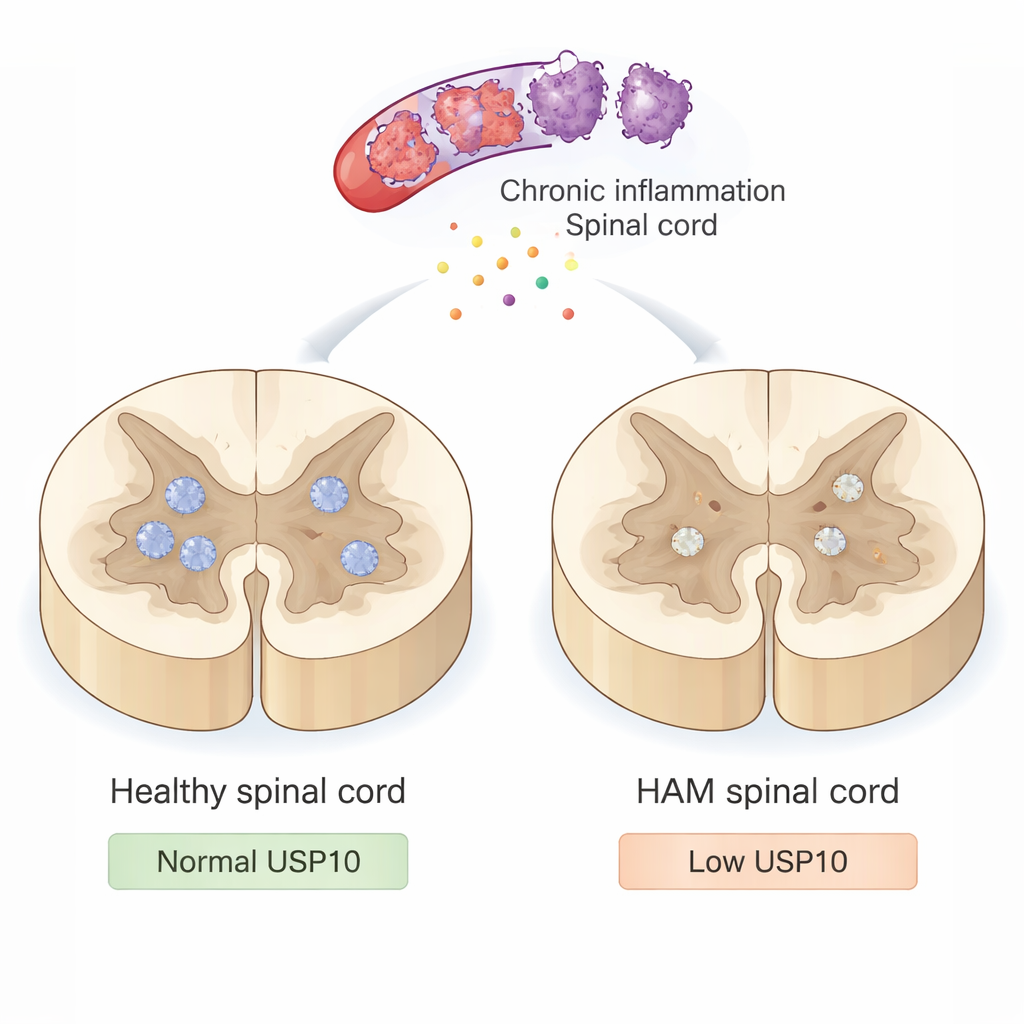
Un attacco lento al midollo spinale
La HAM non è causata dall’infezione diretta dei neuroni da parte del virus. Piuttosto, HTLV-1 infetta le cellule immunitarie che invadono il midollo spinale e scatenano un’infiammazione di lunga durata. Queste cellule immunitarie iperattive rilasciano sostanze tossiche e segnali infiammatori che, pur essendo intesi a controllare l’infezione, danneggiano anche i neuroni vicini e la loro mielina isolante. Col tempo questo assalto latente provoca gambe rigide e deboli e difficoltà nella deambulazione. Eppure i medici non comprendono ancora del tutto perché alcuni neuroni soccombono a questo ambiente infiammatorio mentre altri sopravvivono per decenni.
Un enzima cellulare di "pulizia" sotto sospetto
I ricercatori si sono concentrati su una proteina chiamata USP10, un enzima che aiuta a gestire il sistema di controllo della qualità delle proteine della cellula ed è noto per limitare lo stress cellulare e la morte cellulare programmata (apoptosi). USP10 è attivo in molti tessuti, incluso il cervello e il midollo spinale, e lavori precedenti nel morbo di Parkinson, nell’ictus e in altre condizioni suggeriscono che aiuti i neuroni a resistere al danno ossidativo e infiammatorio. Utilizzando campioni di midollo spinale di otto persone decedute con HAM e di due controlli neurologicamente sani, il team ha impiegato tecniche di colorazione per vedere dove USP10 era presente e quanto intensamente veniva espresso nei neuroni.
Meno USP10, più neuroni in morte
Nei midolli spinali sani, USP10 era chiaramente visibile in molti neuroni. Nella maggior parte dei casi di HAM, tuttavia, la colorazione per USP10 nei neuroni risultava nettamente ridotta e in un paziente era quasi assente. Gli scienziati hanno quindi cercato i segni caratteristici dell’apoptosi con due metodi: un test TUNEL che rileva il DNA frammentato e la colorazione per la caspasi-3 attiva, una proteina coinvolta nelle fasi iniziali della morte cellulare. Nei controlli, praticamente nessun neurone mostrava questi segnali di morte. Al contrario, nei pazienti con HAM una larga frazione di neuroni era TUNEL-positiva e molti mostravano caspasi-3 attiva. Importante, i campioni con espressione più bassa di USP10 tendevano ad avere più neuroni apoptotici e meno neuroni sopravvissuti marcati da NeuN, un marcatore neuronale standard. Un paziente con HAM degno di nota che camminava ancora con un solo bastone dopo 22 anni presentava una forte espressione di USP10 e un numero di neuroni relativamente preservato, suggerendo che livelli più elevati di USP10 possano contribuire a proteggere contro una disabilità severa.
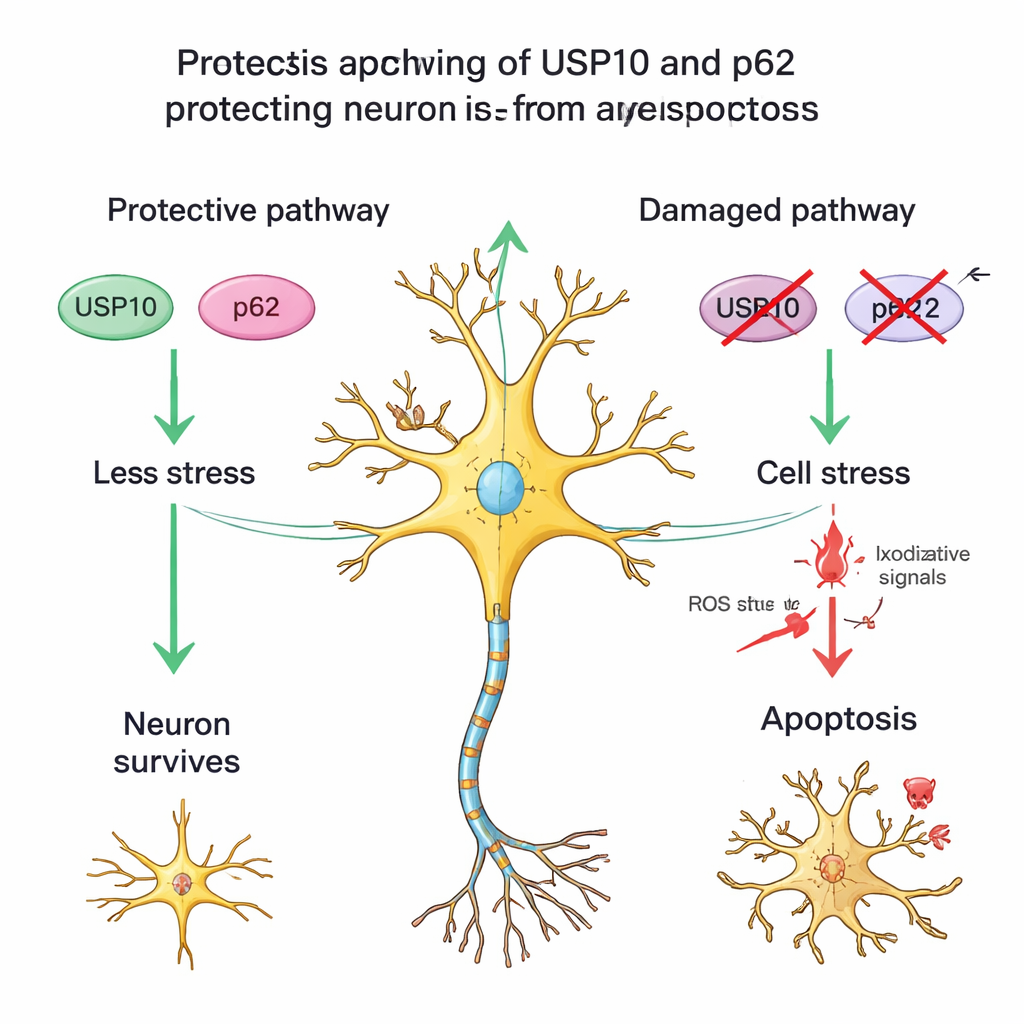
Una proteina partner e cellule stressate ma sopravvissute
Il team ha esaminato anche un’altra proteina, p62, che lavora con USP10 nella gestione delle proteine danneggiate e nella regolazione delle vie di stress e sopravvivenza. Nei midolli spinali sani, la colorazione per p62 era moderata; tra i pazienti con HAM, quelli con basso USP10 spesso avevano anche una colorazione più debole per p62 e meno neuroni sopravvissuti. Questo schema supporta l’idea di una partnership USP10–p62 che aiuta i neuroni a resistere all’infiammazione cronica. I ricercatori hanno inoltre notato molti neuroni nei tessuti HAM che avevano la forma tipica delle cellule nervose ma avevano perso la colorazione per NeuN, un segno osservato in altri danni cerebrali quando i neuroni sono sotto forte stress ma non ancora completamente morti. Ciò suggerisce che nella HAM alcuni neuroni vengono persi definitivamente mentre altri rimangono in uno stato danneggiato e vulnerabile, probabilmente perché le difese legate a USP10 sono indebolite.
Cosa potrebbe significare per la diagnosi e il trattamento futuri
Questo studio non dimostra che la perdita di USP10 causi direttamente la morte neuronale, poiché si basa su un piccolo numero di campioni autoptici e non può seguire i cambiamenti nel tempo. Tuttavia, i legami coerenti tra basso USP10, riduzione di p62, maggiori segni di apoptosi e meno neuroni sopravvissuti indicano una via comune che potrebbe collegare l’infiammazione cronica alla lenta degenerazione neuronale nella HAM. Per i pazienti, questo apre una possibilità incoraggiante: misurare o aumentare le vie correlate a USP10 nel midollo spinale — o potenzialmente in campioni più accessibili come il liquido cerebrospinale — potrebbe un giorno aiutare a identificare chi è a maggior rischio di progressione rapida, guidare il monitoraggio o ispirare nuovi trattamenti pensati per rafforzare i sistemi di protezione dallo stress della cellula nelle malattie neuroinfiammatorie indotte da virus.
Citazione: Arishima, S., Takahashi, M., Dozono, M. et al. Downregulation of the deubiquitinating enzyme USP10 correlates with neuronal apoptosis in HTLV-1-associated myelopathy. Sci Rep 16, 6062 (2026). https://doi.org/10.1038/s41598-026-37271-x
Parole chiave: Mielopatia associata a HTLV-1, neuroinfiammazione, apoptosi neuronale, USP10, degenerazione del midollo spinale