Clear Sky Science · it
Visualizzazione di biomolecole intercellulari usando indicatori proteici fluorescenti con ancore lipidiche-PEG
Guardare le cellule comunicare in tempo reale
I nostri cervelli e corpi dipendono da una costante conversazione chimica tra le cellule. Ioni e neurotrasmettitori scambiano messaggi attraverso spazi minuscoli, ma questi segnali rapidi e fugaci sono difficili da osservare senza disturbarli. Questo studio introduce un modo semplice per “verniciare” le cellule vive con sensori fluorescenti che si agganciano alla loro superficie esterna, permettendo agli scienziati di osservare questi messaggi — in particolare gli ioni potassio e il neurotrasmettitore glutammato — dal vivo e con dettaglio. 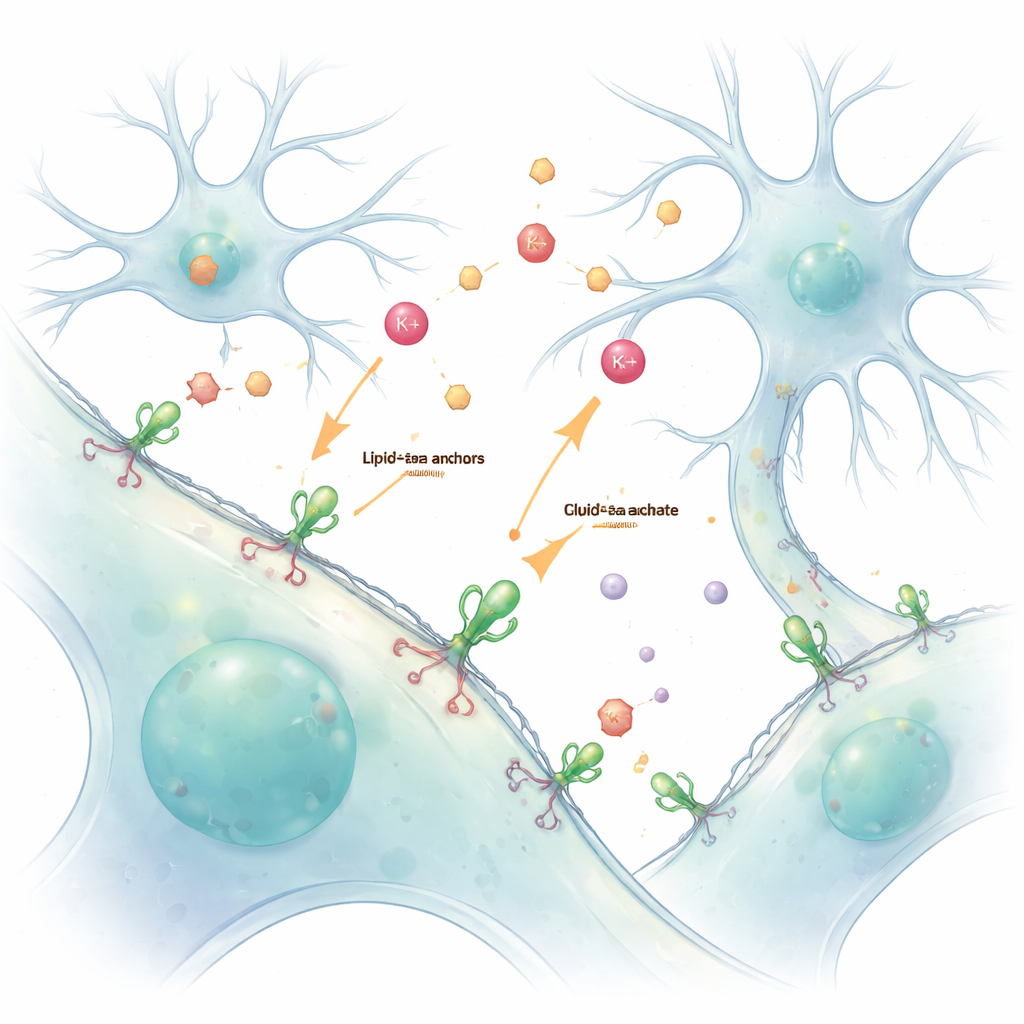
Un nuovo modo di etichettare la superficie cellulare
Tradizionalmente, i ricercatori ingegnerizzano le cellule perché producano sensori proteici fluorescenti dal loro stesso DNA. Pur essendo potente, questo approccio genetico spesso colloca i sensori all’interno della cellula, rendendo difficile separare ciò che avviene dentro da ciò che avviene fuori. Gli autori hanno risolto il problema usando una maniglia chimica chiamata ancora lipidica–PEG. Un’estremità di questa molecola si inserisce nella membrana esterna, mentre l’altra estremità è legata chimicamente a un sensore proteico fluorescente. Quando questi sensori preparati vengono semplicemente aggiunti alle cellule vive, rivestono spontaneamente la superficie esterna, formando uno strato stabile e luminoso che segnala cosa succede nel fluido circostante.
Trasformare potassio e glutammato in luce
Il gruppo ha adattato due indicatori fluorescenti esistenti: GINKO2, che risponde agli ioni potassio, e R-iGluSnFR1, che risponde al glutammato. Hanno purificato queste proteine da batteri e poi vi hanno attaccato le ancore lipidiche–PEG. Nelle cellule umane coltivate, il sensore del potassio ancorato ha formato un contorno regolare lungo la superficie cellulare e si è illuminato ogni volta che il potassio extracellulare aumentava, per poi affievolirsi quando i livelli scendevano. È importante che le proprietà di emissione della luce e la sensibilità corrispondessero strettamente al sensore originale non modificato negli esperimenti in provetta, mostrando che l’ancoraggio non ne ha intaccato le prestazioni. Lo stesso valeva per il sensore del glutammato, che è rimasto reattivo dopo l’ancoraggio e ha messo in evidenza chiaramente il glutammato nello spazio appena esterno alle cellule.
Ascoltare i neuroni in colture e fette
I ricercatori sono quindi passati a cellule nervose dell’ippocampo di topo, una regione cerebrale importante per l’apprendimento e la memoria. Hanno rivestito questi neuroni con il sensore del glutammato ancorato lipidico–PEG e hanno caricarto l’interno delle stesse cellule con un diverso colorante per il calcio che segnala l’attività elettrica. Usando la microscopia a riflessione interna totale, hanno potuto osservare lampi rossi del glutammato sulla superficie cellulare mentre segnali verdi all’interno delle cellule riportavano il loro sparo. Questa visione a due colori mostrava che i sensori ancorati potevano tracciare il rilascio spontaneo di neurotrasmettitore senza alcuna modifica genetica dei neuroni stessi.
Mappare onde chimiche attraverso il tessuto cerebrale
Successivamente il gruppo ha testato il metodo in fette cerebrali acute, che preservano l’innervazione naturale dell’ippocampo. Hanno applicato il sensore del potassio ancorato alle fette e stimolato elettricamente le fibre nervose. Il sensore ancorato ha prodotto aumenti di fluorescenza chiari e ripetibili dopo ogni stimolo, mentre i sensori non ancorati hanno rapidamente diffuso via e fornito segnali deboli e instabili. Bagnando le fette in soluzioni con livelli noti di potassio e correggendo per il lieve bagliore intrinseco del tessuto, gli autori hanno costruito una curva di calibrazione e stimato le concentrazioni extracellulari effettive di potassio. I livelli basali erano circa 2,5 millimolari e salivano a circa 3,4 millimolari con stimolazione modesta, in linea con misure classiche a elettrodo. I sensori ancorati per potassio e glutammato hanno rivelato come questi segnali si diffondano in modo diverso: le variazioni di glutammato restavano vicine alle sinapsi attive, mentre gli aumenti di potassio si estendevano per centinaia di micrometri, suggerendo effetti più ampi sull’eccitabilità della rete. 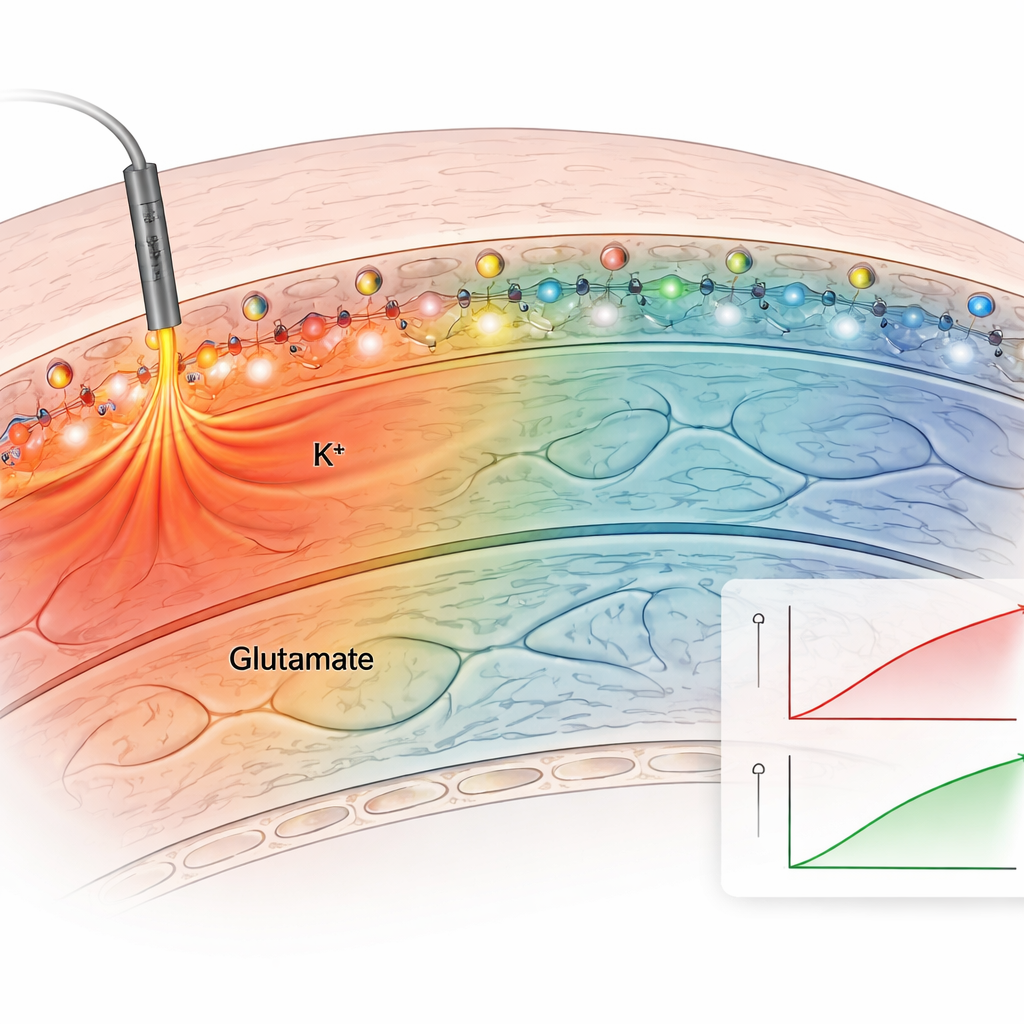
Indagare come il cervello pulisce e genera segnali
Poiché i sensori sono fissati sulla superficie cellulare, gli autori hanno potuto scomporre quali processi modellano queste onde extracellulari. Il blocco dei trasportatori di glutammato, che normalmente rimuovono il glutammato, ha fatto sì che il sensore del glutammato ancorato mostrasse segnali più grandi e di durata più lunga, confermando che la captazione locale limita la diffusione del glutammato. Il blocco dei recettori glutamatergici di tipo AMPA ha ridotto sia le risposte elettriche sia i segnali di potassio, indicando che la maggior parte dell’aumento di potassio proviene dai neuroni postsinaptici attivati dall’input sinaptico. Il blocco dei canali del sodio con tetrodotossina ha quasi abolito i cambiamenti di potassio, collegandoli direttamente ai potenziali d’azione. Insieme, questi esperimenti illustrano come i sensori ancorati possano trasformare chimica complessa e distribuita in filmati e mappe intuitivi.
Perché questo è importante per la ricerca cerebrale futura
Per i non specialisti, il messaggio chiave è che questo lavoro offre un modo rapido e non genetico per rivestire cellule e tessuti vivi con reporter molecolari altamente sensibili. Invece di re-ingegnerizzare ogni tipo cellulare, gli scienziati possono aggiungere dall’esterno proteine sensoriali preconfezionate e visualizzare immediatamente come ioni e neurotrasmettitori cambiano in tempo reale sulla superficie cellulare. Questo approccio migliora il controllo, la riproducibilità e la precisione spaziale, evitando le sfide della consegna genica, specialmente in preparazioni delicate come le fette cerebrali acute. Man mano che verranno sviluppati più indicatori fluorescenti per diverse sostanze chimiche, la stessa strategia di ancoraggio lipidico–PEG potrebbe diventare un kit ampiamente usato per osservare il linguaggio chimico delle cellule in tutto il corpo.
Citazione: Mita, M., Kiyosue, K. & Tani, T. Imaging intercellular biomolecules by using fluorescent protein indicators with lipid-PEG anchors. Sci Rep 16, 6964 (2026). https://doi.org/10.1038/s41598-026-37240-4
Parole chiave: segnalazione extracellulare, biosensori fluorescenti, imaging del glutammato, dinamiche del potassio, neuroni ippocampali