Clear Sky Science · it
Convoluzione grafica dinamica con potatura completa e classificazione GNN per la rilevazione precisa delle metastasi linfonodali
Perché piccole variazioni nei linfonodi contano
Quando il cancro al seno si diffonde, la sua prima tappa è spesso rappresentata dai linfonodi, piccoli filtri lungo il sistema di drenaggio del corpo. Rilevare se le cellule tumorali hanno raggiunto questi linfonodi è uno degli indizi più importanti che i medici usano per scegliere tra intervento chirurgico, chemioterapia e radioterapia. Eppure anche i patologi esperti possono non riconoscere gruppi molto piccoli di cellule tumorali nelle immagini microscopiche digitali, specialmente quando appaiono quasi identiche al tessuto sano. Questo studio presenta un nuovo framework di intelligenza artificiale che considera il tessuto come una rete di regioni connesse, permettendo di individuare segni sottili di diffusione con notevole accuratezza.
Trasformare le immagini di tessuto in reti
I ricercatori lavorano con enormi vetrini digitali colorati, chiamati whole-slide images, provenienti da biopsie linfonodali per il cancro al seno. Queste immagini contengono milioni di pixel e una confusa mescolanza di tipi cellulari, colori e texture. Per domare questa complessità, il gruppo prima pulisce le immagini: normalizza luminosità e colore, riduce il rumore e genera copie aumentate ruotando e capovolgendo i patch, così che il computer impari a gestire la variazione naturale. Ogni patch d’immagine viene quindi suddiviso in piccole regioni abbastanza uniformi ("superpixel"), che diventano i punti — o nodi — di un grafo, mentre le relazioni tra regioni adiacenti formano le linee di collegamento — o archi. Questa visione a rete conserva meglio le forme irregolari e la disposizione del tessuto reale rispetto ai metodi di imaging tradizionali basati su griglie.
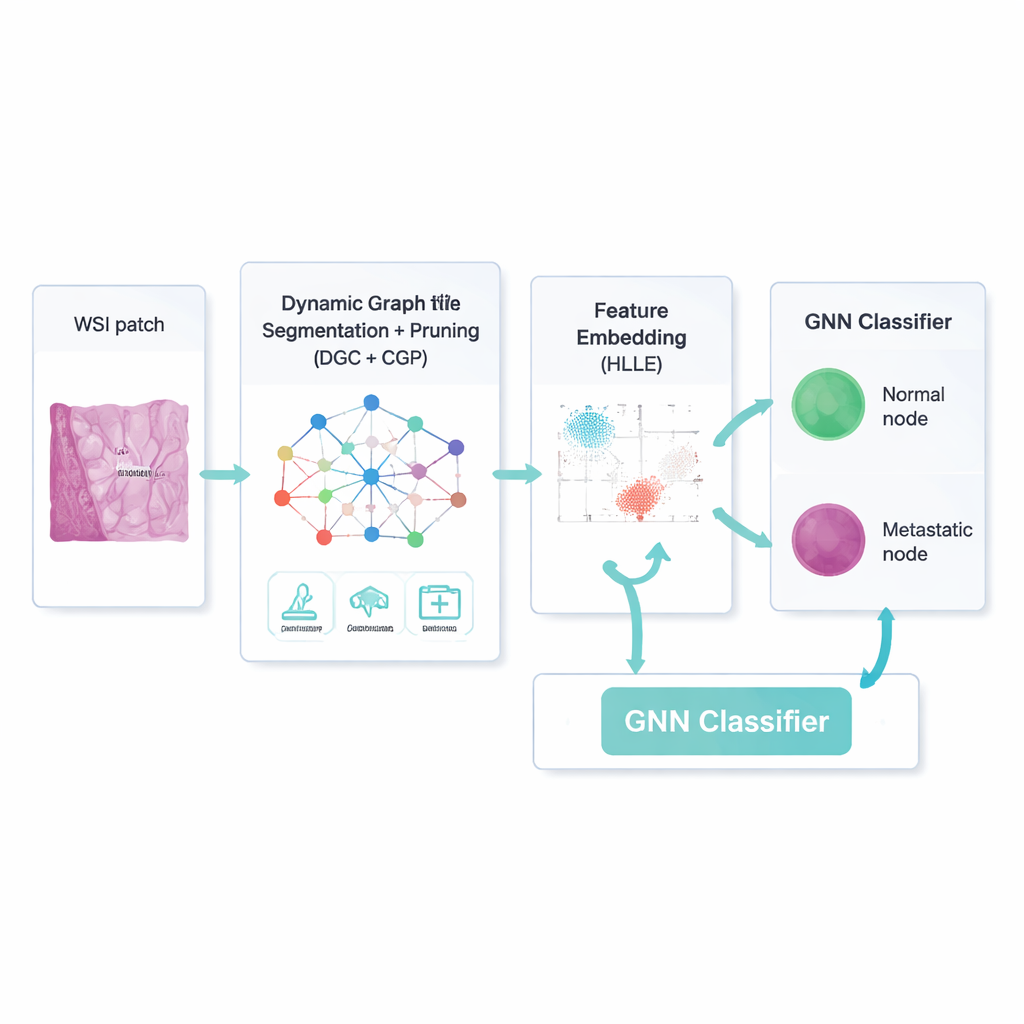
Un modo più intelligente per concentrarsi su ciò che conta
Costruire semplicemente una rete non basta; molte connessioni e caratteristiche delle immagini sono irrilevanti o addirittura fuorvianti. Il framework quindi usa un autoencoder convoluzionale grafico dinamico — un tipo di rete neurale che impara sia l’aspetto di ogni regione sia come le regioni si influenzano a vicenda. Un meccanismo aggiuntivo di "attenzione" insegna al modello a pesare alcuni canali dell’immagine più di altri, per esempio enfatizzando i bordi al confine di un tumore. Allo stesso tempo, una strategia chiamata Comprehensive Graph Gradual Pruning pota in modo graduale i componenti poco utili: connessioni deboli tra regioni, caratteristiche numeriche meno informative e pesi del modello a basso impatto. Questa potatura avviene durante l’addestramento, non dopo, così il sistema impara a fare di più con meno, risultando sia più veloce sia più facile da interpretare.
Comprimere i pattern senza perderne la forma
Dopo che il modello ha separato le regioni probabilmente linfonodali dal tessuto di sfondo, deve comunque descrivere ogni regione in modo compatto ma significativo. Per farlo, gli autori impiegano una tecnica chiamata Hessian-based Locally Linear Embedding. In termini semplici, riduce molte caratteristiche numeriche in un insieme più piccolo cercando di preservare la "forma" curva di come i casi reali sono disposti nello spazio delle caratteristiche — per esempio, come le minuscole metastasi differiscano dalle normali cellule immunitarie lungo sottili pattern di texture o colore. Queste descrizioni compresse diventano l’input per un classificatore basato su reti neurali su grafi, che lavora nuovamente sulla rete di regioni e sulle loro connessioni depurate, decidendo per ogni nodo se è metastatico o meno.
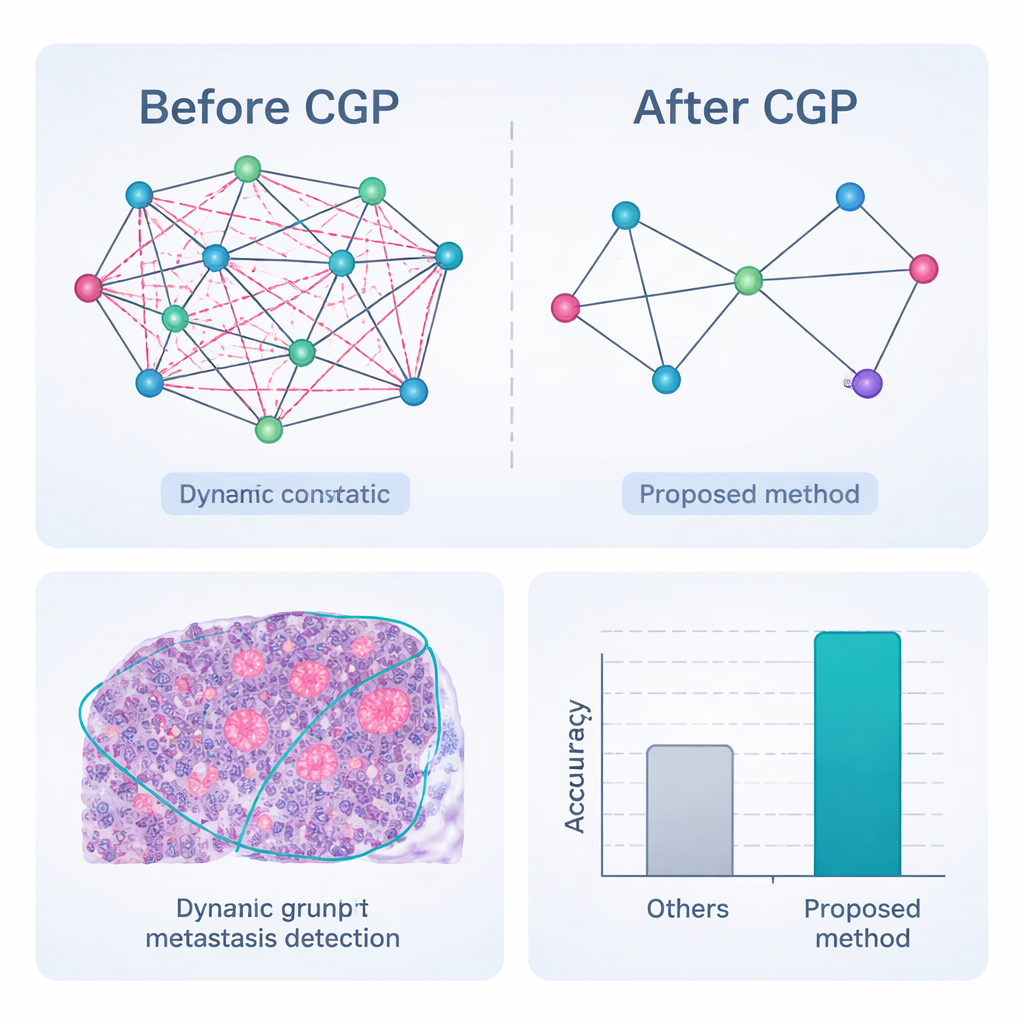
Mettere il framework alla prova
La pipeline completa — pre-elaborazione, segmentazione grafica dinamica con potatura, embedding delle caratteristiche e classificazione basata su grafi — è stata valutata su CAMELYON17, una raccolta pubblica di 1.000 vetrini linfonodali accuratamente annotati da esperti per pazienti con cancro al seno. Rispetto a una serie di forti competitor nel deep learning, inclusi popolari network convoluzionali e modelli ibridi transformer, il nuovo metodo ha ottenuto i punteggi più alti su quasi tutte le misure. Ha classificato correttamente i nodi come cancerosi o meno nel 98,65% dei casi e ha mostrato una migliore corrispondenza con i contorni esperti delle regioni tumorali, in particolare per metastasi molto piccole o deboli. Fondamentale, poiché il grafo è fortemente potato, il sistema raggiunge questi risultati con molte meno operazioni e minore uso di memoria, rendendolo più adatto all’uso in tempo reale nei laboratori di patologia affollati.
Cosa significa per pazienti e clinici
In termini pratici, questo lavoro dimostra come considerare il tessuto come una rete di regioni connesse sapientemente ridotta possa aiutare i computer a fungere da lettori di seconda opinione estremamente accurati per i vetrini linfonodali. Concentrando attenzione e risorse computazionali sulle strutture più informative e scartando il rumore, il framework è migliore nel riconoscere minuscoli semi di cancro che altrimenti potrebbero essere persi, e lo fa in modo sufficientemente efficiente da essere pratico. Pur richiedendo ulteriori validazioni cliniche, tali strumenti potrebbero supportare i patologi nel prendere decisioni più rapide e consistenti sulla presenza di diffusione tumorale — informazioni che modellano direttamente i piani di trattamento e, in ultima analisi, gli esiti per i pazienti.
Citazione: H. N., C., N., S., S., A.R. et al. Dynamic graph convolution with comprehensive pruning and GNN classification for precise lymph node metastasis detection. Sci Rep 16, 6682 (2026). https://doi.org/10.1038/s41598-026-37193-8
Parole chiave: metastasi linfonodali, patologia digitale, reti neurali su grafi, segmentazione di immagini mediche, cancro al seno