Clear Sky Science · it
Caratterizzazione strutturale del legame dei metalli nella tirosilproteina solfotransferasi umana 2, TPST2
Perché piccoli ioni metallici contano nel segnalare cellulare
All’interno delle nostre cellule, innumerevoli macchine molecolari regolano silenziosamente come i tessuti crescono, come agiscono gli ormoni e come comunicano le cellule immunitarie. Una di queste macchine, un enzima chiamato TPST2, aggiunge un piccolo tag solfato ad alcune proteine mentre passano attraverso il centro di smistamento della cellula, l’apparato del Golgi. Questo studio rivela come ioni metallici semplici, come il sodio e il manganese, aiutino TPST2 a funzionare in modo più efficiente irrigidendo sottilmente parti della sua struttura—un’osservazione che potrebbe collegare l’equilibrio dei minerali nelle cellule a cancro e disturbi legati agli ormoni. 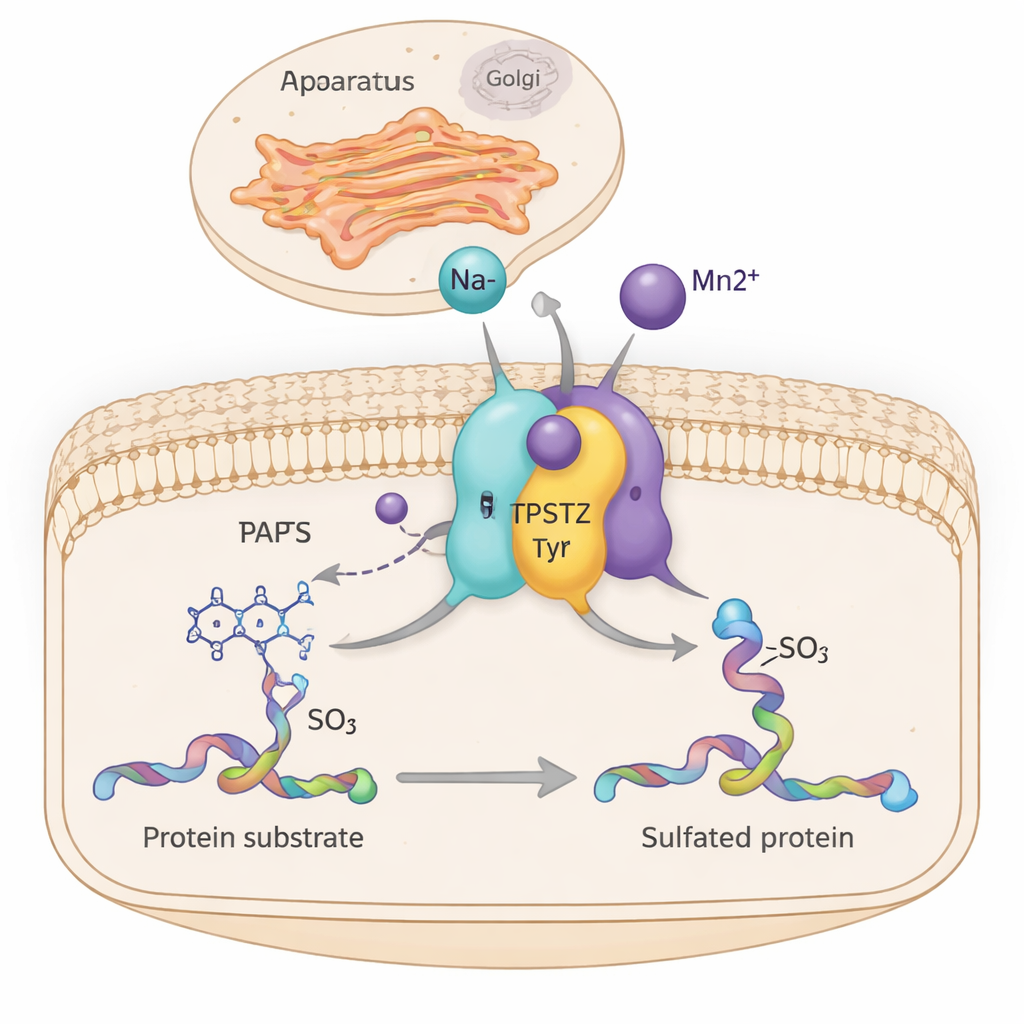
Una proteina che “decora” altre proteine
TPST2 appartiene a una famiglia di enzimi che eseguono la “solfatazione della tirosina”, una modifica chimica aggiunta a specifici residui di tirosina sulle proteine. Queste proteine solfatate svolgono ruoli chiave all’esterno delle cellule, influenzando la coagulazione del sangue, il movimento dei globuli bianchi, il legame tra ormoni e recettori e persino l’ingresso dei virus nelle cellule. Negli esseri umani esistono due principali enzimi solfatanti, TPST1 e TPST2, che risiedono nella membrana del Golgi e modificano le proteine mentre vengono preparate per l’esportazione. Studi sul topo mostrano che la perdita di TPST2 compromette la produzione di ormoni tiroidei, rallenta la crescita e causa infertilità maschile, sottolineandone l’importanza per la fisiologia normale.
Collegamenti con il cancro e l’evasione immunitaria
Ricerche recenti hanno collegato TPST2 direttamente alle malattie. Nel melanoma, TPST2 modifica una componente del recettore dell’interferone in modo da indebolire la segnalazione immunitaria, e bloccare TPST2 aumenta l’efficacia delle terapie con checkpoint immunitari che prendono di mira PD-1. Nel tumore del pancreas, una via dipendente da TPST2 aiuta a stabilizzare una proteina (integrina β4) che favorisce la crescita tumorale e la diffusione. Inibire TPST2 in questi modelli rallenta la divisione e l’invasione delle cellule tumorali. Poiché TPST2 agisce su proteine alla superficie cellulare, rimappa di fatto il modo in cui le cellule percepiscono e rispondono all’ambiente circostante, rendendolo un bersaglio interessante per nuove terapie.
Trovare gli “interruttori” metallici
I biochimici sanno da tempo che TPST2 diventa molto più attivo quando sono presenti metalli bivalenti come il manganese (Mn²⁺), ma mancava la spiegazione strutturale. In questo studio gli autori hanno prodotto il nucleo catalitico della TPST2 umana e l’hanno cristallizzato insieme a un sottoprodotto della reazione e a sodio (Na⁺) o manganese. Utilizzando cristallografia a raggi X ad alta risoluzione, hanno scoperto due piccole tasche di legame per i metalli all’interno dell’enzima, ciascuna con un ordinato arrangiamento a sei lati (ottaedrico) degli atomi circostanti. Sintonizzando la lunghezza d’onda dei raggi X sulle firme uniche dei diversi metalli, hanno confermato che Mn²⁺ occupa selettivamente questi siti, mentre metalli come zinco e rame si legano debolmente in altri punti o non si legano affatto.
Irrigidire parti mobili chiave invece di rimodellare l’intero enzima
Sorprendentemente, TPST2 con sodio e TPST2 con manganese sembravano quasi identici nel complesso; non c’era un’apertura o chiusura drammatica della proteina. Invece, i metalli influenzavano principalmente due regioni flessibili vicino all’ingresso del sito attivo: un’elica chiamata α3 e una vicina ansa nota come ansa α12–α13. Nello stato privo di metallo o con legami deboli questi segmenti oscillano e sono parzialmente disordinati. Quando si lega Na⁺ diventano più ordinati; Mn²⁺ li irrigidisce ulteriormente, come mostrano la riduzione del moto termico nei dati a raggi X e le analisi computerizzate della flessibilità. Questa rigidità aggiuntiva aumenta modestamente la temperatura di fusione dell’enzima ed è pensata per ridurre il costo “entropico” di organizzare il sito attivo—rendendo più facile e veloce per TPST2 posizionare i substrati correttamente per la solfatazione. 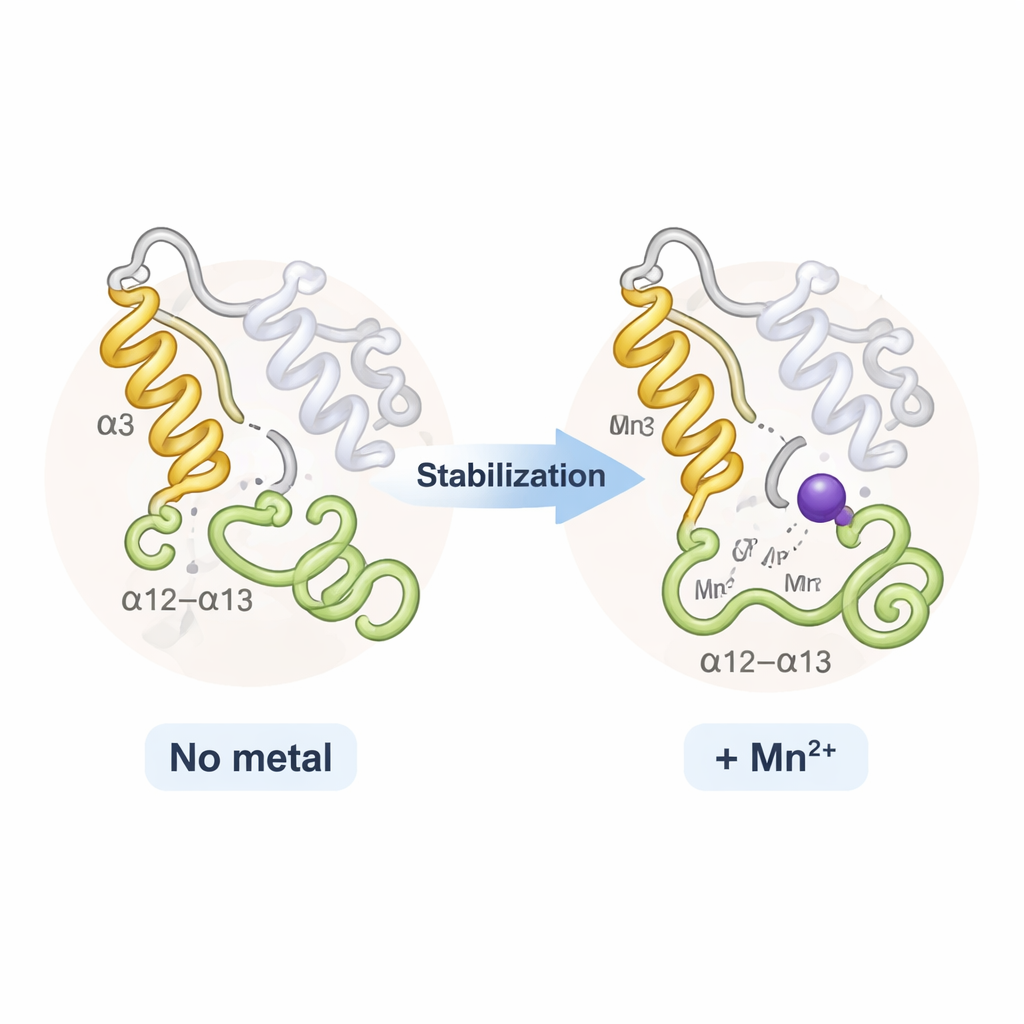
Dai minerali cellulari al controllo della segnalazione
Gli autori propongono un modello di “attivazione per ordinamento”. In assenza di metallo legato, TPST2 è flessibile attorno all’ingresso del sito attivo e funziona in modo inefficiente. Il sodio, abbondante nelle cellule, può legare gli stessi siti e creare uno stato parzialmente ordinato e moderatamente attivo. Il manganese, presente in quantità micromolari finemente controllate all’interno del Golgi, si lega più saldamente e blocca le regioni chiave in uno stato ottimamente disposto, massimizzando l’efficienza catalitica. Ciò suggerisce che sottili variazioni nei livelli di manganese nel Golgi potrebbero modulare quanto fortemente TPST2 modifica i suoi target. Poiché TPST2 influenza la produzione di ormoni e la segnalazione nei tumori, il lavoro mette in evidenza un possibile legame tra equilibrio degli ioni metallici, “decorazioni” proteiche e malattia—e fornisce un quadro strutturale per progettare farmaci che modulino l’attività di TPST2 imitando o interrompendo il legame dei metalli.
Citazione: Jin, M., Noh, C., Yang, J. et al. Structural characterization of metal binding in human tyrosylprotein sulfotransferase 2, TPST2. Sci Rep 16, 6066 (2026). https://doi.org/10.1038/s41598-026-37189-4
Parole chiave: solfatazione della tirosina, TPST2, manganese, apparato del Golgi, modificazione delle proteine