Clear Sky Science · it
Ensemble ibrido interpretabile con fusione basata su attention e ottimizzazione EAOO-GA per la rilevazione del cancro polmonare
Perché la diagnosi precoce del cancro polmonare riguarda tutti
Il cancro polmonare è uno dei tumori più letali in gran parte perché viene spesso scoperto troppo tardi, quando le opzioni terapeutiche sono limitate e le probabilità di sopravvivenza diminuiscono bruscamente. I medici fanno sempre più affidamento su scansioni TC e programmi informatici per individuare formazioni sospette nei polmoni prima che compaiano i sintomi. Questo articolo presenta un nuovo sistema di intelligenza artificiale (IA) che punta a rendere queste diagnosi computerizzate non solo più accurate, ma anche più affidabili e più facili da comprendere per i clinici.
Come i computer leggono le scansioni polmonari
I moderni sistemi di IA possono analizzare immagini TC e apprendere modelli che distinguono una macchia innocua da un tumore pericoloso. Questi sistemi, costruiti su reti neurali profonde, hanno già dimostrato di poter competere o addirittura superare gli esperti umani in compiti ristretti. Ma affrontano tre ostacoli importanti negli ospedali reali: possono adattarsi troppo a un singolo dataset e fallire con pazienti nuovi, faticano con dati sbilanciati dove alcuni tipi di patologia sono rari, e spesso funzionano come scatole nere opache di cui i clinici diffidano. Gli autori si concentrano su queste sfide usando un ampiamente impiegato dataset di TC polmonari che contiene tre tipi di casi: noduli benigni, noduli maligni e scansioni normali.
Molti occhi esperti invece di uno solo
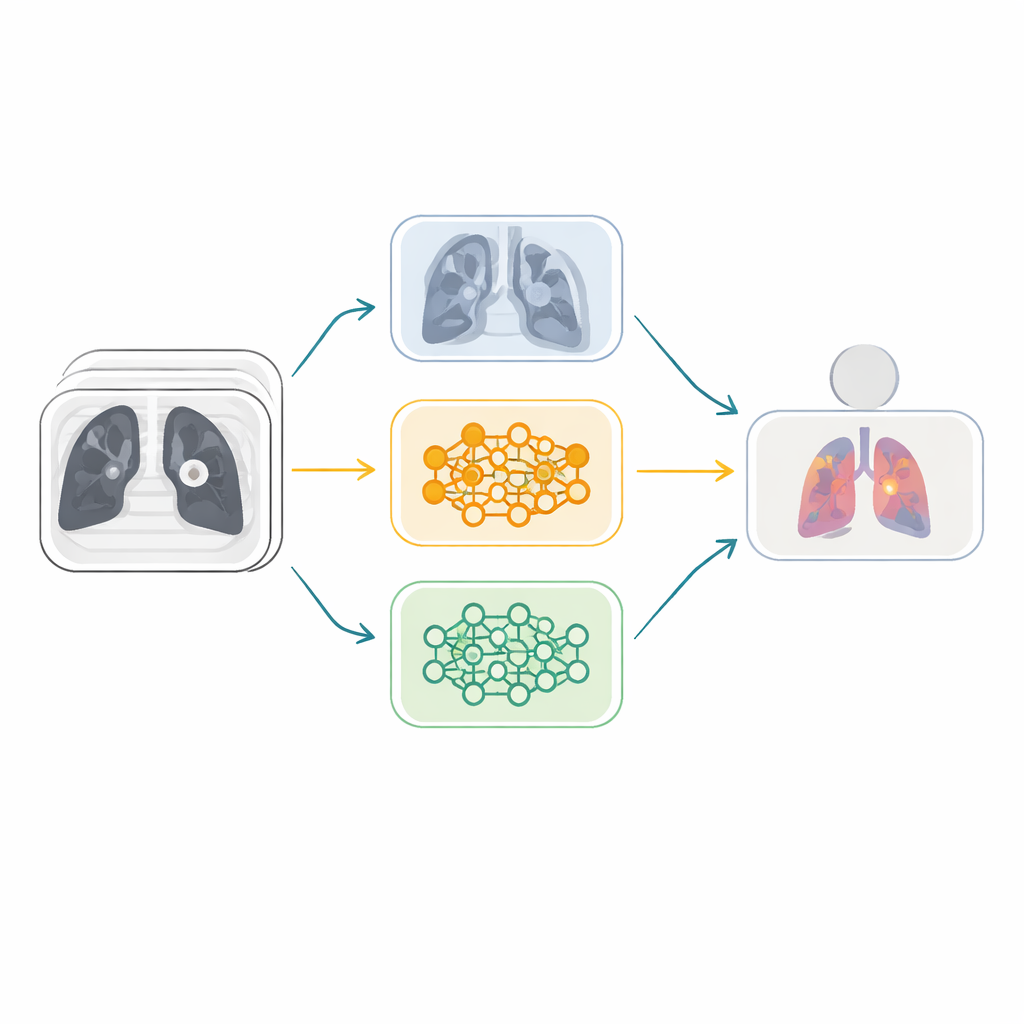
Invece di dipendere da una singola rete neurale, i ricercatori costruiscono un ensemble—una squadra di diversi modelli IA che votano insieme. Partono da sei potenti architetture di riconoscimento delle immagini originariamente addestrate su milioni di foto comuni e le adattano alle scansioni TC polmonari. Questi modelli sono poi accoppiati in tre rami di “fusione”, ciascuno combinando due reti con punti di forza complementari. All’interno di ogni ramo, un meccanismo di attenzione speciale, noto come Squeeze-and-Excitation, impara quali canali di feature interni contengono gli indizi visivi più utili—come texture sottili o forme dei noduli—e li amplifica mentre attenua i pattern meno informativi. Questo aiuta il sistema a concentrarsi su dettagli di significato medico anziché sul rumore.
Lasciare che una ricerca ispirata alla natura affini la squadra
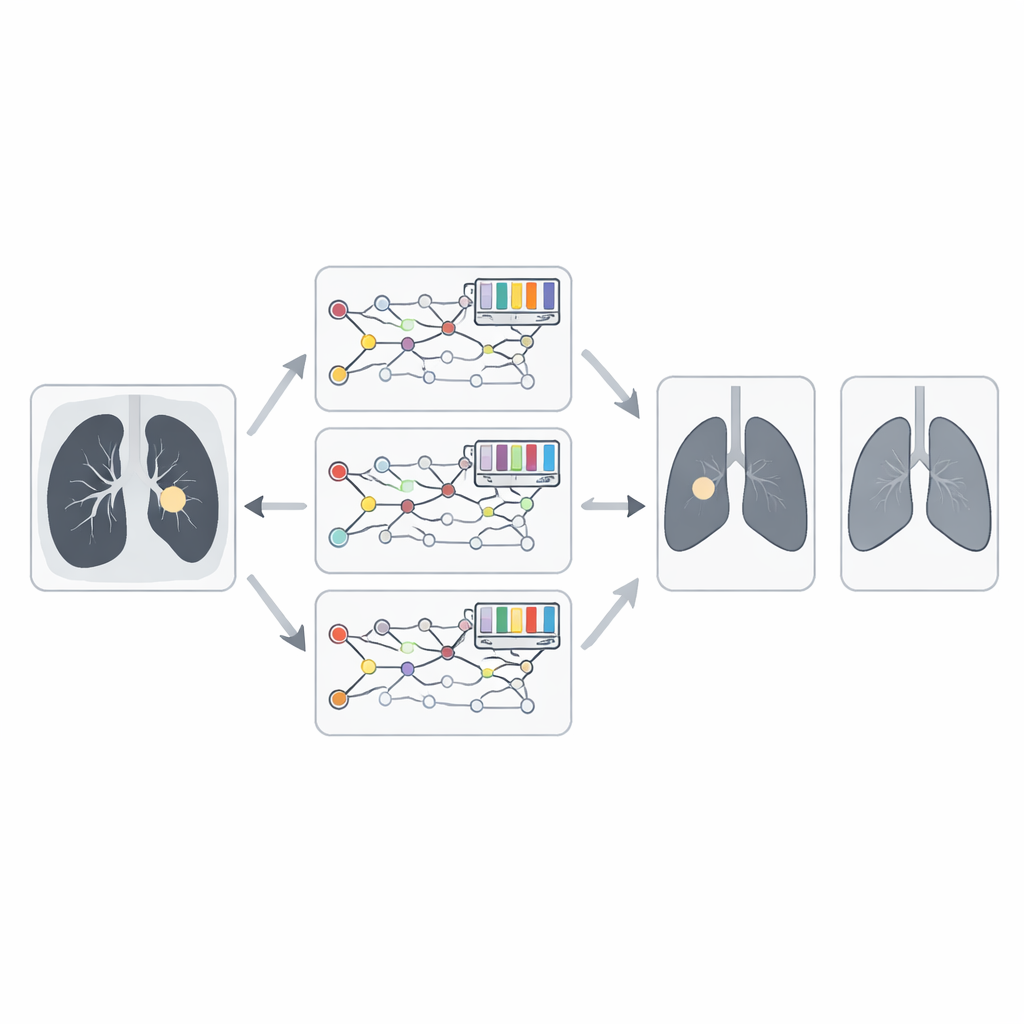
Semplicemente mediare le opinioni dei tre rami forti lascia ancora margini di miglioramento. L’idea chiave di questo lavoro è lasciare che un ottimizzatore ispirato alla natura decida quanto peso assegnare a ciascun ramo. Il team introduce una versione migliorata dell’algoritmo Animated Oat Optimization, potenziata con operazioni genetiche come crossover e mutazione. In termini semplici, questo algoritmo tratta le combinazioni candidate di pesi come una popolazione e le “evolve” ripetutamente, mantenendo quelle che portano a previsioni del cancro più accurate e rimescolando le altre. Dopo molte iterazioni scopre un equilibrio efficace in cui i modelli di fusione più affidabili contribuiscono in misura maggiore alla diagnosi finale.
Bilanciare i casi rari e aprire la scatola nera
I dati medici reali spesso contengono molti più esempi maligni rispetto a quelli benigni o normali, il che può indurre un sistema di IA a sovrastimare la presenza di cancro. Per contrastare questo, gli autori usano una tecnica chiamata SMOTE per generare esempi sintetici aggiuntivi per le classi sottorappresentate, riequilibrando la distribuzione di addestramento. Aggiungono inoltre uno strato esplicativo usando Grad-CAM, che produce mappe di calore che mostrano le regioni dell’immagine che hanno maggiormente influenzato ogni decisione. Nei casi maligni, le aree evidenziate coincidono tipicamente con noduli irregolari e spiculati; per le scansioni benigne o normali, l’attenzione si sposta su tessuti più lisci. Questo aiuta i radiologi a verificare che il modello stia guardando le strutture giuste piuttosto che artefatti irrilevanti.
Quanto bene si comporta il sistema sui dati del mondo reale
Quando testato sul dataset di cancro polmonare IQ-OTH/NCCD, l’ensemble proposto raggiunge un’impressionante accuratezza di circa il 99,4 percento, con precisione, recall e F1-score altrettanto elevati. Supera costantemente ogni singola rete, schemi di fusione più semplici e una gamma di altri metodi di ottimizzazione. Fondamentale, gli autori validano anche il modello su una raccolta TC separata e ampiamente utilizzata nota come LIDC-IDRI, dove mantiene quasi il 98 percento di accuratezza. Questo test esterno suggerisce che il sistema si generalizza oltre le immagini su cui è stato originariamente addestrato, requisito chiave per qualsiasi strumento destinato ad assistere clinici in diversi ospedali e con impostazioni di scanner differenti.
Cosa significa questo per pazienti e clinici
Per un profano, la conclusione più importante è che combinare diversi “esperti” IA, sintonizzare accuratamente il modo in cui collaborano e rendere più trasparente il loro ragionamento può migliorare sensibilmente la rilevazione precoce del cancro polmonare dalle scansioni TC. Il framework introdotto in questo articolo trasforma immagini grezze in un parere secondario altamente accurato e relativamente interpretabile per i radiologi. Se ulteriormente validato in trial clinici e adattato ai flussi di lavoro ospedalieri quotidiani, tali sistemi potrebbero aiutare a individuare tumori pericolosi prima, ridurre test di controllo non necessari e, in ultima analisi, migliorare la sopravvivenza e la qualità della vita delle persone a rischio di cancro polmonare.
Citazione: Al Duhayyim, M., Aldawsari, M.A., Ismail, A. et al. Interpretable hybrid ensemble with attention-based fusion and EAOO-GA optimization for lung cancer detection. Sci Rep 16, 8159 (2026). https://doi.org/10.1038/s41598-026-37187-6
Parole chiave: rilevazione del cancro polmonare, analisi TC, ensemble di deep learning, IA per immagini mediche, diagnostica spiegabile