Clear Sky Science · it
Valutazione multimodale mediante imaging del microambiente midollare ipossico e del danno vascolare di tipo H nel diabete
Perché la salute delle ossa conta nel diabete
Spesso si associa il diabete di tipo 1 al glucosio nel sangue e all’insulina, ma la malattia rimodella silenziosamente anche lo scheletro. Molti pazienti sviluppano ossa più fragili e corrono un rischio elevato di fratture, anche quando i test sulla densità ossea appaiono quasi normali. Questo studio esplora cosa accade in profondità nel midollo osseo di conigli modello di diabete, utilizzando tecniche di imaging medico avanzate per osservare in vivo i piccoli vasi e i livelli di ossigeno. Capire questo danno nascosto potrebbe indicare la via a diagnosi più precoci e a nuovi trattamenti per proteggere la solidità ossea nelle persone con diabete.
Le autostrade sanguigne nascoste dell’osso
All’interno delle ossa lunghe come la tibia si trova una fitta rete di vasi sanguigni che non solo nutrono l’osso, ma ne guidano crescita e riparazione. Tra questi vasi esiste un sottotipo speciale chiamato «vasi di tipo H», concentrati vicino alle estremità dell’osso, dove sono presenti le cartilagini di accrescimento e il rimodellamento osseo attivo. Questi vasi trasportano più ossigeno rispetto ad altri e sono strettamente legati alla formazione di nuovo osso. Nel diabete di tipo 1, tuttavia, l’iperglicemia cronica produce sottoprodotti chimici e stress ossidativo che possono soffocare questo sistema finemente regolato. I ricercatori si sono proposti di visualizzare, negli animali vivi, come questi cambiamenti si sviluppano in diverse regioni dell’osso.
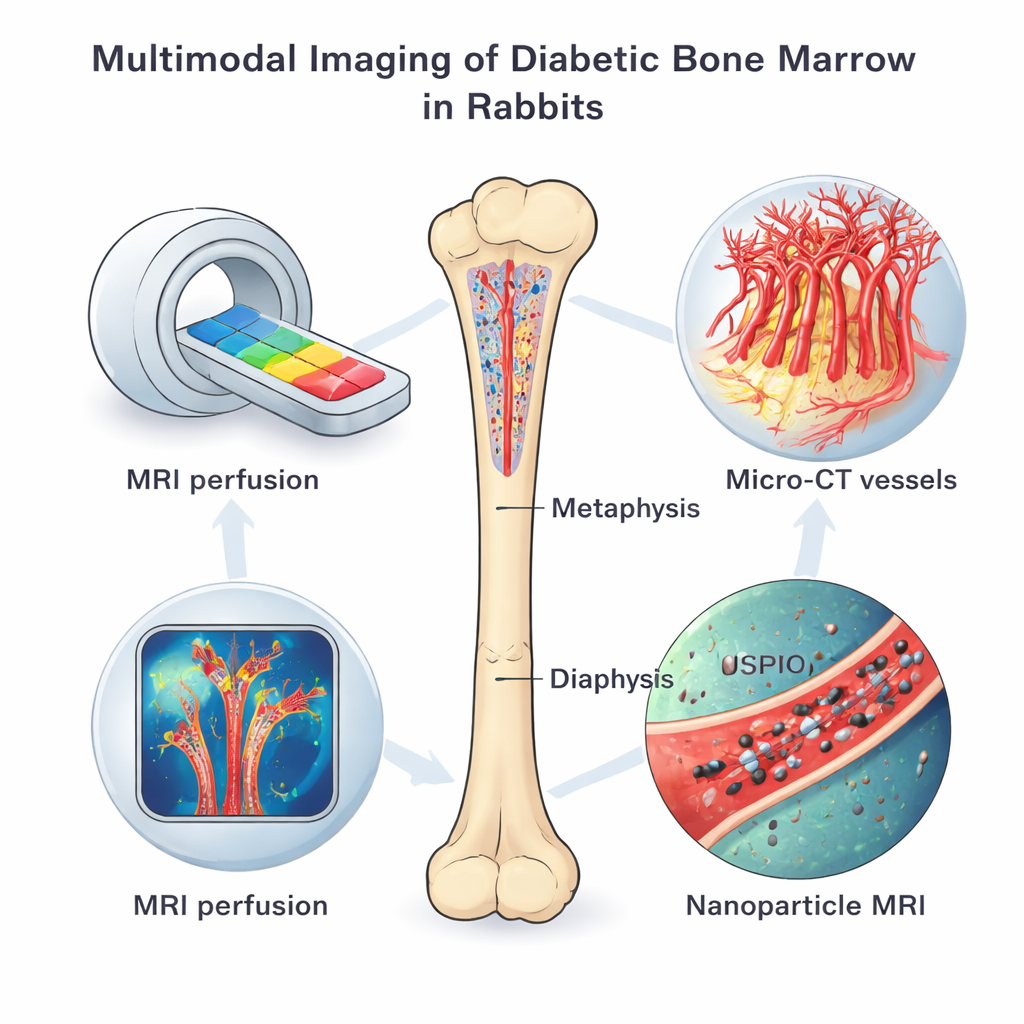
Scansionare l’osso vivo da molte angolazioni
Il gruppo ha impiegato una batteria di strumenti di imaging su conigli con diabete di tipo 1 indotto chimicamente e su controlli sani, tutti esaminati quattro mesi dopo l’instaurarsi del diabete. La risonanza magnetica dinamica con contrasto ha tracciato la velocità con cui un colorante entra ed esce dal midollo osseo, rivelando quanto i piccoli vasi perfondono il tessuto e quanto risultino permeabili. Un’altra tecnica di risonanza magnetica, potenziata con nanoparticelle a base di ferro, ha mostrato quanto attivamente le cellule endoteliali captassero particelle, indice di metabolismo e comportamento vascolare alterati. Dopo il sacrificio degli animali, scansioni micro-CT ad alta risoluzione hanno mappato la rete tridimensionale dei microvasi, mentre colorazioni fluorescenti, test genetici e microscopia elettronica hanno esaminato i tipi di vasi, le proteine sensibili all’ossigeno e i danni cellulari con grande dettaglio.
Dove il diabete colpisce più duramente dentro l’osso
In tutti i metodi di imaging, i conigli diabetici mostravano vasi midollari più permeabili e anomali rispetto agli animali sani. Il colorante di contrasto si muoveva più rapidamente e si tratteneva più a lungo, e le nanoparticelle di ferro venivano assorbite con maggiore intensità, in particolare vicino alla metafisi—la regione terminale dell’osso ricca di vasi di tipo H. La micro-CT ha rivelato che le ossa diabetiche avevano molte meno piccole ramificazioni vascolari e un volume vascolare complessivo inferiore, al punto che il consueto vantaggio della metafisi rispetto alla diafisi svaniva. Citometria a flusso e marcature fluorescenti hanno confermato che la proporzione dei vasi di tipo H è diminuita drasticamente nel diabete, mentre i nuovi vasi che spuntano lungo la cartilagine di accrescimento sono diventati scarsi. In breve, il nicchio vascolare che normalmente sostiene una robusta formazione ossea è stato selettivamente assottigliato e danneggiato.
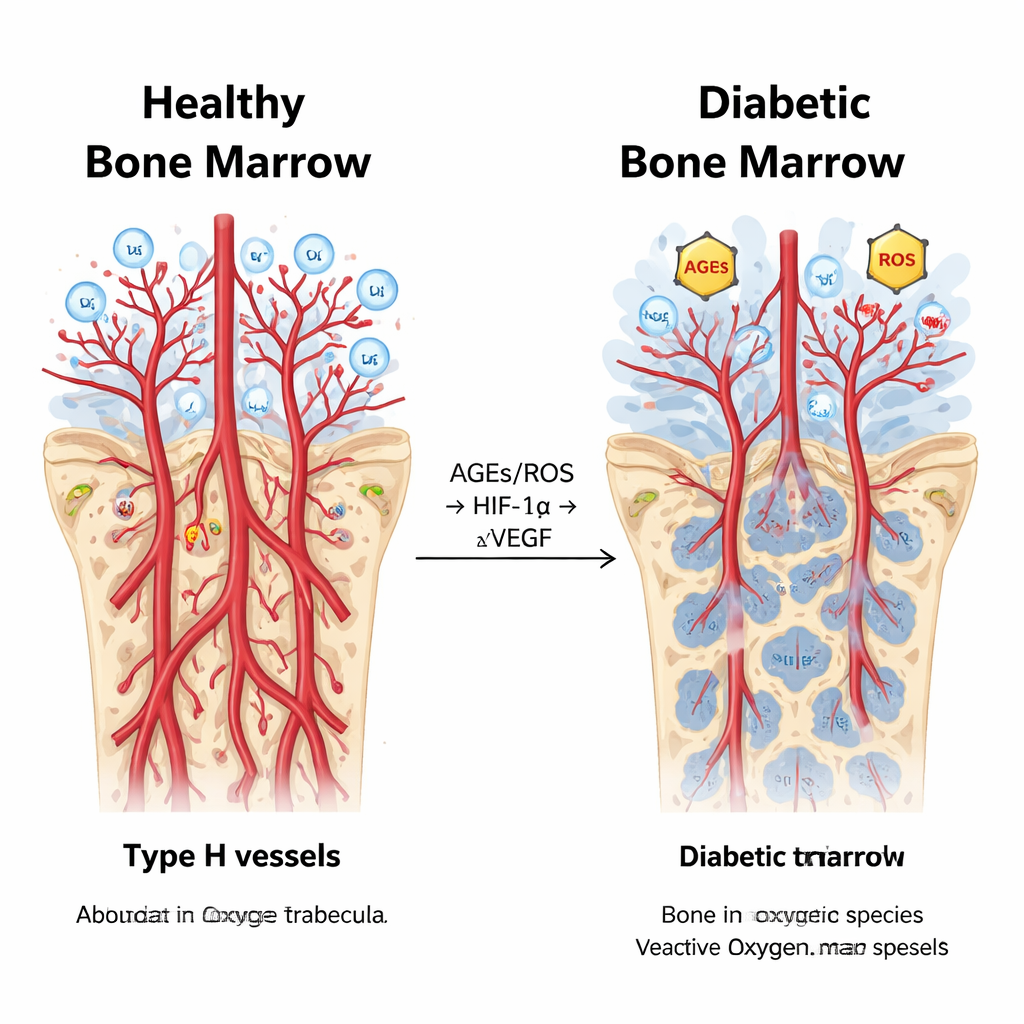
Una cascata chimica ingarbugliata nel midollo diabetico
Approfondendo, gli scienziati hanno misurato le molecole coinvolte nell’ipossia—la carenza di ossigeno sufficiente—e nello stress ossidativo indotto dall’alta glicemia. I conigli diabetici presentavano livelli più elevati di prodotti terminali della glicazione avanzata (AGEs) e specie reattive dell’ossigeno (ROS), insieme a una maggiore attività della proteina sensibile all’ossigeno HIF-1α e del suo recettore partner AGER, in particolare nella metafisi. Sorprendentemente, sebbene HIF-1α normalmente promuova la crescita vascolare, il segnale chiave di crescita VEGF risultava in realtà soppresso nel midollo osseo diabetico, e lo sviluppo di nuovi vasi è diminuito. Le analisi statistiche hanno collegato questi elementi: i marker di stress ossidativo e di perfusione anomala variavano in parallelo con HIF-1α, mentre VEGF e le misure della densità vascolare si muovevano nella direzione opposta. Questo schema suggerisce che, nel diabete cronico, il normale «allarme» dell’ossigeno venga dirottato, alimentando infiammazione e permeabilità anziché una sana formazione di nuovi vasi e di osso.
Cosa significa per le persone con diabete
In termini semplici, lo studio mostra che il diabete non assottiglia le ossa in modo uniforme; crea punti focali di danno vascolare e ipossia, soprattutto dove l’osso dovrebbe essere più forte e rigenerativo. Combinando più metodi di imaging, i ricercatori hanno potuto vedere sia la permeabilità funzionale sia la perdita strutturale dei vasi di tipo H, e collegare questi cambiamenti a una specifica via chimica che coinvolge AGEs, ROS, HIF-1α e VEGF. Per i pazienti, questo lavoro suggerisce che in futuro esami di imaging potrebbero individuare precocemente il danno osseo prima che insorgano fratture, e che terapie volte a ripristinare una segnalazione ossigenica sana e a proteggere i vasi di tipo H potrebbero diventare una nuova strategia per prevenire la malattia ossea diabetica.
Citazione: Lei, H., Wang, K., Li, L. et al. Multimodal imaging evaluation of hypoxic bone marrow microenvironment and type H vascular injury in diabetes. Sci Rep 16, 7206 (2026). https://doi.org/10.1038/s41598-026-37164-z
Parole chiave: diabete di tipo 1, midollo osseo, danno microvascolare, ipossia, fragilità ossea