Clear Sky Science · it
L’ultra-raffreddamento ultra-rapido su doppia superficie solida potenziato dalla pressione migliora il recupero dopo scongelamento in epatociti e fette di fegato a taglio di precisione
Perché è importante congelare il tessuto epatico
Mantenere cellule e tessuti vitali al di fuori del corpo è uno dei lavori silenziosi della medicina moderna. Cellule epatiche congelate aiutano i ricercatori a testare nuovi farmaci, modellare malattie e potrebbero un giorno riparare organi in insufficienza. Ma congelare materiale vivente è complesso: se i cristalli di ghiaccio crescono dentro o tra le cellule, lacerano strutture delicate. Questo studio esplora un nuovo modo di congelare rapidamente cellule epatiche e sottili fette di fegato in condizioni così controllate che i cristalli dannosi hanno a malapena il tempo di formarsi.
Il problema del ghiaccio e dei protettori chimici
La crioconservazione convenzionale si basa su due strumenti imperfetti: il freddo e i prodotti chimici. Quando i campioni vengono raffreddati, l’acqua tende a formare ghiaccio, che può perforare le membrane e danneggiare i tessuti. Per contrastare questo, gli scienziati aggiungono agenti crioprotettivi, come il dimetilsolfossido (DMSO), che aiutano l’acqua a solidificarsi in uno stato vetroso anziché in cristalli. Tuttavia, alle alte concentrazioni tipicamente utilizzate, questi agenti possono essere tossici per le cellule o causare dannosi rigonfiamenti e restringimenti mentre si muovono dentro e fuori dal tessuto. L’obiettivo degli autori era ridurre la quantità di DMSO necessaria pur evitando il ghiaccio dannoso, rendendo il banking di cellule e tessuti epatici più sicuro e pratico.
Un nuovo modo di comprimere e raffreddare contemporaneamente
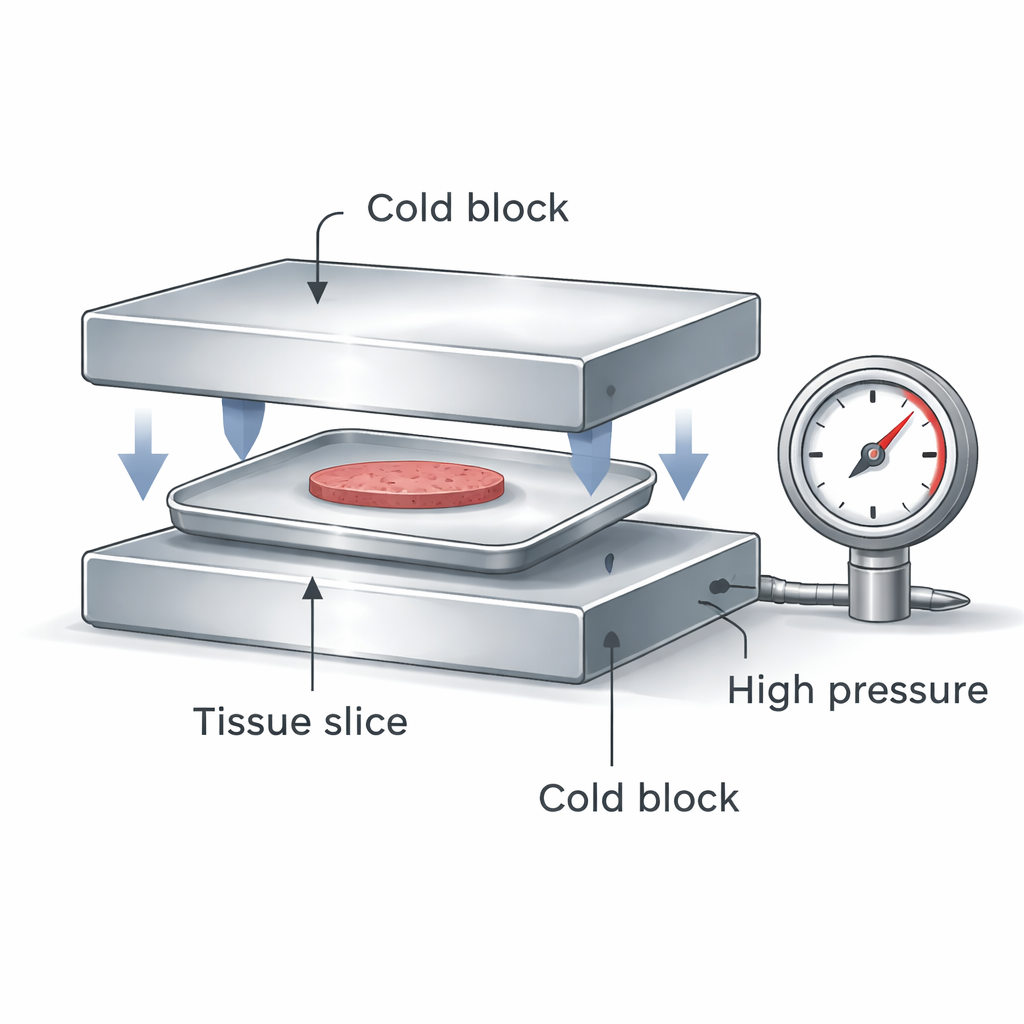
Il team ha progettato un dispositivo compatto che intrappola un contenitore piano sigillato in alluminio contenente cellule epatiche o fette di fegato tra due blocchi metallici estremamente freddi. Quando i blocchi vengono serrati, fanno due cose importanti contemporaneamente: creano alta pressione all’interno del contenitore sigillato e estraggono calore dal campione sia dall’alto che dal basso. L’alta pressione modifica il comportamento dell’acqua, facendo sì che il ghiaccio si formi a temperature più basse e che la soluzione vetrifichi più facilmente. Il contatto su due lati garantisce una velocità di raffreddamento molto più rapida e uniforme rispetto all’immergere semplicemente una provetta di plastica nel nitrogeno liquido, e il contenitore sigillato mantiene il campione isolato da contaminazioni.
Trovare il punto ottimale tra sicurezza e sopravvivenza
Per verificare se questo approccio fosse abbastanza delicato per il materiale vivente, i ricercatori hanno prima controllato che lo stesso contenitore in alluminio non danneggiasse le cellule HepG2 derivate dal fegato durante i brevi tempi di manipolazione utilizzati. La sopravvivenza cellulare è rimasta sostanzialmente invariata. Hanno quindi esposto queste cellule a diversi livelli di DMSO prima del congelamento e confermato un compromesso noto: più DMSO sopprime meglio il ghiaccio ma risulta chiaramente tossico al 30%, mentre il 20% rimane in gran parte tollerabile. Per le fette di fegato di topo hanno testato quanta pressione il tessuto poteva sopportare in assenza di congelamento. Raffiche brevi fino a 150 megapascal hanno avuto poco effetto sulla vitalità, ma 200 megapascal hanno causato circa un calo del 30%, segnando un limite superiore per un’operazione sicura.
Fette di fegato meglio conservate dopo lo scongelamento
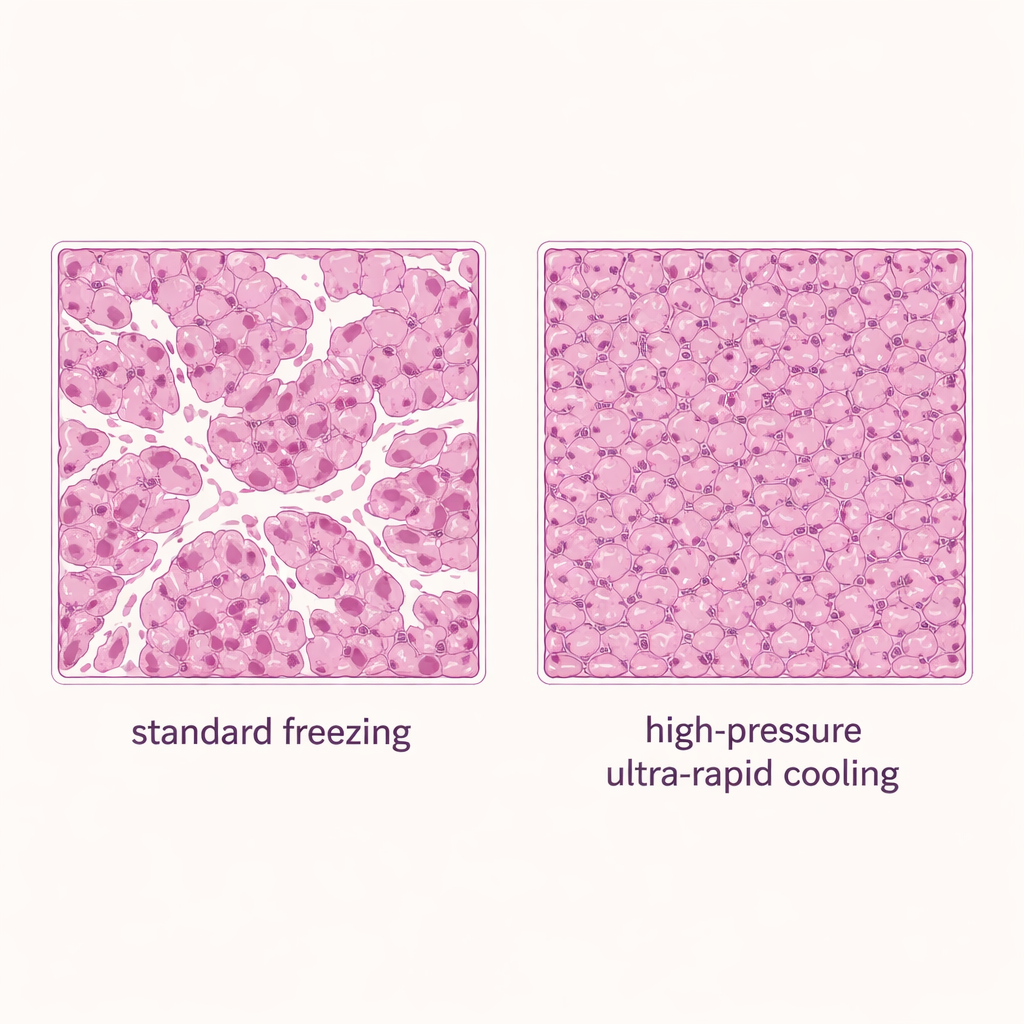
Con i limiti di sicurezza stabiliti, gli autori hanno confrontato tre metodi di congelamento per le fette di fegato: immersione standard del contenitore sigillato nel nitrogeno liquido (un approccio convettivo, basato su fluido), raffreddamento su superficie solida senza pressione aggiuntiva e raffreddamento su superficie solida con alta pressione a 150 megapascal. Tutti i gruppi hanno usato il 20% di DMSO. Il metodo assistito da pressione ha fornito i migliori risultati: è stata mantenuta circa l’80% della vitalità originale del tessuto, superando sia il congelamento standard che il raffreddamento su superficie solida da solo. La microscopia delle fette tissutali colorate ha supportato questi risultati. I campioni congelati per immersione convenzionale mostravano molti spazi bianchi aperti—segni di danno da ghiaccio—mentre il raffreddamento su superficie solida potenziato dalla pressione ha prodotto tessuti più densi e integri con molte meno lacune.
Cosa significa per il futuro del banking dei tessuti
Complessivamente, lo studio mostra che comprimere una fetta di fegato sigillata in alluminio tra due blocchi ultra-freddi sotto pressione elevata e controllata può migliorare notevolmente la sopravvivenza del tessuto dopo lo scongelamento. Combinando un raffreddamento più rapido e uniforme con il comportamento dell’acqua alterato dalla pressione, il metodo limita la crescita di ghiaccio dannoso pur utilizzando una concentrazione moderata e clinicamente familiare di DMSO. Per un lettore non specialista, la conclusione è che un’ingegneria più intelligente—come impacchettiamo e raffreddiamo i tessuti—può essere importante quanto i chimici che aggiungiamo. Questo approccio a doppia superficie e ad alta pressione potrebbe diventare un passo verso un banking del fegato più sicuro e affidabile e, in futuro, di altri organi per ricerca e terapia.
Citazione: Amini, M., Benson, J.D. Pressure enhanced dual-solid-surface ultra-rapid cooling improves post-thaw recovery in hepatocytes and precision cut liver slices. Sci Rep 16, 5994 (2026). https://doi.org/10.1038/s41598-026-37136-3
Parole chiave: crioconservazione, tessuto epatico, vetrificazione, raffreddamento ad alta pressione, congelamento senza ghiaccio