Clear Sky Science · it
DANEELpath strumenti digitali open source per l’analisi istopatologica nella ricerca sul neuroblastoma
Perché i piccoli tumori nel gel contano
Il cancro non è solo un ammasso di cellule impazzite; è un intero quartiere in cui le cellule comunicano tra loro e con l’impalcatura che le circonda. Nei tumori infantili come il neuroblastoma, questa struttura di supporto può favorire la crescita tumorale e la resistenza alle terapie. Questo studio presenta DANEELpath, un insieme gratuito e open source di strumenti digitali che trasforma immagini al microscopio di mini-tumori coltivati in laboratorio in mappe quantitative ricche di informazioni. In questo modo aiuta gli scienziati a comprendere come le cellule tumorali si organizzano, come rispondono a farmaci sperimentali e come questi risultati potrebbero tradursi in terapie migliori per i bambini.
Costruire piccoli mondi tumorali in laboratorio
Per imitare l’ambiente complesso di un vero tumore, i ricercatori coltivano cellule di neuroblastoma all’interno di idrogeli 3D morbidi a base di gelatina e seta. In questo contesto, le cellule formano naturalmente aggregati rotondi, simili a mini-tumori. Un protagonista in questo ambiente è la vitronectina, una proteina adesiva della matrice extracellulare che aiuta le cellule ad ancorarsi e può favorire un comportamento più aggressivo. Il gruppo ha preparato idrogeli con e senza vitronectina aggiunta e ha esposto alcuni di essi a cilengitide, un farmaco sperimentale che blocca i recettori cellulari legati alla vitronectina. Dopo settimane di crescita, i gel sono stati sezionati, colorati e scannerizzati come immagini digitali ad alta risoluzione dell’intero vetrino, creando una versione digitale di ogni mini-mondo tumorale.
Trasformare immagini complesse in pattern misurabili
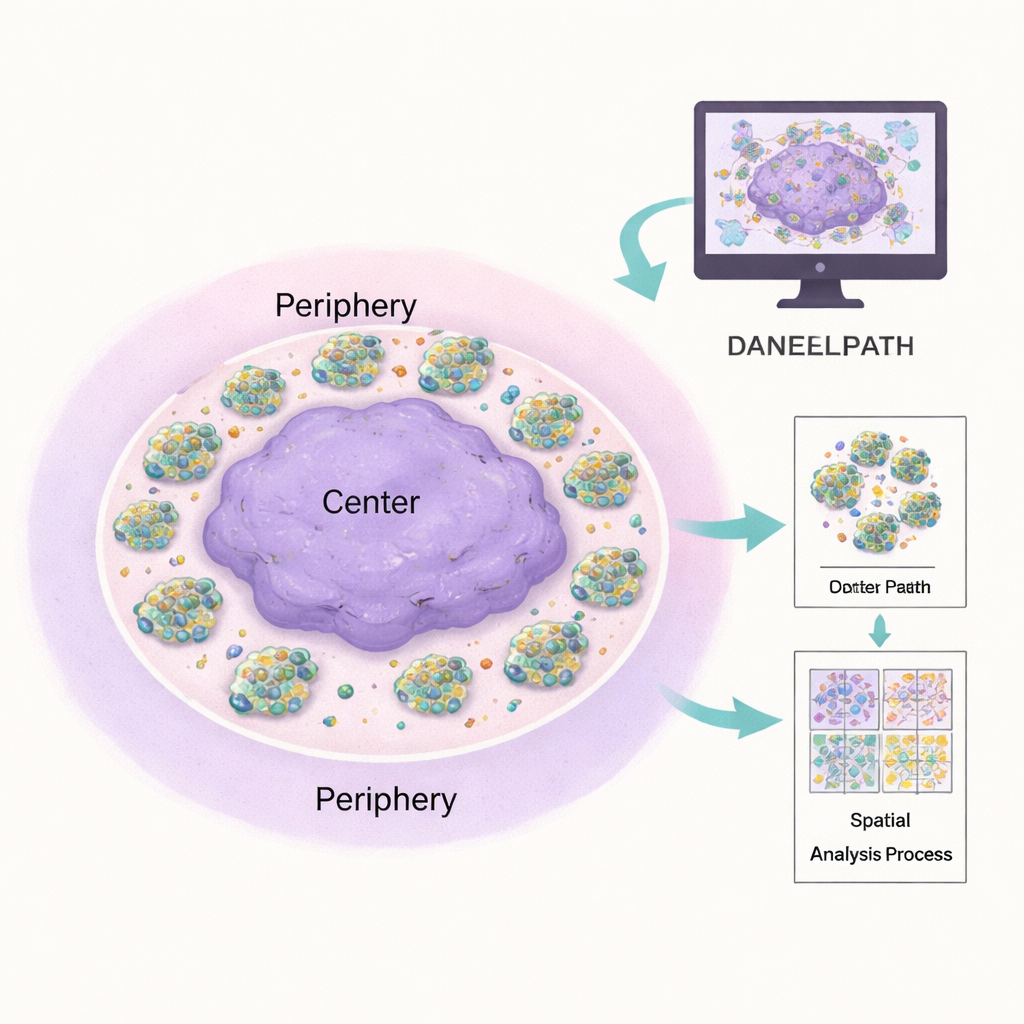
La patologia tradizionale si basa sull’occhio esperto al microscopio, che è potente ma difficile da standardizzare e scalare. DANEELpath si integra con la popolare piattaforma open source QuPath e automatizza gran parte di questo lavoro. Utilizzando modelli di deep learning chiamati U-Net, il toolkit può delineare con precisione ogni ammasso cellulare in colorazioni comuni, anche quando gli aggregati variano da poche cellule a centinaia. Applica quindi metodi matematici per suddividere ogni idrogel dalla forma irregolare in un anello “centrale” e un anello “periferico” bilanciati, assicurando che i confronti tra regioni interne ed esterne siano equi indipendentemente dalla forma del gel. Questo ha permesso agli autori di confermare che gli aggregati di neuroblastoma tendono a essere più densi verso il bordo dell’idrogel e che questo schema cambia a seconda del contenuto di vitronectina e del trattamento farmacologico.
Misurare la distanza tra le cellule e i vicini degli aggregati
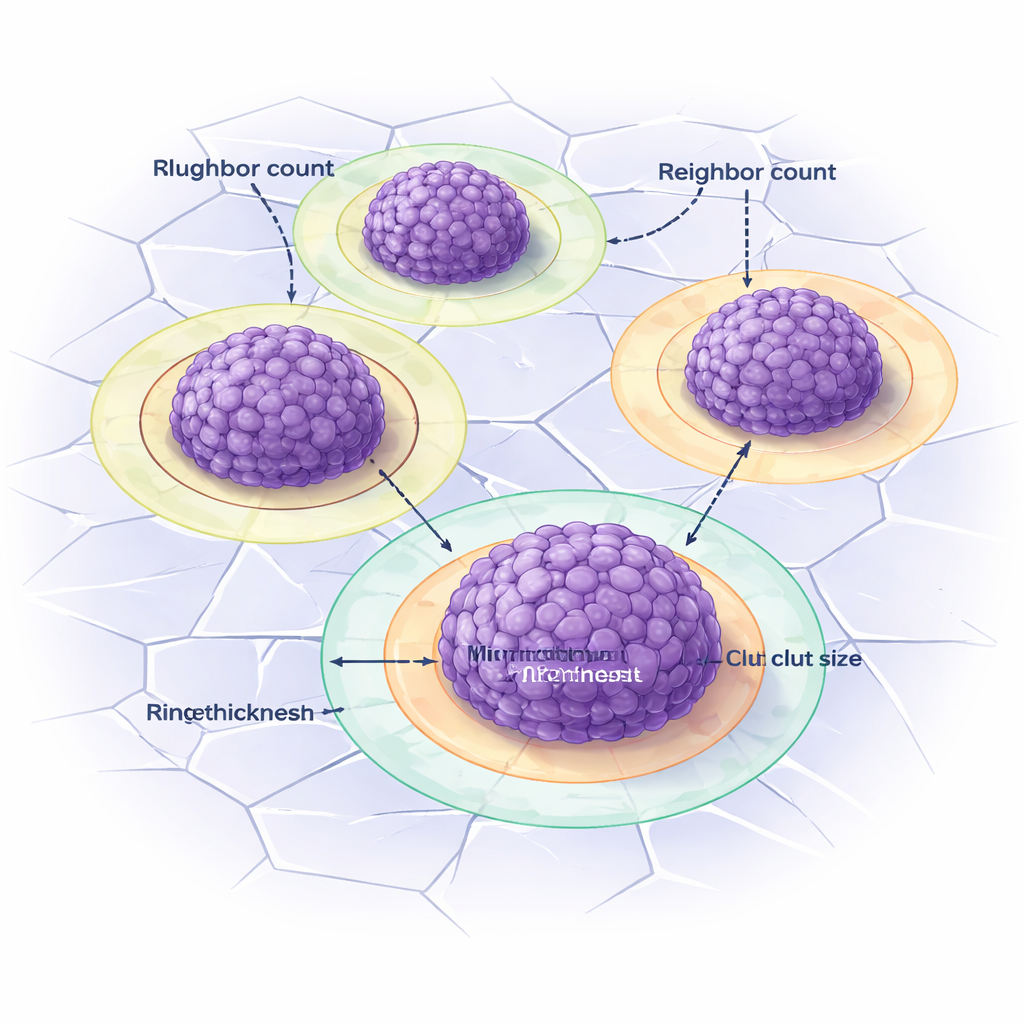
Oltre al conteggio degli aggregati, DANEELpath analizza come cellule e ammassi sono disposti nello spazio. All’interno di ogni aggregato, un altro strumento individua i singoli nuclei cellulari e misura la distanza dal vicino più prossimo, riassumendo quanto siano compatte le cellule. Tra gli aggregati, il toolkit offre tre modi per definire i “vicini”, incluso un metodo basato sui diagrammi di Voronoi che traccia zone di influenza attorno a ciascun aggregato. Confrontando queste misure in condizioni diverse, i ricercatori hanno mostrato che il cilengitide modifica il numero di aggregati vicini a un grande ammasso e la loro distribuzione, ma in modi che dipendono dalla presenza o meno di vitronectina nel gel. Questo evidenzia come la matrice circostante e i farmaci meccanici modellino insieme l’organizzazione tumorale.
Vedere l’alone attorno agli aggregati tumorali
La vitronectina in questi modelli spesso forma anelli evidenti attorno agli aggregati: una brillante “corona” quando è presente solo la vitronectina prodotta dalle cellule e un alone pallido quando la vitronectina è incorporata nel gel. Separare questi anelli dal nucleo dell’aggregato è difficile a occhio nudo. DANEELpath affronta il problema disegnando prima regioni di influenza basate sui Voronoi attorno a ciascun aggregato, quindi espandendole verso l’esterno quanto basta per catturare l’anello senza sovrapporsi ai vicini. Regole semplici basate sul contrasto d’immagine vengono usate per rilevare corone e aloni, e il toolkit misura automaticamente il loro spessore. Strategie simili sono state applicate anche a campioni umani, ad esempio mappando le cellule immunitarie al margine delle regioni tumorali o definendo zone attorno ai vasi sanguigni per studiare come la vitronectina e altri marker siano disposti nei neuroblastomi pediatrici.
Cosa significa per la ricerca sul cancro futura
In sostanza, questo lavoro trasforma immagini patologiche statiche in misure dettagliate e riproducibili di come le cellule tumorali e il loro ambiente sono organizzate. Per i non specialisti, ciò significa che i ricercatori possono ora testare più facilmente come nuovi farmaci, materiali di impalcatura o modifiche genetiche alterino non solo se i tumori crescono, ma come crescono nello spazio. Poiché DANEELpath è open source, funziona tramite un’interfaccia grafica ed è eseguibile su computer comuni, abbassa la barriera per i laboratori di tutto il mondo che vogliano adottare analisi d’immagine avanzate. Col tempo, strumenti di questo tipo potrebbero aiutare a collegare i pattern osservati nei modelli 3D e nei tessuti dei pazienti agli esiti clinici, guidando terapie più mirate ed efficaci per i bambini con neuroblastoma ad alto rischio.
Citazione: Vieco-Martí, I., López-Carrasco, A., Navarro, S. et al. DANEELpath open source digital analysis tools for histopathological research in neuroblastoma models. Sci Rep 16, 6162 (2026). https://doi.org/10.1038/s41598-026-37134-5
Parole chiave: neuroblastoma, patologia digitale, idrogel 3D, matrice extracellulare, deep learning