Clear Sky Science · it
Le LncRNA associate alla senescenza TRMP e TRMP-S promuovono il carcinoma gastrico attivando IGFL4
Perché questa ricerca è importante
Il cancro dello stomaco (gastrico) resta uno dei tumori più letali al mondo, in gran parte perché spesso viene diagnosticato in fase avanzata e può essere difficile da trattare. Questo studio rivela come due molecole genetiche poco conosciute, chiamate TRMP e TRMP-S, favoriscano la crescita e la diffusione dei tumori gastrici. Spiegando la catena di eventi che attivano all’interno delle cellule tumorali e nell’ambiente immunitario del tumore, il lavoro indica nuove strade che un giorno potrebbero aiutare i medici a diagnosticare prima i pazienti e a progettare terapie mirate più efficaci.
Messaggi nascosti nel nostro DNA
La maggior parte delle persone pensa ai geni come piani per produrre proteine, ma il nostro DNA genera anche RNA lunghi non codificanti (lncRNA) che non traducono proteine eppure influenzano profondamente il comportamento cellulare. TRMP e la sua variante di splicing più corta TRMP-S sono due di questi lncRNA. In precedenza erano stati collegati all’invecchiamento e al controllo del ciclo cellulare in cellule polmonari e del colon, ma il loro ruolo nel cancro gastrico era sconosciuto. Poiché i lncRNA possono fungere da marcatori diagnostici e da bersagli terapeutici, gli autori hanno cercato di capire se TRMP e TRMP-S spingano le cellule gastriche verso la trasformazione tumorale e come interagiscano con altre molecole per farlo.
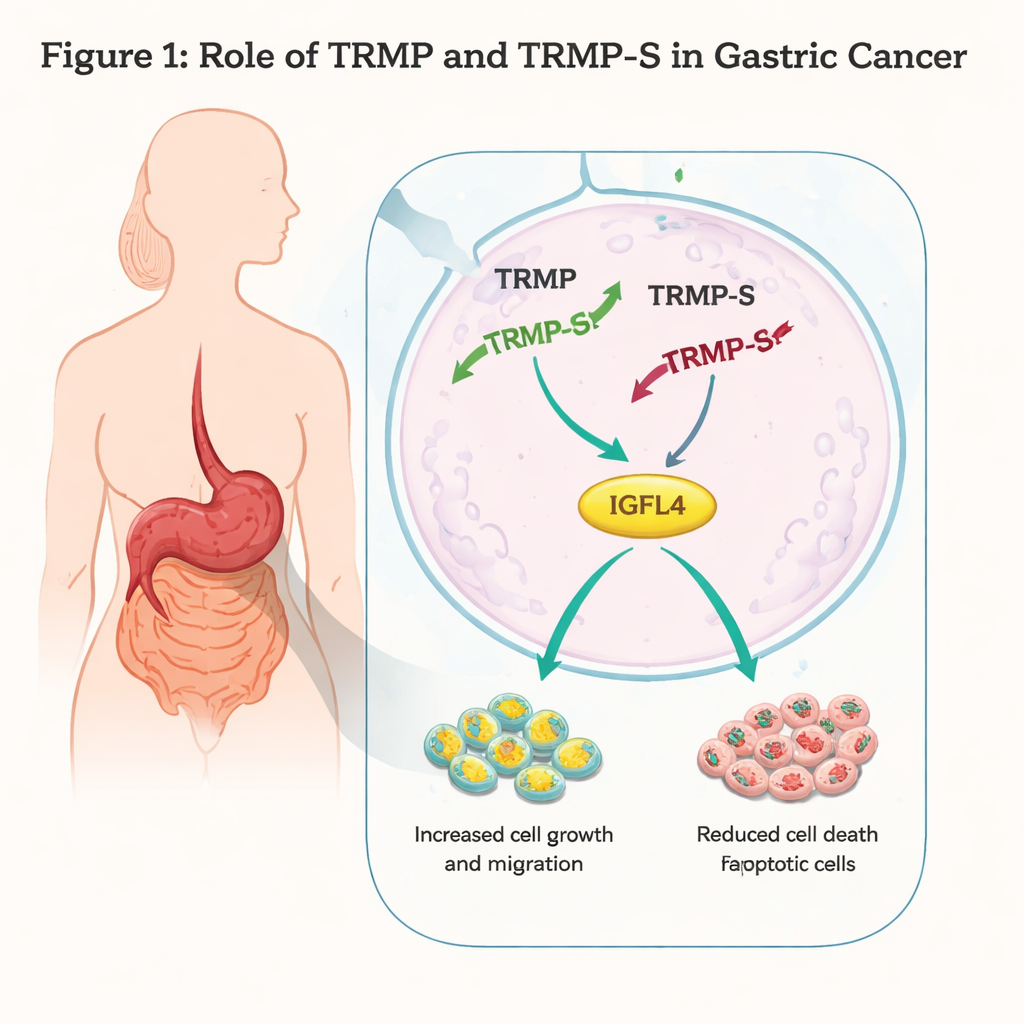
Spegnere un acceleratore del cancro
I ricercatori hanno lavorato con due linee cellulari umane di cancro gastrico, AGS e MKN45, e hanno usato strumenti genetici per ridurre i livelli di TRMP-S e TRMP. Quando hanno silenziato TRMP-S, le cellule tumorali crescevano più lentamente, formavano meno colonie e avevano una ridotta capacità di migrare attraverso barriere artificiali o di chiudere ferite in coltura. La citometria a flusso e le analisi proteiche hanno mostrato un aumento delle cellule in apoptosi (morte cellulare programmata) e un arresto del ciclo cellulare in fase G1, un checkpoint chiave prima della replicazione del DNA. I livelli di p73, un membro della famiglia del soppressore tumorale p53, aumentavano quando TRMP-S veniva eliminato, coerente con un maggiore controllo del ciclo cellulare e più morte cellulare. Nel complesso questi risultati indicano che TRMP-S agisce normalmente come un pedale dell’acceleratore per le cellule del cancro gastrico.
Un partner chiave: il segnale IGFL4
Per capire come TRMP e TRMP-S esercitino i loro effetti, il team ha analizzato grandi dataset di pazienti provenienti da The Cancer Genome Atlas e da una coorte coreana di carcinoma gastrico. Hanno cercato geni sia anormalmente elevati nei tumori sia positivamente correlati ai livelli di TRMP, costruendo poi un modello di rischio a sei geni in grado di predire la sopravvivenza dei pazienti—punteggi più alti erano associati a esiti peggiori. Tra questi geni, uno si distingueva: IGFL4, membro di una famiglia correlata ai fattori di crescita simili all’insulina, noti per promuovere crescita e sopravvivenza in molti tumori. Nelle cellule di cancro gastrico, l’abbattimento di TRMP-S riduceva nettamente i livelli di RNA e proteina di IGFL4, mentre un saggio di immunoprecipitazione dell’RNA mostrava che sia TRMP sia TRMP-S si legano fisicamente alla proteina IGFL4. La riduzione diretta di TRMP produceva lo stesso effetto attenuante su IGFL4, suggerendo che questi lncRNA aiutano a stabilizzare o favorire la produzione di questo segnale che promuove la crescita.
Rallentare la diffusione e rimodellare il panorama immunitario
Quando i ricercatori hanno usato piccoli RNA interferenti per silenziare direttamente IGFL4, le cellule di cancro gastrico rallentavano nella crescita, migravano meno e mostrato una minore capacità di invadere membrane e chiudere ferite. L’analisi dei dati tumorali dei pazienti ha rivelato che i livelli di IGFL4 erano significativamente più alti nei tumori gastrici rispetto al tessuto gastrico normale, ed elevati in molti altri tipi di tumore. Importante, i tumori con alta espressione di IGFL4 mostravano pattern distinti di infiltrazione delle cellule immunitarie: più macrofagi indifferenziati (M0) e meno plasmacellule, monociti, eosinofili e neutrofili. Punteggi immunitari computazionali suggerivano che i tumori con alto IGFL4 potrebbero rispondere meglio alle immunoterapie moderne che bloccano i checkpoint immunitari, indicando che IGFL4 potrebbe aiutare a identificare i pazienti candidati a questi trattamenti.
Un piccolo RNA che contrasta
Lo studio ha anche individuato un contrappeso a questa via promotrice di tumore. Correlando l’espressione di microRNA e geni nei dati dei pazienti, gli autori hanno identificato miR-129-5p come un piccolo RNA negativamente correlato sia a TRMP sia a IGFL4. Nelle cellule di cancro gastrico, l’aggiunta di miR-129-5p riduceva i livelli di IGFL4 e rallentava la crescita, mentre il blocco di miR-129-5p aumentava IGFL4 e accelerava la proliferazione. Un’altra microRNA candidata, miR-4739, non influenzava misurabilmente IGFL4 ed è stata esclusa. Questi risultati supportano una catena regolatoria in cui TRMP e TRMP-S, miR-129-5p e IGFL4 formano una rete che modula quanto aggressivamente le cellule di cancro gastrico crescono e come interagiscono con il loro ambiente.
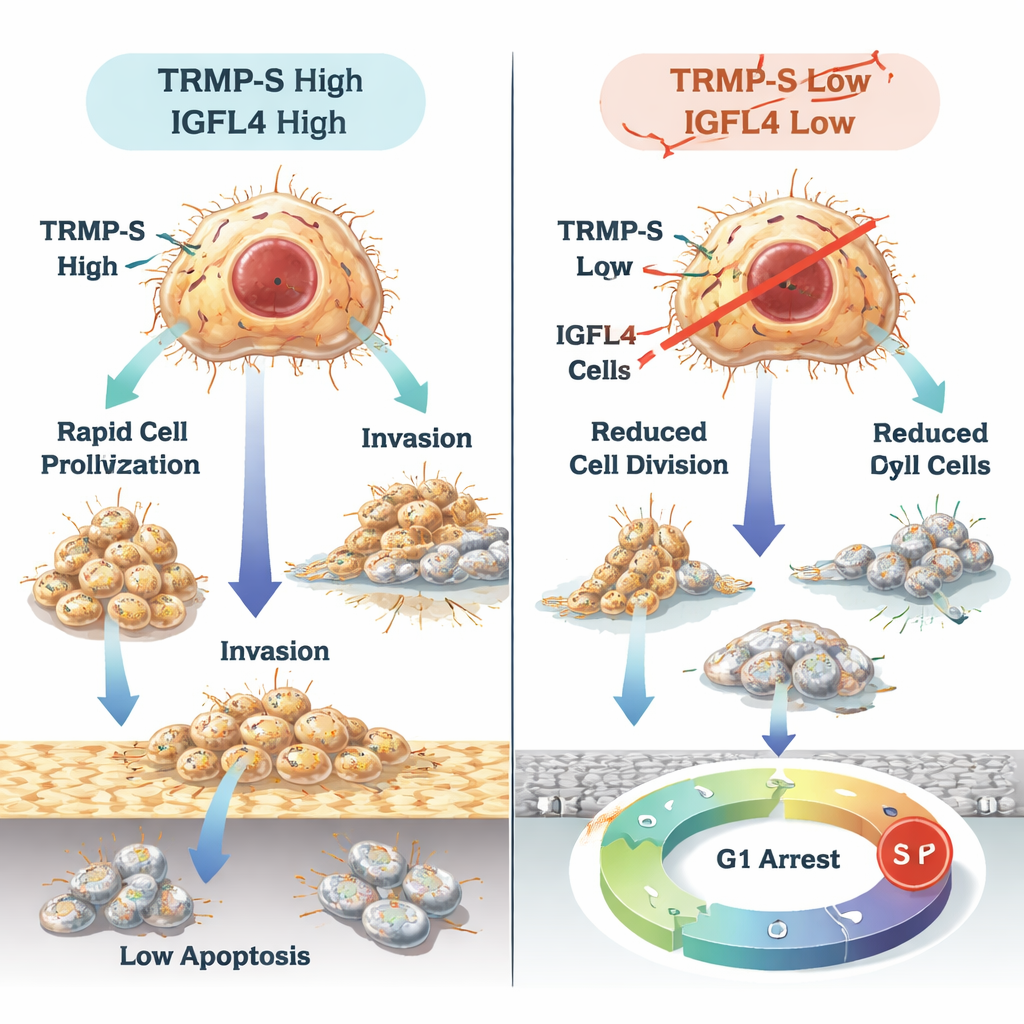
Cosa potrebbe significare per i pazienti
In termini semplici, questo lavoro mostra che TRMP e TRMP-S agiscono come direttori dietro le quinte che attivano IGFL4 e favoriscono la crescita, la diffusione e l’elusione dei meccanismi di freno naturali nelle cellule del cancro gastrico. Allo stesso tempo, il piccolo RNA miR-129-5p funge da freno su IGFL4, e IGFL4 stesso contribuisce a modellare come le cellule immunitarie si raccolgono attorno ai tumori e quanto bene possano funzionare le terapie che risvegliano il sistema immunitario. Sebbene siano necessarie ulteriori ricerche e sperimentazioni cliniche, TRMP, TRMP-S, IGFL4 e miR-129-5p rappresentano insieme un insieme promettente di marcatori prognostici e potenziali nuovi bersagli farmacologici per rallentare o arrestare il cancro gastrico.
Citazione: Zhang, M., Mi, Y., Li, F. et al. Senescence-associated LncRNAs TRMP and TRMP-S promote gastric cancer by activating IGFL4. Sci Rep 16, 6740 (2026). https://doi.org/10.1038/s41598-026-37106-9
Parole chiave: cancro gastrico, RNA lungo non codificante, TRMP, IGFL4, microambiente tumorale